2020-2021学年第一节 酸及其性质综合训练题
展开1.(目标2)下列选项中有关物质的用途错误的是( )
A.①②③ B.②③④ C.①②④ D.③④
2.(目标1)下列物质长期露置在空气中,质量会减少的是( )
A.NaCl B.浓硫酸 C.浓盐酸 D.碳酸钙
3.(目标1)下列说法正确的是( )
A.浓盐酸敞口放置一段时间后,溶液的质量增加
B.浓盐酸在空气中会冒白烟
C.浓硫酸敞口放置一段时间后,溶液的溶质质量会减小
D.浓硫酸敞口放置一段时间后,溶液的溶质质量分数会减小
4.(目标1)下列关于盐酸的描述,错误的是( )
A.盐酸中的溶质是HCl
B.盐酸能使石蕊试液变红
C.盐酸与硫酸的化学性质完全相同
D.打开装有浓盐酸的试剂瓶瓶盖,瓶口处有白雾出现
5.(目标2)不能用金属跟酸直接反应得到的物质是( )
A.FeCl2 B.ZnCl2 C.FeCl3 D.MgSO4
6.(目标1、2)盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质。下列有关叙述正确的是( )
A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.在稀盐酸、稀硫酸中加入碳酸钙粉末,粉末都会逐渐溶解,且液体变为黄色
7.(目标2)物质X可发生下列所示的两个反应,则X可能是( )
①X+金属→盐+H2↑②X+金属氧化物→盐+H2O
A.CaO B.CO2 C.CO D.H2SO4
8.(目标1、2)下列有关酸的性质及应用的叙述正确的是( )
A.由于盐酸能和金属反应,所以不能用于金属除锈
B.浓硫酸沾到手上可用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液
C.由于浓硫酸具有脱水性,所以常用作某些气体的干燥剂
D.稀释浓硫酸时,应将水注入浓硫酸中
9.(目标3)下列反应属于复分解反应的是( )
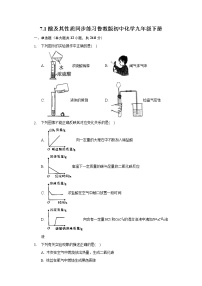
10.(目标2)下列是关于盐酸和硫酸性质的研究实验,请回答下列问题。
(1)图1实验过程中的现象是__________________________________________。
(2)图2中电子天平上表面皿中盛有浓H2SO4,放置一段时间,天平示数变化如图乙所示,说明浓硫酸具有________性。
(3)图3中的操作存在一处错误,请改正:__________________________________。
【化学用语天天练】
请写出下列反应的化学方程式:
铁和稀硫酸反应:_________________________________________________
氧化铁和稀盐酸反应:_____________________________________________
氧化铜和稀硫酸反应:______________________________________________
大理石与稀盐酸反应:______________________________________________
碳酸钠与稀盐酸反应:_______________________________________________
答案解析
1. eq \a\vs4\al(A) 2. eq \a\vs4\al(C) 3. eq \a\vs4\al(D) 4. eq \a\vs4\al(C)
5. eq \a\vs4\al(C) Fe和稀盐酸反应可生成FeCl2,不会生成FeCl3;Zn和稀盐酸反应可生成ZnCl2;Mg和稀硫酸反应可生成MgSO4。
6. eq \a\vs4\al(B) 7. eq \a\vs4\al(D) 8. eq \a\vs4\al(B)
9. eq \a\vs4\al(B) A、由微观模型图可以看出:是由一种单质和一种化合物反应,生成另一种单质和另一种化合物,属于置换反应,故错;B、由微观模型图可以看出:属于两种化合物交换成分生成另外两种化合物的复分解反应,故对;C、由微观模型图可以看出:属于一种化合物和一种单质生成另一种化合物的化合反应,故错;D、由微观模型图可以看出:属于一种化合物生成两种单质的分解反应,故错。
10.【解析】(1)浓盐酸具有挥发性,挥发出来的氯化氢气体进入A烧杯形成盐酸,使石蕊溶液变红色。(2)电子天平上表面皿中盛有浓H2SO4,放置一段时间,溶液质量增加,是因为吸收了空气中的水蒸气,说明浓硫酸具有吸水性。(3)稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;切不可把水注入浓硫酸中,这是因为浓硫酸的密度比水大,如果添加顺序颠倒,那么水会浮在浓硫酸上,又由于浓硫酸溶于水放出大量的热,能使水沸腾,容易造成酸液飞溅。
答案:(1)A烧杯中石蕊溶液变红色 (2)吸水 (3)将浓硫酸缓缓地沿器壁注入水中
【化学用语天天练】
Fe + H2SO4 ===FeSO4 + H2↑
Fe2O3 + 6HCl ===2FeCl3 + 3H2O
CuO + H2SO4 ===CuSO4 + H2O
CaCO3 + 2HCl ===CaCl2 + H2O + CO2↑
Na2CO3+ 2HCl ===2NaCl + H2O + CO2↑
初中化学鲁教版九年级下册第一节 酸及其性质达标测试: 这是一份初中化学鲁教版九年级下册<a href="/hx/tb_c91622_t7/?tag_id=28" target="_blank">第一节 酸及其性质达标测试</a>,共12页。试卷主要包含了选择题,判断题,综合应用题等内容,欢迎下载使用。
初中化学鲁教版九年级下册第一节 酸及其性质同步练习题: 这是一份初中化学鲁教版九年级下册第一节 酸及其性质同步练习题,共13页。试卷主要包含了已知等内容,欢迎下载使用。
初中化学鲁教版九年级下册第一节 酸及其性质测试题: 这是一份初中化学鲁教版九年级下册第一节 酸及其性质测试题,共9页。试卷主要包含了1酸及其性质,6%等内容,欢迎下载使用。