
初中化学鲁教版九年级下册第一节 酸及其性质同步练习题
展开这是一份初中化学鲁教版九年级下册第一节 酸及其性质同步练习题,共13页。试卷主要包含了已知等内容,欢迎下载使用。
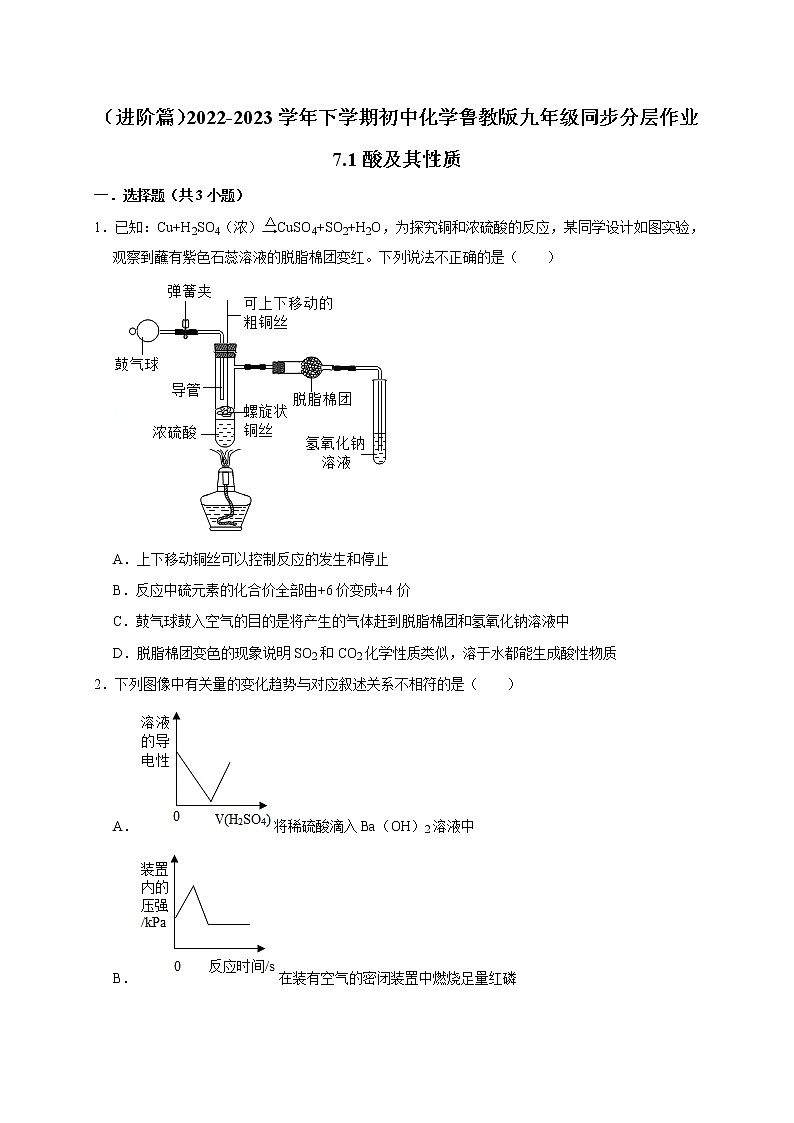
1.已知:Cu+H2SO4(浓)CuSO4+SO2+H2O,为探究铜和浓硫酸的反应,某同学设计如图实验,观察到蘸有紫色石蕊溶液的脱脂棉团变红。下列说法不正确的是( )
A.上下移动铜丝可以控制反应的发生和停止
B.反应中硫元素的化合价全部由+6价变成+4价
C.鼓气球鼓入空气的目的是将产生的气体赶到脱脂棉团和氢氧化钠溶液中
D.脱脂棉团变色的现象说明SO2和CO2化学性质类似,溶于水都能生成酸性物质
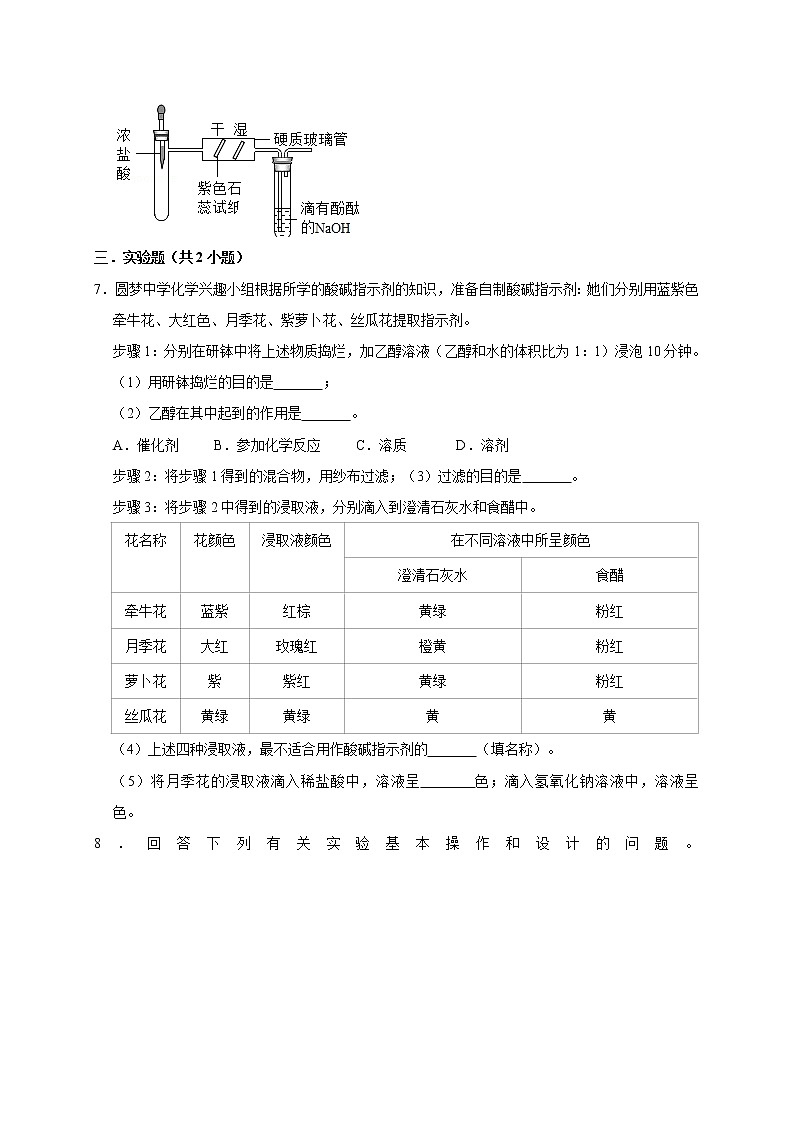
2.下列图像中有关量的变化趋势与对应叙述关系不相符的是( )
A.将稀硫酸滴入Ba(OH)2溶液中
B.在装有空气的密闭装置中燃烧足量红磷
C.在101KPa时,氧气的溶解度曲线
D.将等质量等浓度的稀硫酸分别与足量MgO和MgCO3中,充分反应
3.构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“﹣”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
A.CO2、Ba(OH)2、CuSO4B.Ba(OH)2、HNO3、K2CO3
C.KOH、FeCl3、CaCO3 D.NaOH、BaCl2、H2SO4
二.填空题(共3小题)
4.纯净的浓盐酸是 色的,有 气味的液体,打开瓶塞会看到 ,产生此现象的原因是 敞口放置质量会 ,质量分数会 .
5.我们要学会用一分为二的观点解释一些问题。例如我们的胃液中含有盐酸,它既有助于消化作用,但盐酸过多也可能引起胃部不适,盐酸过多时可用小苏打治疗,反应的化学方程式为 ,反应前后一定没有变化的离子是 (用离子符号表示)。
6.根据如图装置进行实验,探究盐酸的某些性质。滴入浓盐酸后,观察到硬质玻璃管中的现象为 ;右侧试管内溶液由红色变为无色,溶液中除含有酚酞、水外,一定含有的物质为 ;请选用一种试剂来检验可能存在的物质,写出反应的化学方程式 (合理即可)。
三.实验题(共2小题)
7.圆梦中学化学兴趣小组根据所学的酸碱指示剂的知识,准备自制酸碱指示剂:她们分别用蓝紫色牵牛花、大红色、月季花、紫萝卜花、丝瓜花提取指示剂。
步骤1:分别在研钵中将上述物质捣烂,加乙醇溶液(乙醇和水的体积比为1:1)浸泡10分钟。
(1)用研钵捣烂的目的是 ;
(2)乙醇在其中起到的作用是 。
A.催化剂 B.参加化学反应 C.溶质 D.溶剂
步骤2:将步骤1得到的混合物,用纱布过滤;(3)过滤的目的是 。
步骤3:将步骤2中得到的浸取液,分别滴入到澄清石灰水和食醋中。
(4)上述四种浸取液,最不适合用作酸碱指示剂的 (填名称)。
(5)将月季花的浸取液滴入稀盐酸中,溶液呈 色;滴入氢氧化钠溶液中,溶液呈 色。
8.回答下列有关实验基本操作和设计的问题。
(1)量取18.0mL蒸馏水,最好选用的量筒规格是 (填序号)。
A 5mL B.10mL C.25mL D.100mL
(2)向如图1所示烧杯中,加入适量的 (填序号),可能引燃铜片上的白磷。
A.浓硫酸 B.硝酸铵 C.氯化钠
(3)探究紫色石蕊变色规律的实验中,往点滴板1﹣6号的孔穴中先加入如图2所示的试剂,分别滴入2滴紫色石蕊溶液。其中作为空白对照实验的是孔穴 (填孔穴编号)
(4)实验室常用较浓的过氧化氢溶液与二氧化锰制氧气。
①反应的化学方程式为 。
②实验中,为了得到平稳的气流,最适合的装置组合(如图3)是 (填序号)。
四.推断题(共1小题)
9.构建知识网格,可以帮助理解知识间的内在联系,如图是盐酸与不同类别物质之间反应的知识网格
(1)图中M应为 类物质。
(2)写出一种能与盐酸反应的盐 。
(3)用盐酸除铁锈(主要成分Fe2O3)的化学方程式是 。
五.解答题(共1小题)
10.在2019年年底开始,我国爆发了新冠肺炎,给国家和人民的财产带来巨大的损失,给人民的生命带来严重的威胁,全国人民在党中央的领导下众志成城抗击新冠肺炎。抗疫中用到了许多消毒剂,过氧乙酸溶液以及84消毒液【有效成分为次氯酸钠和二氧化氯(ClO2)】是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式,其反应原理:Cl2+2NaOH═NaCl+H2O+ 。
(2)二氧化氯(ClO2)中氯元素的化合价 ,该物质由 (选填“分子”、“原子”或“离子”)构成。
(3)过氧乙酸溶液中通常含有过氧化氢、醋酸等物质,向过氧乙酸溶液中加入下列物质,不能产生气体的是 。
A.Al
B.NaCl
C.Na2CO3
D.MnO2
(进阶篇)2022-2023学年下学期初中化学鲁教版九年级同步分层作业
7.1酸及其性质
参考答案与试题解析
一.选择题(共3小题)
1.已知:Cu+H2SO4(浓)CuSO4+SO2+H2O,为探究铜和浓硫酸的反应,某同学设计如图实验,观察到蘸有紫色石蕊溶液的脱脂棉团变红。下列说法不正确的是( )
A.上下移动铜丝可以控制反应的发生和停止
B.反应中硫元素的化合价全部由+6价变成+4价
C.鼓气球鼓入空气的目的是将产生的气体赶到脱脂棉团和氢氧化钠溶液中
D.脱脂棉团变色的现象说明SO2和CO2化学性质类似,溶于水都能生成酸性物质
【解答】解:A、拉动铜丝,可以控制铜与浓硫酸是否接触,控制反应是否发生和停止,选项A正确;
B、反应中硫元素生成了硫酸铜和二氧化硫,硫元素在硫酸铜中化合价没有变化,部分由+6价变为+4价,选项B不正确;
C、鼓入空气可以将内部残留的二氧化硫排出,此时使气体进入脱脂棉团和氢氧化钠溶液中,选项C正确;
D、二氧化硫与水反应生成亚硫酸,溶液显酸性,使脱脂棉团变色,选项D正确;
故选:B。
2.下列图像中有关量的变化趋势与对应叙述关系不相符的是( )
A.将稀硫酸滴入Ba(OH)2溶液中
B.在装有空气的密闭装置中燃烧足量红磷
C.在101KPa时,氧气的溶解度曲线
D.将等质量等浓度的稀硫酸分别与足量MgO和MgCO3中,充分反应
【解答】解:A、氢氧化钡与硫酸反应生成硫酸钡沉淀和水,随着硫酸加入,离子浓度降低,导电性降低,当全部反应后,没有离子存在,导电性为零,之后再加入硫酸,离子浓度增大,导电性增强,选项A正确;
B、燃烧刚开始温度升高,内部压强增大,随着反应进行,气体减少,且反应慢慢停止,温度开始下降,压强减小,直至反应完毕,压强降至最低,不再变化,选项B正确;
C、气体溶解度在压强一定是,温度升高溶解度下降,选项C正确;
D、硫酸与氧化镁反应生成硫酸镁和水,硫酸与碳酸镁反应生成硫酸镁、二氧化碳和水,氧化镁相对分子质量小于碳酸镁,因此相同质量固体消耗硫酸的质量为碳酸镁大于氧化镁,相同质量的氧化镁和碳酸镁,与硫酸反应后生成硫酸镁的质量为氧化镁大于碳酸镁,最后硫酸全部反应质量不再变化,选项D错误;
故选:D。
3.构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“﹣”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
A.CO2、Ba(OH)2、CuSO4B.Ba(OH)2、HNO3、K2CO3
C.KOH、FeCl3、CaCO3 D.NaOH、BaCl2、H2SO4
【解答】解:A、A为二氧化碳不能与盐酸反应,C为硫酸铜也不与盐酸反应,选项A错误;
B、A氢氧化钡与盐酸发生酸碱中和反应,B硝酸与A氢氧化钡可以发生酸碱中和反应,B硝酸与C碳酸钾反应生成硝酸钾、二氧化碳和水,盐酸与硝酸银反应生成硝酸和氯化银,盐酸与碳酸钾反应生成氯化钾、二氧化碳和水,满足上述逻辑框图关系,选项B正确;
C、C碳酸钙与B氯化铁不发生反应,选项C错误;
D、A氢氧化钠与B氯化钡不发生反应,盐酸与C硫酸不反应,选项D错误;
故选:B。
二.填空题(共3小题)
4.纯净的浓盐酸是 无 色的,有 刺激性 气味的液体,打开瓶塞会看到 瓶口有白雾 ,产生此现象的原因是 浓盐酸具有挥发性 敞口放置质量会 减小 ,质量分数会 减小 .
【解答】解:纯净的浓盐酸是无色的,有刺激性气味的液体;浓盐酸具有挥发性,打开瓶塞观察到瓶口有白雾,敞口放置的浓盐酸由于挥发出溶质氯化氢导致溶液质量减小,溶质质量分数减小,故填:无;刺激性;瓶口有白雾;浓盐酸具有挥发性,减小,减小.
5.我们要学会用一分为二的观点解释一些问题。例如我们的胃液中含有盐酸,它既有助于消化作用,但盐酸过多也可能引起胃部不适,盐酸过多时可用小苏打治疗,反应的化学方程式为 HCl+NaHCO3=NaCl+H2O+CO2↑ ,反应前后一定没有变化的离子是 Na+、Cl﹣ (用离子符号表示)。
【解答】解:小苏打为碳酸氢钠的俗称,盐酸与碳酸氢钠反应生成氯化钠、水和二氧化碳,书写化学方程式注意配平及气体符号,所以化学方程式为HCl+NaHCO3=NaCl+H2O+CO2↑;反应前盐酸含有氯离子,碳酸氢钠溶液含有钠离子,反应后氯化钠含有钠离子和氯离子,因此钠离子和氯离子反应前后不变;
故答案为:HCl+NaHCO3=NaCl+H2O+CO2↑;Na+、Cl﹣。
6.根据如图装置进行实验,探究盐酸的某些性质。滴入浓盐酸后,观察到硬质玻璃管中的现象为 干的紫色石蕊试纸不变色,湿的紫色石蕊试纸变红 ;右侧试管内溶液由红色变为无色,溶液中除含有酚酞、水外,一定含有的物质为 氯化钠 ;请选用一种试剂来检验可能存在的物质,写出反应的化学方程式 2HCl+Zn=ZnCl2+H2↑ (合理即可)。
【解答】解:酸能是紫色石蕊变红,氯化氢气体不显酸性,氯化氢溶于水显酸性,故干的紫色石蕊试纸不变色,湿的紫色石蕊试纸变红;氢氧化钠和稀盐酸生成氯化钠和水,溶液中除含有酚酞、水外,一定含有的物质为氯化钠,由于酚酞变为无色,所以溶液不显碱性,因此没有氢氧化钠,可能含有稀盐酸,稀盐酸可以用活泼的金属单质或碳酸盐等检验,稀盐酸和锌反应生成氯化锌和氢气,反应的化学方程式为:2HCl+Zn=ZnCl2+H2↑;
故答案为:干的紫色石蕊试纸不变色,湿的紫色石蕊试纸变红;2HCl+Zn=ZnCl2+H2↑。
三.实验题(共2小题)
7.圆梦中学化学兴趣小组根据所学的酸碱指示剂的知识,准备自制酸碱指示剂:她们分别用蓝紫色牵牛花、大红色、月季花、紫萝卜花、丝瓜花提取指示剂。
步骤1:分别在研钵中将上述物质捣烂,加乙醇溶液(乙醇和水的体积比为1:1)浸泡10分钟。
(1)用研钵捣烂的目的是 便于提取汁液 ;
(2)乙醇在其中起到的作用是 D 。
A.催化剂 B.参加化学反应 C.溶质 D.溶剂
步骤2:将步骤1得到的混合物,用纱布过滤;(3)过滤的目的是 滤出汁液作指示剂 。
步骤3:将步骤2中得到的浸取液,分别滴入到澄清石灰水和食醋中。
(4)上述四种浸取液,最不适合用作酸碱指示剂的 丝瓜花 (填名称)。
(5)将月季花的浸取液滴入稀盐酸中,溶液呈 粉红 色;滴入氢氧化钠溶液中,溶液呈 橙黄 色。
【解答】解:(1)将花捣烂能获取花的汁液;
(2)乙醇能作为溶剂使花汁溶解从而获得花汁的溶液,故为D;
(3)使用纱布过滤能除去花的碎屑得到花汁的浸取液;
(4)根据表格提供的信息可知,丝瓜花的汁液在酸碱溶液中的颜色一样,不能用作酸碱指示剂;
(5)月季花的汁液在酸性溶液中为粉红色,在碱性溶液中为橙黄色,故加入盐酸呈粉红色,加入氢氧化钠溶液呈橙黄色;
故答案为:(1)便于提取汁液;(2)D;(3)滤出汁液作指示剂;(4)丝瓜花;(5)粉红;橙黄。
8.回答下列有关实验基本操作和设计的问题。
(1)量取18.0mL蒸馏水,最好选用的量筒规格是 C (填序号)。
A 5mL B.10mL C.25mL D.100mL
(2)向如图1所示烧杯中,加入适量的 A (填序号),可能引燃铜片上的白磷。
A.浓硫酸 B.硝酸铵 C.氯化钠
(3)探究紫色石蕊变色规律的实验中,往点滴板1﹣6号的孔穴中先加入如图2所示的试剂,分别滴入2滴紫色石蕊溶液。其中作为空白对照实验的是孔穴 1 (填孔穴编号)
(4)实验室常用较浓的过氧化氢溶液与二氧化锰制氧气。
①反应的化学方程式为 2H2O22H2O+O2↑ 。
②实验中,为了得到平稳的气流,最适合的装置组合(如图3)是 AD (填序号)。
【解答】解:(1)25mL量筒量取18.0mL蒸馏水,能保证测量一次,且量程与液体的取用量最接近,误差最小;故填:C;
(2)要引燃铜片上的白磷,该物质溶于水需放出热量,浓硫酸溶于水放热,硝酸铵溶于水吸热,氯化钠溶于水温度几乎不变;故填:A;
(3)探究紫色石蕊变色规律的实验中,就是根据石蕊试液遇到酸性溶液和碱性溶液的颜色变化,1中的水为中性,紫色石蕊不变色,起对照作用;故填:1;
(4)①过氧化氢在二氧化锰的催化作用下分解为水和氧气;故填:2H2O22H2O+O2↑;
②实验中,为了得到平稳的气流,最适合的装置组合AD,通过注射器来控制过氧化氢溶液的加入速率,进而控制反应的速率得到平稳的气流;故填:AD。
四.推断题(共1小题)
9.构建知识网格,可以帮助理解知识间的内在联系,如图是盐酸与不同类别物质之间反应的知识网格
(1)图中M应为 碱 类物质。
(2)写出一种能与盐酸反应的盐 AgNO3 。
(3)用盐酸除铁锈(主要成分Fe2O3)的化学方程式是 6HCl+Fe2O3=2FeCl3+3H2O 。
【解答】解:(1)盐酸可与五类物质发生化学反应,图中M应为其中的碱类物质;
(2)能与盐酸反应的盐类可以是:碳酸盐或碳酸氢盐或AgNO3等,本题答案可以是:AgNO3;
(3)盐酸和氧化铁反应生成氯化铁和水,化学方程式为:6HCl+Fe2O3=2FeCl3+3H2O。
故答案为:(1)碱;
(2)AgNO3;
(3)6HCl+Fe2O3=2FeCl3+3H2O。
五.解答题(共1小题)
10.在2019年年底开始,我国爆发了新冠肺炎,给国家和人民的财产带来巨大的损失,给人民的生命带来严重的威胁,全国人民在党中央的领导下众志成城抗击新冠肺炎。抗疫中用到了许多消毒剂,过氧乙酸溶液以及84消毒液【有效成分为次氯酸钠和二氧化氯(ClO2)】是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式,其反应原理:Cl2+2NaOH═NaCl+H2O+ NaClO 。
(2)二氧化氯(ClO2)中氯元素的化合价 +4 ,该物质由 分子 (选填“分子”、“原子”或“离子”)构成。
(3)过氧乙酸溶液中通常含有过氧化氢、醋酸等物质,向过氧乙酸溶液中加入下列物质,不能产生气体的是 B 。
A.Al
B.NaCl
C.Na2CO3
D.MnO2
【解答】解:(1)反应前含有2个氯原子,2个钠原子,2个氢原子和2个氧原子,反应后目前有1个钠原子,1个氯原子,2个氢原子和1个氧原子,还需要1个钠原子,1个氯原子和1个氧原子,正好组成1分子次氯酸钠;
故答案为:NaClO。
(2)二氧化氯中氧元素为﹣2价,设氯元素化合价为x,x×1+(﹣2)×2=0,x=+4;二氧化氯含有两种元素,是由分子构成;
故答案为:+4;分子。
(3)A、铝可与醋酸反应生成氢气,选项A不符合题意;
B、氯化钠与过氧化氢和醋酸都不反应,无气体生成,选项B符合题意;
C、碳酸钠与醋酸反应生成二氧化碳,选项C不符合题意;
D、二氧化锰可以催化过氧化氢产生氧气,选项D不符合题意;
故答案为:B花名称
花颜色
浸取液颜色
在不同溶液中所呈颜色
澄清石灰水
食醋
牵牛花
蓝紫
红棕
黄绿
粉红
月季花
大红
玫瑰红
橙黄
粉红
萝卜花
紫
紫红
黄绿
粉红
丝瓜花
黄绿
黄绿
黄
黄
花名称
花颜色
浸取液颜色
在不同溶液中所呈颜色
澄清石灰水
食醋
牵牛花
蓝紫
红棕
黄绿
粉红
月季花
大红
玫瑰红
橙黄
粉红
萝卜花
紫
紫红
黄绿
粉红
丝瓜花
黄绿
黄绿
黄
黄
相关试卷
这是一份初中化学鲁教版九年级下册第三节 海水“制碱“复习练习题,共15页。试卷主要包含了3“海水”制碱等内容,欢迎下载使用。
这是一份初中化学鲁教版九年级下册第二节 海水“晒盐“当堂达标检测题,共15页。试卷主要包含了2“海水”晒盐,1).,3g,稀盐酸质量分数==14,9 g.等内容,欢迎下载使用。
这是一份九年级下册第四节 酸碱中和反应同步训练题,共21页。试卷主要包含了4酸碱中和反应等内容,欢迎下载使用。













