





- 第十一单元 课题1 第1课时 氯化钠 课件 课件 5 次下载
- 第十一单元 课题1 第2课时 碳酸钠、碳酸氢钠和碳酸钙 课件 课件 6 次下载
- 第十一单元《课题2 化学肥料》教案 教案 4 次下载
- 第十一单元《课题1 生活中常见的盐》教案 教案 6 次下载
- 第十二单元 课题1 人类重要的营养物质 课件 课件 5 次下载
初中人教版第十二单元 化学与生活课题3 有机合成材料精品课件ppt
展开A.HCl 和 Ca(OH)2
B.Na2CO3 和 H2SO4
C.Ca(OH)2 和 Na2CO3 D.KCl 和 CuSO4
A.在复分解反应中,没有单质参与B.化合反应一定要加热C.置换反应一定有新的单质生成D.中和反应一定有水生成
识的提高,市场上出现了“加碘盐”、“叶绿素锌钠盐”、“低钠盐”等。某种低钠盐由 NaCl、KCl、MgSO4 三种物质组成,用它进行以下实验(假设每步均恰好完全反应)。
(1)写出步骤①的化学方程式:________________________。(2)当 X 是 AgNO3 时,白色沉淀 C 是______,其化学方程式是:__________________________________(写其中的一条)。当 X 是 NaOH 时,白色沉淀 C 是__________,其化学方程式是:___________________________________。
5.食盐是人们生活中不可缺少的调味剂,随着人们健康意
MgSO4+BaCl2===MgCl2+BaSO4↓
NaCl+AgNO3===AgCl↓+NaNO3
MgCl2+2NaOH===Mg(OH)2↓+2NaCl
两种化合物相互交换成分,生成另外两种化合物的反应。2.反应特点
(1)简记:位交换;价不变。可以用通式表示:AB+CD―→
(2)属于四大基本反应类型。
(1)生成物中有气体、沉淀或水生成时,反应才能发生(三条
件满足其一即可)。(2)对反应物的要求。
反应物均能溶于水,或一种反应物虽不溶于水却能溶于另一种反应物的溶液中。初中阶段只掌握难溶碳酸盐和碱不能溶于水但都能溶于酸这两种情况。
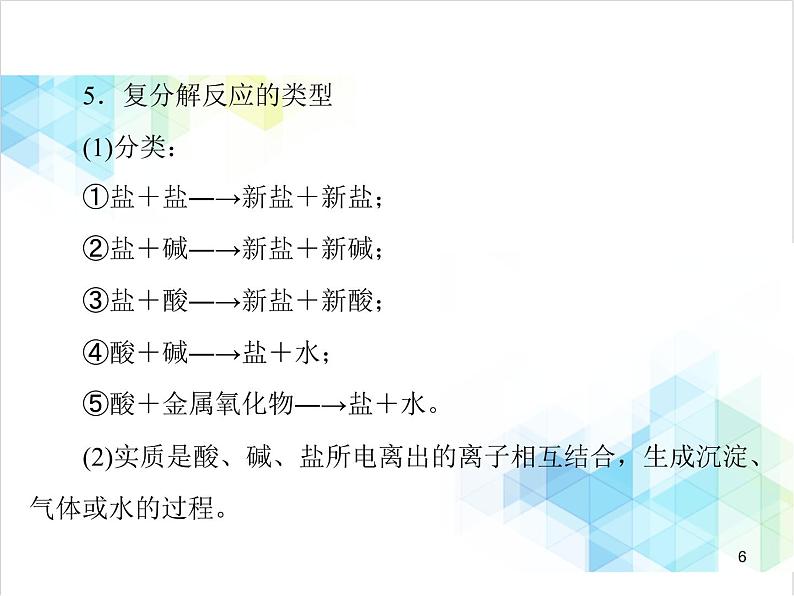
5.复分解反应的类型(1)分类:
①盐+盐―→新盐+新盐;②盐+碱―→新盐+新碱;③盐+酸―→新盐+新酸;④酸+碱―→盐+水;
⑤酸+金属氧化物―→盐+水。
(2)实质是酸、碱、盐所电离出的离子相互结合,生成沉淀、
(1)酸碱盐的溶解性:要熟悉课本 P115 溶解性表。记忆口诀
②碱:KOH、NaOH、Ba(OH)2、Ca(OH)2 四种溶于水。③盐:钾钠铵硝皆可溶;盐酸盐中银不溶;硫酸盐中钡不
解释:钾盐、钠盐、铵盐和硝酸盐都能溶于水,都不是沉淀;氯化物中只有 AgCl 是沉淀;硫酸盐中只有 BaSO4 是沉淀;碳酸盐中除钾、钠、铵之外都是沉淀。(2)气体:常见的是生成 CO2、NH3。
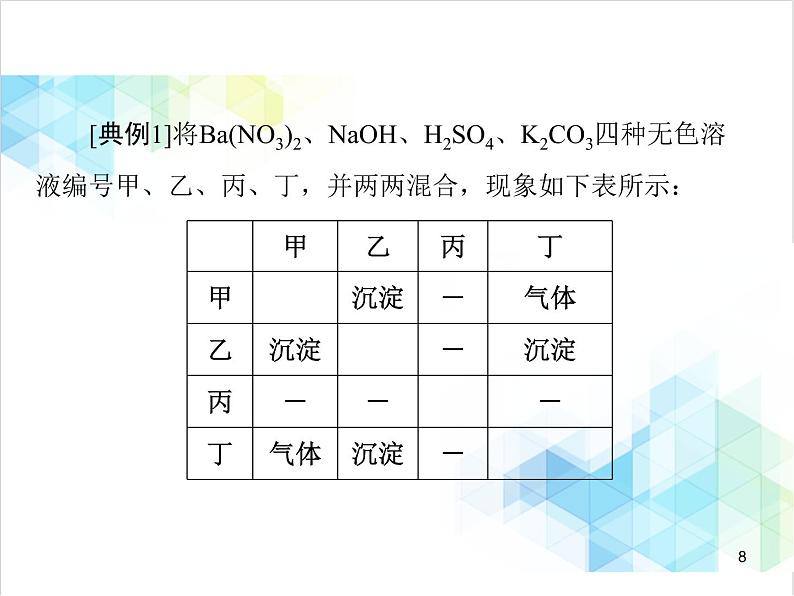
[典例1]将Ba(NO3)2、NaOH、H2SO4、K2CO3四种无色溶液编号甲、乙、丙、丁,并两两混合,现象如下表所示:
下列选项中物质的排序符合表中甲、乙、丙、丁排序的是
)。A.Ba(NO3)2、NaOH、H2SO4、K2CO3B.H2SO4、K2CO3、Ba(NO3)2、NaOHC.NaOH、Ba(NO3)2、H2SO4、K2CO3D.H2SO4、Ba(NO3)2、NaOH、K2CO3
点拨:首先从甲和丁能反应生成气体突破,甲和丁一定有一种为H2SO4另一种为K2CO3,则NaOH、Ba(NO3)2为乙、丙中的一种。由图表信息可知,丙与其他物质混合都没有明显现象,故丙为NaOH,乙为Ba(NO3)2;由于H2SO4和K2CO3 反应产生气体,又和Ba(NO3)2反应产生沉淀,故甲为H2SO4,丁为K2CO3。巧解由选项可知只有D项甲、丁是H2SO4与K2CO3 的组合。
盐的化学性质【知识精讲】
1.盐+盐―→________+________
发生的条件:(1)反应物必须都可溶;(2)生成物至少一种为
__________。
如:Na2SO4+BaCl2===__________↓+2NaCl。2.盐+酸―→________+________
发生的条件:(1)反应物的盐要除去 AgCl、BaSO4;(2)生成物至少一种为________、________或________。如:2HCl+Na2CO3===2NaCl+______+______↑。
3.盐+碱―→________+________
发生的条件:(1)反应物必须_______;(2)生成物至少一种为沉淀、气体或水。
如:CuSO4+2NaOH===________↓+Na2SO4。4.盐+金属―→新盐+新金属
发生条件:(1)盐必须可溶;(2)金属单质除_____________;(3)反应物中金属的活动性比盐中金属的活动性______。
如:2AgNO3+Cu===______+__________。
[典例2]盐能与许多物质发生复分解反应,请分析下列化学反应,回答问题:①BaCl2+H2SO4===2HCl+BaSO4↓;②CuSO4+2NaOH===Na2SO4+Cu(OH)2↓。
(1)从反应物的类别分析:①式是盐与酸的反应;②式是盐
与______的反应。
(2)从复分解反应发生的条件分析:①式和②式都能发生的
原因是生成物中都有______________________。
(3)利用 K2CO3 溶液和____________溶液反应,可制取 KOH。点拨:对盐的化学性质要熟悉,根据发生复分解反应的条件分析;制取一种新碱要考虑K2CO3溶液与可溶性碱反应,并且反应后生成的碳酸盐不溶于水。
沉淀(难溶物或不溶物)
氢氧化钙[Ca(OH)2]
考点1 复分解反应及其发生条件1.豆腐不可与菠菜一起煮,原因是菠菜中含有丰富的草酸、草酸钠,豆腐中含有较多硫酸钙等钙盐,相
互反应会生成草酸钙沉淀等物质。其中发生的反应属于(
A.化合反应C.置换反应
B.分解反应D.复分解反应
点拨:复分解反应是两种化合物相互交换成分。这里是草酸钠与硫酸钙交换成分生成草酸钙和硫酸钠。
2.现有氧化铁、稀硫酸、氢氧化钠溶液、氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发
A.4 个 B.5 个 C.6 个 D.7 个点拨:稀硫酸分别能与氧化铁、氢氧化钠、氯化钡、碳酸钾发生复分解反应,氯化钡也能与碳酸钾发生复分解反应。
考点2 离子的大量共存问题3.下列各组物质分别加入到足量的水中,
能得到无色透明溶液的是(A.FeCl3、NaOH、NaClC.CuSO4、KCl、HCl
B.Na2SO4、HCl、BaCl2D.Na2CO3、NaCl、Na2SO4
点拨:能得到无色透明溶液,一是要求物质间不能生成沉淀;二是物质溶于水不能有颜色。FeCl3和CuSO4溶于水都有颜色,且A项有Fe(OH)3沉淀生成,B项有BaSO4沉淀生成。
初中化学人教版九年级下册课题1 生活中常见的盐图文课件ppt: 这是一份初中化学人教版九年级下册课题1 生活中常见的盐图文课件ppt,文件包含第2课时复分解反应ppt、实验11-3硫酸铜溶液与氢氧化钠氯化钡溶液的反应mp4等2份课件配套教学资源,其中PPT共19页, 欢迎下载使用。
初中课题1 生活中常见的盐优秀课件ppt: 这是一份初中课题1 生活中常见的盐优秀课件ppt,文件包含第2课时复分解反应课件pptx、第2课时复分解反应导学案doc、第2课时复分解反应教案doc、复分解反应wmv等4份课件配套教学资源,其中PPT共28页, 欢迎下载使用。
初中化学人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐习题ppt课件: 这是一份初中化学人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐习题ppt课件,共22页。PPT课件主要包含了化合物,交换成分,另外两种化合物,互相交换成分,有白色沉淀产生,CO32-,Ba2+和NO3-等内容,欢迎下载使用。














