





化学必修 第一册第四章 物质结构 元素周期律第三节 化学键评课课件ppt
展开为什么2个氢原子结合成氢分子,2个氯原子结合成氯分子,而不是3个、4个呢?为什么1个氢原子和1个氯原子结合成氯化氢分子,而不是以其他的个数比相结合呢?
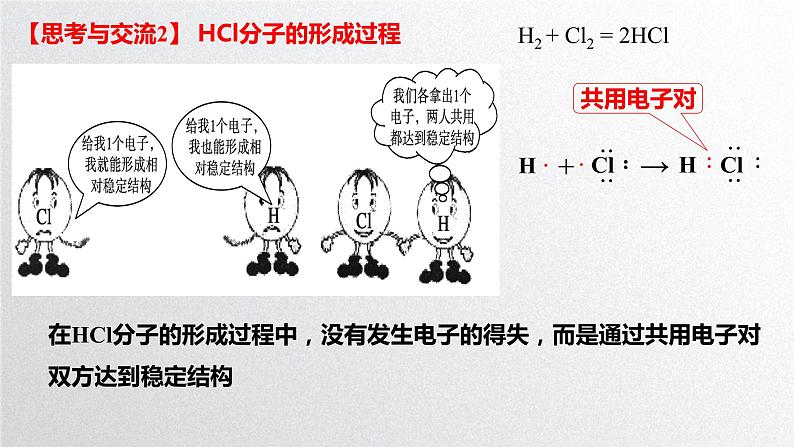
在HCl分子的形成过程中,没有发生电子的得失,而是通过共用电子对双方达到稳定结构
H2 + Cl2 = 2HCl
【思考与交流3】氯原子是如何形成氯气分子的?
氯原子最外层有7个电子,不能通过原子间得失电子达到稳定结构
2个氯原子各提供一个电子,形成共用电子对,2个氯原子就都形成了8电子稳定结构
原子之间通过共用电子对所形成的强烈相互作用,叫共价键
不同原子之间以共用电子对形成分子的化合物。
(2) 多原子非金属单质
(3) 含根的离子化合物 :
含有共价键的化合物不一定是共价化合物
NaOH 、 Na2O2 、 NH4Cl 、NH4NO3
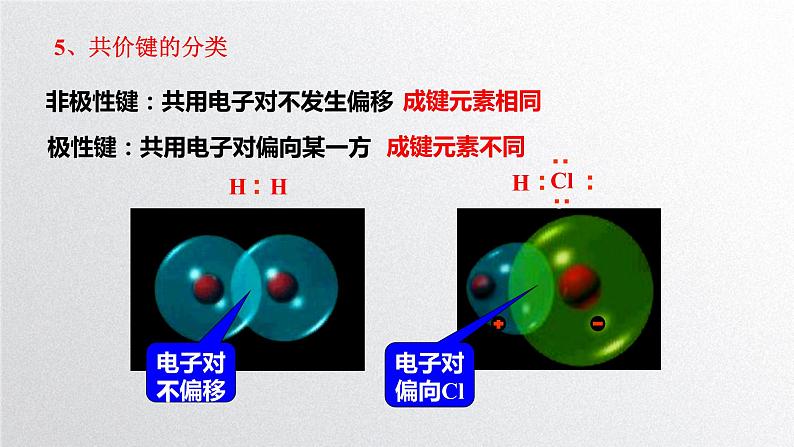
非极性键:共用电子对不发生偏移
极性键:共用电子对偏向某一方
指出下列物质中的共价键类型
O2CH4CO2H2O2Na2O2NaOH
化学反应的过程,本质上就是旧化学键的断裂和新化学键形成的过程。
[讨论] 用化学键的观点分析化学反应过程:
(2)H和Cl 结合生成HCl,形成了H 和Cl之间的化学键H-Cl(新化学键)
1、用化学键的观点来分析 H2 与 Cl2 反应的过程,可以把它想象为2个步骤:
(1)H2 和 Cl2 中的化学键断裂(旧化学键),生成 H 和 Cl
化学反应的过程,本质上就是旧化学键断裂和新化学键形成的过程,所以化学反应中反应物一定有化学键被破坏。
注意:化学反应中反应物的化学键并非全部被破坏
如: (NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl
只破坏反应物中的离子键,共价键未被破坏。
①每个原子一般达到相对稳定结构
②不加中括号[ ],不标正负电荷数
③原子周围共用电子对数=8-原子最外层电子数
6、分子的电子式和结构式(共价键)
(2)结构式
分别用“-、═、≡”表示一对、二对和三对共用电子对
7、用电子式表示原子形成共价键
【共价键形成的分子及其结构模型】
【资料卡片】 分子间作用力和氢键
化学键和化合物关系的“三个一定”和“三个可能”(1)“三个一定”①离子化合物中一定含离子键;②含离子键的一定是离子化合物;③共价化合物中一定不含离子键。(2)“三个可能”①离子化合物中可能含有共价键,如 NaOH;②金属与非金属形成的化合物可能是共价化合物,如 AlCl3;③完全由非金属形成的化合物可能是离子化合物,如 NH4Cl。
离子化合物与共价化合物的比较
离子键或离子键与共价键
1.并不是所有的物质内部都有化学键,稀有气体一定无化学键2.不同种非金属元素形成的化合物,其分子内一定含有极性共价键,但不一定只含极性键,还可能含有非极性共价键、离子键3.含有金属元素的化合物,不一定含有离子键;活泼金属与活泼非金属元素形成的化合物,一定含有离子键4.含有离子键的化合物一定是离子化合物5.含有共价键的化合物不一定是共价化合物6.金属元素与非金属元素形成的化合物不一定是离子化合物
1、下列说法正确的是( )A、单质分子中一定存在共价键;B、气态物质中一定有共价键;C、在共价化合物中一定有共价键;D、全部由非金属元素构成的化合物中,一定不含离子键。
2、下列说法正确的是 ( )A、化学键只存在于分子之间;B、化学键只存在于离子之间;C、化学键是相邻原子(或离子)之间的强烈相互作用;D、化学键是相邻分子之间的相互作用;
3、下列各分子中,所有的原子都满足最外层为8个电子结构的是 A、H2O B、BF3 C、CCl4 D、PCl5 E、NH3 F、CO2
4.下列化合物中只有共价键的是 ( )A.NaCl B.NaOHC.(NH4)2SO4 D.H2SO4
5、下列说法正确的是( ) A、含有金属元素的化合物一定是离子化合物 B、第ⅠA族和第ⅦA族原子化合时,一定生成离子键 C、由非金属元素形成的化合物一定不是离子化合物 D、活泼金属与非金属化合时,能形成离子键
6、下列说法正确的是( ) A.离子键就是使阴、阳离子结合成化合物的静电引力 B.所有金属与所有非金属原子之间都能形成离子键 C.在化合物CaCl2中,两个氯离子之间也存在离子键 D.钠原子与氯原子结合成氯化钠后体系能量降低
AlCl3为共价化合物
7、画出下列物质的电子式,后用线标出化学键种类
A、HCl B、N2 C、NaCl D、NaOH E、Na2O2 F、NH4Cl
Na O O Na
[ ]
8.A、B、C三种短周期元素,其原子序数依次增大,三种元素的原子序数之和为35,A、C同主族,B+原子核外有10个电子。请回答下列问题:(1)A、B、C三种元素分别为____________、__________、______________。(填名称)(2)A、B、C两两之间可形成多种化合物,其中属于离子化合物的化学式分别为________、________、________。(3)用电子式表示B和C形成化合物的过程:________________。
人教版 (2019)必修 第一册第三节 化学键优秀ppt课件: 这是一份人教版 (2019)必修 第一册<a href="/hx/tb_c162000_t3/?tag_id=26" target="_blank">第三节 化学键优秀ppt课件</a>,共32页。PPT课件主要包含了Cl2,不一定,O22-,NH4+,HCl,H2O,②NH3,①CO2等内容,欢迎下载使用。
人教版 (2019)必修 第一册第三节 化学键图片课件ppt: 这是一份人教版 (2019)必修 第一册第三节 化学键图片课件ppt,共46页。
化学必修 第一册第三节 化学键课文内容课件ppt: 这是一份化学必修 第一册第三节 化学键课文内容课件ppt,共23页。PPT课件主要包含了共价键,2成键三要素,1概念,①成键微粒,③成键本质,②成键元素,共用电子对,3分类,极性键,成键原子不显电性等内容,欢迎下载使用。













