





2024河北化学中考备考重难专题:在情景化中解决物质的检验与鉴别、分离与除杂 (课件)
展开一、课件设计初衷 基于老师在总复习过程中对重难题型有较大的需求,难易结合化学学科的重难点,为此设计重难专题复习课件,助力高效课堂二、课件亮点1.对专题知识体系的构建侧重专题知识体系分解再构建,根据本区域近五年的中考真题提炼知识点,通过知识点讲授方法和技巧,并进一步形成对应体系,再让学生尝试应用已有体系中的方法与技巧去解决问题,在复习过程中构建自己的重难专题知识体系。会对难题进行分解,降低梯度,准确、高效攻克重难专题。2.过程性分析设置分步动画对方法讲解、解题步骤设置分步动画,按步骤播放,更清晰有条理。三、课件使用场景适用于中考二轮专题复习
原理:利用物质(或离子)特有的性质(物理性质、化学性质),对两种或两种以上物质进行区分,鉴别时只需出现不同现象即可。
你知道哪些物质可以通过颜色来鉴别吗?
CuSO4 FeCl3 FeCl2 KMnO4
蓝色溶液 黄色溶液 浅绿色溶液 紫红色溶液
黑色固体
CuO、Fe3O4、C、Fe(铁粉)、MnO2 Cu、Fe2O3
有哪些物质可以通过闻气味的方法鉴别?
C2H5OH、H2O、白酒、白醋
根据所学知识,请你总结一下不溶于水、易溶于水的物质有什么。
CaCO3、BaSO4、BaCO3、AgCl不溶于水,Na2CO3易溶于水
这些物质可以通过溶解性的不同进行鉴别
回忆一下:什么物质溶解时吸热,什么物质溶解时放热?
NH4NO3固体溶解时吸热,NaOH固体溶解时放热,这些物质可以通过溶解时的吸放热现象进行鉴别
还有什么物理方法可以鉴别物质?
利用是否有磁性:Fe与Fe3O4都能被磁铁吸引,而FeO不能被吸引
【注意】不能用品尝的方法鉴别药品。
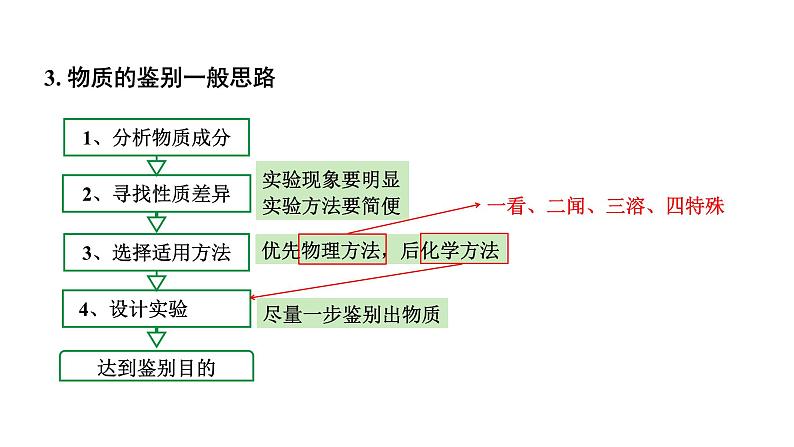
3. 物质的鉴别一般思路
一看、二闻、三溶、四特殊
优先物理方法,后化学方法
实验现象要明显实验方法要简便
请你将下列每组物质和鉴别方法匹配起来。
硬水和软水 相互刻画 黄金和黄铜 加入硝酸银溶液天然纤维和合成纤维 加入等量肥皂水 食盐水和蔗糖水 加入稀盐酸氧化铜和二氧化锰 加入稀盐酸 食盐和小苏打 点燃,闻气味
有明显划痕的是黄金,无划痕或划痕较浅的是黄铜
产生泡沫多、浮渣少的为软水,产生泡沫少、浮渣多的为硬水
丝或毛:有烧焦羽毛气味,燃烧后残留物是黑褐色且能捏碎 ,棉或麻:有烧纸气味有特殊气味,燃烧残留物是黑色或褐色硬块且不易捏碎的为合成纤维
产生白色沉淀的是食盐水,无明显现象的是蔗糖水
有气泡产生的是小苏打,无明显现象的是食盐
固体溶解,溶液变为蓝色的是氧化铜,固体不溶解的是二氧化锰
原理:根据物质的某一特性,一般通过实验的方法加以确定。
1. 气体的检验2. 离子的检验
如何检验氧气和二氧化碳?
氧气特性:助燃性检验方法:将带火星的木条伸入集气瓶中,带火星的木条复燃
将燃着的木条伸入集气瓶中,木条熄灭可以检验二氧化碳吗?不可以,因为不支持燃烧的气体不止CO2,还有N2等
二氧化碳特性:与氢氧化钙溶液反应时有白色沉淀生成检验方法:通入澄清石灰水中,澄清石灰水变浑浊
你还记得初中化学哪些气体的检验方法?你能说出它们分别是利用各自的什么特性检验的吗?
NH3:HCl:水蒸气:
你知道氢离子的检验有几种方法吗?检验氢离子可以转化为证明溶液显酸性,因此利用酸的通性进行检验。
①指示剂法:加入紫色石蕊溶液,溶液变红②加入活泼金属:加入锌粉,有气泡产生③加入碳酸盐:加入Na2CO3溶液,有气泡产生④pH试纸法:用pH试纸,测得溶液的pH<7⑤加入金属氧化物:加入氧化铜,观察到固体溶解,溶液变为蓝色
请你根据碱的性质总结一下检验OH-的方法。
①指示剂法:滴加酚酞溶液,溶液变红②加入可溶性盐:加入氯化铜溶液,有蓝色沉淀生成③pH试纸法:用pH试纸,测得溶液的pH>7
根据碳酸根离子的什么特性可以将其检验呢?
加入过量强碱(氢氧化钠等),加热,用湿润的红色石蕊试纸放在试管口,观察到试纸变蓝 加入硝酸酸化的硝酸银溶液,观察到有白色沉淀产生 加入硝酸酸化的硝酸钡溶液,观察到有白色沉淀产生
你知道下列离子的检验方法吗?
铵根离子:氯离子:硫酸根离子:
适量的Ba(OH)2或Ca(OH)2与Na2CO3反应生成BaCO3或CaCO3沉淀,易于与溶液分离,且没有引入新的杂质,而且还增加了主要成分,可以选择。
除去NaOH溶液中的Na2CO3时,可以选择的下列除杂试剂是?
HCl、H2SO4、CaCl2、BaCl2、适量的Ba(OH)2、适量的Ca(OH)2
与NaOH发生反应,消耗主要成分。
与Na2CO3反应生成NaCl,引入新的杂质
1. 除杂原则根据上页内容你能总结出哪些除杂时需要遵守的原则?(1)主不减:所选试剂不能与被提纯物质(主成分)反应。(2)杂不增:在除去杂质的同时,不引入新的杂质。(3)易分离:除杂后生成的产物的状态要与被提纯物质的状态不同,方便除去。
2. 常见物质的除杂(1)气体的除杂除去O2或者CO中的CO2:先通过氢氧化钠溶液,再通过浓硫酸。
为什么不用氢氧化钙溶液呢?此处浓硫酸的作用是什么?
氢氧化钙是微溶物,吸收CO2的效果不明显,常用于二氧化碳的检验。浓硫酸的作用:通过浓硫酸将水蒸气吸收达到干燥气体(除去水蒸气)的目的。
除了用浓硫酸干燥气体,还有那些物质可用于干燥气体?他们的适用条件是什么?
浓硫酸:可以干燥酸性气体或者中性气体。酸性气体:CO2、SO2、HCl等;中性气体:H2、O2、CO、N2、CH4等。生石灰、碱石灰、NaOH固体:可以干燥碱性气体或者中性气体。碱性气体:NH3等;中性气体:H2、O2、CO、N2、CH4等。
例如:除去Na2CO3中的CaCO3、除去Ca(OH)2中的CaO
碳酸钙不溶于水,碳酸钠溶于水,通过溶解、过滤、蒸发结晶的方法可以达到目的。
氧化钙与水反应生成氢氧化钙,氢氧化钙不与水反应。
例如:除去KNO3固体中的少量NaCl杂质
KNO3的溶解度受温度变化的影响较大,且温度越高,溶解度越大
NaCl溶解度受温度变化的影响较小
可通过降温结晶的方式将其提纯
例如:除去BaSO4中的少量BaCO3
BaSO4 不溶于水、不溶于酸BaCO3 不溶于水、溶于酸
可以根据两个物质的差异性将BaCO3除去,加入盐酸,待不再产生气泡之后,过滤、洗涤、烘干。
(3)液体的除杂除去NaCl溶液中的Na2CO3(阳离子相同,阴离子不同)
选取除杂试剂:适量的BaCl2、CaCl2、HCl
选取除杂试剂的原则:①与杂质离子不共存 (Ba2+、Ca2+、H+)②不引入新的杂质离子(Cl-)
除去NaOH中的Ca(OH)2(阳离子不同,阴离子相同)
在该溶液中的杂质离子是Ca2+
选取除杂试剂:适量的Na2CO3
1. 原理:运用物理方法或化学方法把混合物中的几种物质分开。2. 物理方法
判断:下列哪些混合物可以用过滤法分离?a. NaCl和Na2CO3的混合物 b. AgCl和NaCl的混合物 c. CaCO3和CaCl2的混合物 d. CaCl2和NaNO3的混合物答案:bc
分离碳粉和铁粉有什么好的办法吗?
用磁铁吸引,分离碳粉和铁粉。
3. 化学方法针对使用物理方法不能分离的混合物。
加入适量HCl蒸发结晶
滤渣[Mg(OH)2]
MgCl2和NaCl的混合物
例如:分离MgCl2和NaCl
1.与酸反应2.与氢氧化钡、 氢氧化钙反应3.与可溶性钙盐、 钡盐反应4.溶于水显碱性
操作方法都简单,安全,实验现象也很明显
分别取两种待测样品于试管中,分别加入适量稀盐酸
分别取两种待测样品于试管中并配成溶液,分别滴入无色酚酞溶液
分别取两种待测样品于试管中并配成溶液,分别滴入澄清石灰水或氢氧化钡溶液(或者氯化钡/氯化钙)
1.与酸碱指示剂反应2.与碱反应3.与氢前金属反应4.与金属氧化物反应5.与盐反应
1.与酸碱指示剂反应2.与酸反应3.与非金属氧化物反应4.与盐反应
紫色石蕊试液 酚酞试液
反应无明显现象,不能用于鉴别
任务二:碳酸钙的检验、分离与除杂
胃液的主要成分:HCl
→2HCl+CaCO3===CaCl2+CO2↑+H2O
常见物质主要成分是碳酸钙的有:石灰石、大理石、鸡蛋壳、贝壳、水垢等
取少量待测样品于试管中滴加少量稀盐酸若有气体生成,则其成分为碳酸盐
请你判断一下这个实验方案是否可行?
存在干扰因素稀盐酸+氢前金属→H2↑需要确定气体的成分
参考物质的鉴别一般思路
碳酸钙物理性质:白色块状物 化学性质:与酸反应生成气体
取少量待测样品于试管中滴加少量稀盐酸收集生成的气体将其通入澄清石灰水中若澄清石灰水变浑浊,则证明该样品中的主要成分是碳酸钙
之前所了解的是将杂质的转化成与主要成分状态不同的物质,将主要成分转化成与杂质状态不同的物质是否也可以达到分离与除杂的目的?
查阅资料:石灰石中的碳酸钙在高温条件下煅烧可发生分解,生成两种氧化物。
CaO+H2O=== Ca(OH)2
CO2+Ca(OH)2==CaCO3↓+H2O
取少量反应后溶液,滴加酚酞试液,若为无色,则已全部转化。
1.鉴别、检验、除杂与分离是进行化学研究的重要方法。下列实验方案能达到实验目的的是 ( )
与熟石灰研磨均会产生氨气
变红证明有氧化铜,浑浊说明有碳
2.实验探究题节选:探究1:使用过的暖宝宝中是否还含有铁粉? (1)打开已使用的暖宝宝,将其中的固体用研钵磨成粉状,平铺在表面皿上,用磁铁吸引,部分被吸引。 小明认为被磁铁吸引的黑色粉末是铁粉,小华对小明的结论提出质疑,理由是______________________________________。
四氧化三铁为黑色粉末,也能被磁铁吸引
【查阅资料】①市售暖宝宝中除了含有铁粉,还含有水、蛭石、吸水树脂、氯化钠、活性炭。 蛭石具有保温、调节酸碱平衡、吸附等作用。②铁粉在一定条件下可转化为四氧化三铁,四氧化三铁具有磁性。
(2)为进一步验证被磁铁吸引的黑色粉末为铁粉,小明取少量被磁铁吸引的黑色粉末于试管中, 加入适量硫酸铜溶液,观察到___________________________________________________________,反应的化学方程式为________________________,得出黑色粉末为铁粉。
溶液由蓝色变为浅绿色,试管底部黑色固体消失,析出红色固体
Fe+CuSO4===FeSO4 +Cu
化学性质:1.与酸反应 2.与氧气反应 3.与盐溶液反应
与酸反应产生氢气→有气泡生成
3.实验探究题节选:天宫课堂上航天员将半片维 C 泡腾片塞入一个蓝色水球里,水球中立即产生很多气泡,在失重的情况下,气泡不离开水球。 小红对此产生浓厚的兴趣,将维 C 泡腾片带到学校和小组同学在老师的指导下进行探究。 【查阅资料】①某品牌维C泡腾片的主要成分是:维生素C(C6H8O6)、碳酸氢钠(NaHCO3)、柠檬酸(C6H8O7);②柠檬酸属于有机酸,具有酸的通性,在水溶液中可以解离出 H+ 。 【实验1】小华将注射器中的水注入盛有维 C 泡腾片的锥形瓶内,将导管通入盛有澄清石灰水的集气瓶中,观察到_________________,证明该气体中有CO2。
中考化学复习重难突破13物质的分离与除杂课件: 这是一份中考化学复习重难突破13物质的分离与除杂课件,共24页。PPT课件主要包含了过滤法,蒸馏法,磁铁吸引法,降温结晶法,浓硫酸,NaOH,饱和NaHCO3溶液,稀盐酸或稀硫酸,高温煅烧,MnO2等内容,欢迎下载使用。
中考化学复习重难突破13物质的分离与除杂练习课件: 这是一份中考化学复习重难突破13物质的分离与除杂练习课件,共28页。PPT课件主要包含了K2CO3溶液,⑤③①④②③,用玻璃棒引流等内容,欢迎下载使用。
中考化学复习重难突破8物质的分离与除杂练习课件: 这是一份中考化学复习重难突破8物质的分离与除杂练习课件,共26页。












