

人教版 (新课标)第一节 醇 酚背景图ppt课件
展开羟基(—OH)与烃基或苯环侧链上的碳原子相连的化合物称为醇。羟基(—OH)与苯环直接相连的化合物称为酚。
练习:判断下列物质中哪些属于醇类,哪些为酚?
二、醇的分类和命名
① 选主链:选最长碳链,且含—OH② 编号位:从离—OH最近的一端起编③ 写名称:取代基位置— 取代基名称 — 羟基位置— 母体名称(羟基位置用阿拉伯数字表示;羟基个数用“二”、“三”等表示。)如:
(简称丙三醇,俗称甘油)
2,3—二甲基—3—戊醇
表3-1相对分子质量相近的醇与烷烃的沸点比较
结论:相对分子质量相近的醇比烷烃的沸点高得多。因为醇分子间可以形成氢键。且C数越多沸点越高
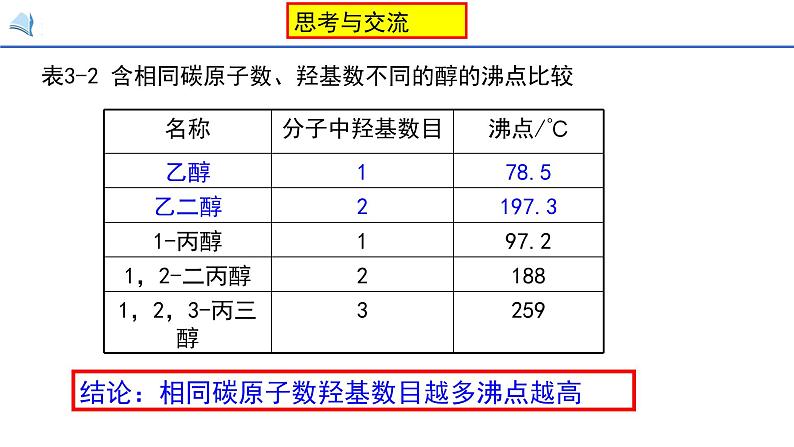
表3-2 含相同碳原子数、羟基数不同的醇的沸点比较
结论:相同碳原子数羟基数目越多沸点越高
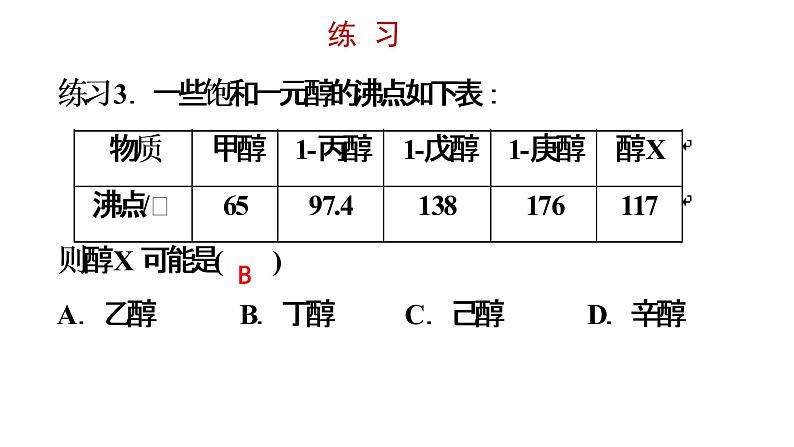
(1) 沸点规律:相对分子质量越大,醇的沸点越高。同碳原子数的醇,羟基数越多,沸点越高。相对分子质量相近的醇和烷烃:醇的沸点大于烷烃(2)溶解性: 甲醇、乙醇、丙醇、乙二醇、丙三醇等低级醇可与水以任意比例互溶。高级醇一般不溶于水。
俗称:酒精.是一种无色透明,有特殊香味的易挥发的液体,密度比水小,且可以与水以任意比互溶。
检验C2H5OH中含水的方法:用无水硫酸铜
(1)取代反应① 乙醇与活泼金属(如Na、K、Ca、Mg)的反应
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
定量关系:1ml—OH参与反应生成0.5 mlH2,此反应可检验—OH的存在,也可计算分子中—OH数目
甲醇、乙二醇、丙三醇中分别加入足量的金属钠,产生等体积的氢气(相同条件下),则上述三种醇的物质的量之比是( ) A.2∶3∶6 B.3∶2∶1 C.4∶3∶1 D.6∶3∶2
结论:2-OH——H2可用于快速确定醇中羟基数目
1.浮在水面2.熔成小球3.四处游动4.发出嘶嘶的响声
1.钠沉在乙醇底部2.不熔成小球3.无明显响声
浓硫酸作用:吸水剂和催化剂
酯化反应原理:酸脱羟基,醇脱氢
④ 和浓HBr溶液反应
反应条件:浓氢卤酸,共热
(现象:淡蓝色火焰,放出大量热)
② 被强氧化剂 KMnO4或K2Cr2O7 氧化:
乙醇可使酸性 KMnO4 溶液的紫色褪去乙醇使酸性 K2Cr2O7 溶液由橙黄色变绿色
反应原理:CH3CH2OH→CH3CHO → CH3COOH
③处的C-H键、①处的O-H键
拓展: 醇的催化氧化规律:
结论:若与羟基相连的碳上有2个氢原子,则醇被氧化成醛; 若与羟基相连的碳上有1个氢原子,则醇被氧化成酮; 若与羟基相连的碳上没有氢原子,则醇不能被氧化。
下列各醇,能发生催化氧化的是( )
(3)乙醇的消去反应(分子内脱水)
① 醇发生消去反应的条件:与羟基-OH所连碳的相邻碳上必须有氢原子.浓硫酸、加热到170℃
原理:脱去—OH和连接—OH碳原子的邻位碳原子上的1个H
小结:溴乙烷和乙醇消去反应的比较
a.实验中浓硫酸和酒精的体积比是3 :1,顺序是先加酒精再加浓硫酸,浓硫酸作催化剂和脱水剂。
b.加入碎瓷片作用,防暴沸
c.温度计的水银球插在液面下,并不接触瓶底。
d.加热温度要迅速升到170℃左右。
e.NaOH溶液的作用:吸收SO2、CO2等
f.反应液随温度升高,混合液颜色会逐渐变黑,是因为浓硫酸使乙醇脱水碳化生成碳。
g.收集乙烯用排水法,不能用向下排空气法。
高中化学人教版 (新课标)选修5 有机化学基础第一节 醇 酚课文配套课件ppt: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第一节 醇 酚课文配套课件ppt,共40页。PPT课件主要包含了来苏水,甲基苯酚,C6H5OH,结构简式,苯酚的结构,球棍模型,比例模型,苯酚的物理性质,纯净的苯酚是无色晶体,有特殊的气味等内容,欢迎下载使用。
高中人教版 (新课标)第一节 醇 酚集体备课课件ppt: 这是一份高中人教版 (新课标)第一节 醇 酚集体备课课件ppt,共26页。PPT课件主要包含了C6H6O,结构简式,C6H5OH,官能团-OH,苯酚球棍模型,苯酚比例模型,熔点43℃,②溶解性,用酒精洗,我国第一块特效除菌皂等内容,欢迎下载使用。
高中化学第一节 醇 酚课前预习课件ppt: 这是一份高中化学第一节 醇 酚课前预习课件ppt,共40页。PPT课件主要包含了学习目标,何以解忧,唯有杜康等内容,欢迎下载使用。