






高中化学人教版 (新课标)选修5 有机化学基础第一节 醇 酚多媒体教学ppt课件
展开1.了解苯酚的主要物理性质。2.掌握苯酚的主要化学性质;体会苯酚结构中羟基与苯环的相互影响。3.了解苯酚的用途。
1.苯酚的分子式是________,结构简式是________、________或________或________。2.羟基与苯环________而形成的化合物称为酚。3.苯酚的物理性质(1)纯净的苯酚是________色晶体,但放置时间较长的苯酚往往呈________色。(2)苯酚具有________的气味,熔点为43℃。(3)苯酚易溶于乙醇等________溶剂,室温下,在水中的溶解度是9.3g,当温度高于65℃时,能与水混溶。
4.苯酚的化学性质(1)弱酸性:跟NaOH反应,生成________和水,但酸性比H2CO3________。(2)取代反应:跟________溴水反应,生成三溴苯酚________色沉淀。(3)显色反应:跟铁盐(FeCl3)反应,生成________色物质。可以检验________的存在。
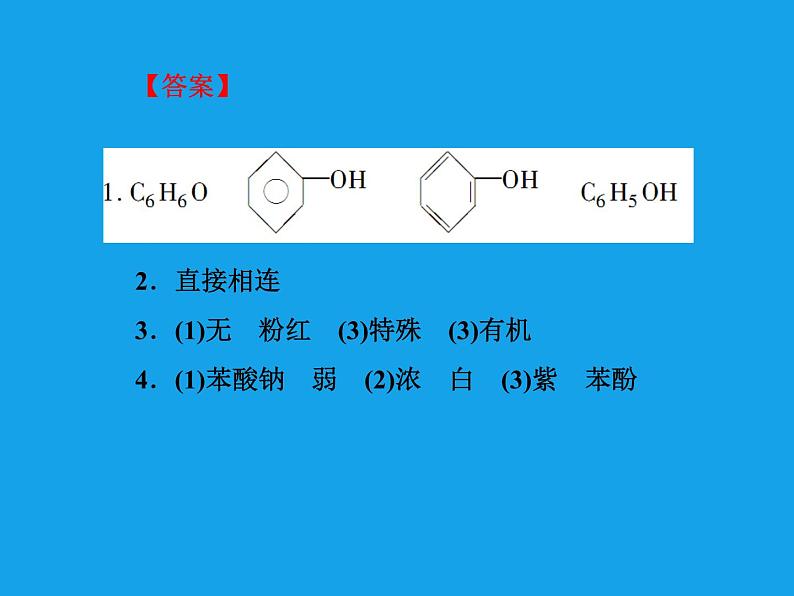
【答案】 2.直接相连3.(1)无 粉红 (3)特殊 (3)有机4.(1)苯酸钠 弱 (2)浓 白 (3)紫 苯酚
1.苯酚俗称石炭酸,具有弱酸性,那么它能不能与酸碱指示剂反应?提示:由于苯酚的酸性太弱,苯酚水溶液不能使石蕊、甲基橙等酸碱指示剂变色。
2.苯酚能和纯碱溶液发生反应吗?说明原因。
3.你如何从分子内基团间相互作用来解释下列事实。①苯和苯酚发生溴代反应的条件和产物有很大的不同。②实验表明,苯酚的酸性比乙醇强。
1.苯酚的结构苯酚的分子式是C6H6O,它的结构式为:
由苯酚分子的比例模型可知(如右图所示),苯酚分子里有12个原子位于同一平面内,即苯环上的6个碳原子及与它直接相连的5个氢原子和一个氧原子,但与氧原子相连的氢原子与它们不在同一平面上。苯酚是最简单的酚。
2.物理性质①纯净的苯酚是无色、有特殊气味的晶体,若接触空气会因小部分被氧化而呈粉红色。②常温下在水中溶解度不大,当温度高于65℃时,能与水混溶;易溶于有机溶剂,如乙醇、乙醚等。③苯酚有毒,它的浓溶液对皮肤有强烈的腐蚀性,若不慎沾到皮肤上,应立即用酒精洗涤。
【例1】 苯酚有毒且有腐蚀性,使用时若不慎溅到皮肤上,可以用来洗涤的试剂是( )A.NaOH溶液 B.酒精C.65℃以上的热水 D.冷水【解析】 不能用NaOH溶液来洗涤沾在皮肤上的苯酚,因为NaOH溶液也具有腐蚀性;也不能用65℃以上的热水,冷水效果不好;苯酚易溶于酒精,所以可用酒精洗涤,故选B。【答案】 B
下列化合物中属于醇类的是________;属于酚类的是________。
【解析】 B中无羟基,首先排除,它既不属于醇,也不属于酚类。A、C、E中的羟基与苯环直接相连属于酚类。F中无苯环,D中的羟基与苯环支链上的碳原子相连,所以D、F属于醇类。【答案】 属于醇类的是:D、F;属于酚类的是:A、C、E。
关于苯酚的说法中,错误的是( )A.纯净苯酚是粉红色晶体B.有特殊气味C.易溶于乙醇、乙醚等有机溶剂,不易溶于冷水D.苯酚有毒,但药皂中掺有少量苯酚【答案】 A
1.苯酚的弱酸性在水溶液中,苯酚易与氢氧化钠反应,苯酚有酸性。(1)苯酚与氢氧化钠溶液反应生成苯酚钠和水,化学方程式如下:
注意:苯酚、H2CO3、HCO3-的酸性强弱顺序为:
2.苯酚的取代反应苯酚可与卤素单质、硝酸、硫酸等发生取代反应。苯酚能与浓溴水反应生成不溶于水的白色沉淀(2,4,6-三溴苯酚),此反应很灵敏,常用于苯酚的定性检验和定量测定。
3.苯酚的显色反应向苯酚溶液中滴入几滴三氯化铁溶液,溶液显紫色,利用此反应可检验苯酚的存在。4.苯酚的用途苯酚是重要的化工原料,广泛用于制造酚醛树脂、染料、医药、农药等,也可用作食品防腐剂和消毒剂。
【解析】 苯酚具有酸性,比碳酸的酸性弱,比HCO3-的酸性强。在水溶液中,酸性较强的物质与碱性较强的物质反应生成酸性和碱性相对较弱的物质,这是反应的一般规律。而进一步分析已知条件还可以得出HCO3-、 的碱性依次增强这一隐含的信息,由此应用较强的碱性物质可制取较弱的碱性物质,即可得出结论。【答案】 BC
下列离子方程式书写正确的是( )A.碳酸氢钠与盐酸反应CO32-+2H+===CO2↑+H2OB.硫化亚铁与盐酸反应 S2-+2H+===H2S↑C.苯酚钠溶于醋酸溶液C6H5O-+CH3COOH―→C6H5OH+CH3COO-D.氯化亚铁溶液中通入少量氯气Fe2++Cl2===Fe3++2Cl-
【解析】 离子方程式的书写和正误判断能很好的考查学生的相关知识,也是一种“区分度”很好的题型。A项中NaHCO3在离子方程式中应写为HCO3-;B项中FeS应写化学式;D项中电子得失不守恒;C项正确。【答案】 C
在下列反应中,既不能说明苯酚分子中羟基受苯环影响而使它比乙醇中羟基活泼,也不能说明由于羟基对苯环的影响,使苯酚中苯环比苯更活泼的是( )
【解析】 羟基和苯环连在一起相互影响,一方面苯环使羟基上的H原子活化,比乙醇中羟基上的H原子易电离;另一方面羟基使苯环邻、对位上的氢原子活化,比苯中的H原子易于取代。依题意要判断酚羟基比醇羟基活泼,即酚羟基发生的反应醇羟基不能,B项符合;苯酚苯环上的氢原子比苯上的氢原子活泼,即苯酚比苯易于取代,C、D两项符合,而A项反应醇也能发生,无法判断活泼性。【答案】 A
【例3】 某有机物结构如图所示,关于该有机物下列说法正确的是( )A.它是苯酚的同系物B.1ml该物质能与溴水反应消耗2ml Br2发生取代反应C.1ml该有机物能与足量金属钠反应产生0.5ml H2D.1ml该有机物能与2ml NaOH反应E.该物质在加热条件下可以与铜反应生成一种具有醛基的化合物
【解析】 (1)首先分析该有机物的结构,可以发现在该分子中既有醇羟基又有酚羟基,因而能表现醇的性质,又能表现酚类的性质;(2)根据同系物的定义可以看出它不属于苯酚的同系物;(3)与钠反应时两类羟基都能参加反应,但是只有酚羟基可以与NaOH溶液反应,醇羟基不可与NaOH溶液反应;(4)与Br2发生取代反应时,按照规律,只与酚羟基的邻、对位有关,而对位已被甲基占有,只能在两个邻位反应;(5)与醇羟基相连碳原子上有2个氢原子,所以可以发生催化氧化反应生成含醛基的化合物。因此B、E为本题正确选项。【答案】 BE
(2010·西安高二检测)关于酚羟基和醇羟基的分析中,错误的是( )A.原子组成一样B.O—H键的化学键类型一样C.羟基中氢原子活泼性不同D.酚羟基能发生电离,醇羟基也能发生电离【答案】 D
高中化学人教版 (新课标)选修5 有机化学基础第一节 醇 酚备课ppt课件: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第一节 醇 酚备课ppt课件,共26页。PPT课件主要包含了第一节醇酚,结构简式,C6H6O,一苯酚的结构,苯酚软膏使用说明书,不能与碱性药物并用,溶液浑浊,得到澄清溶液,二苯酚的物理性质,③有毒有腐蚀作用等内容,欢迎下载使用。
化学选修5 有机化学基础第五章 进入合成高分子化合物的时代综合与测试复习课件ppt: 这是一份化学选修5 有机化学基础第五章 进入合成高分子化合物的时代综合与测试复习课件ppt,共32页。PPT课件主要包含了答案A等内容,欢迎下载使用。
高中化学人教版 (新课标)选修5 有机化学基础第一节 油脂背景图课件ppt: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第一节 油脂背景图课件ppt,共54页。PPT课件主要包含了答案C等内容,欢迎下载使用。













