




2021年中考化学一轮复习《溶液》课件(共24张PPT)
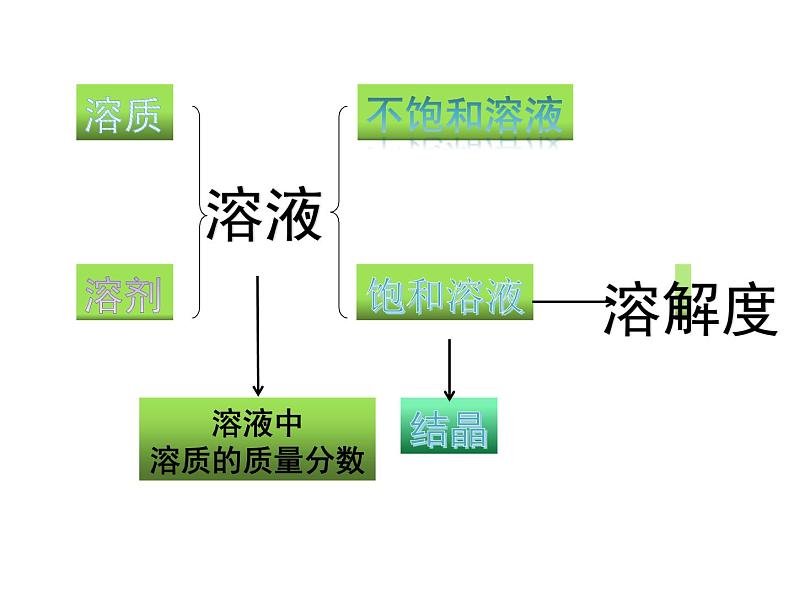
展开均一、稳定 的混合物
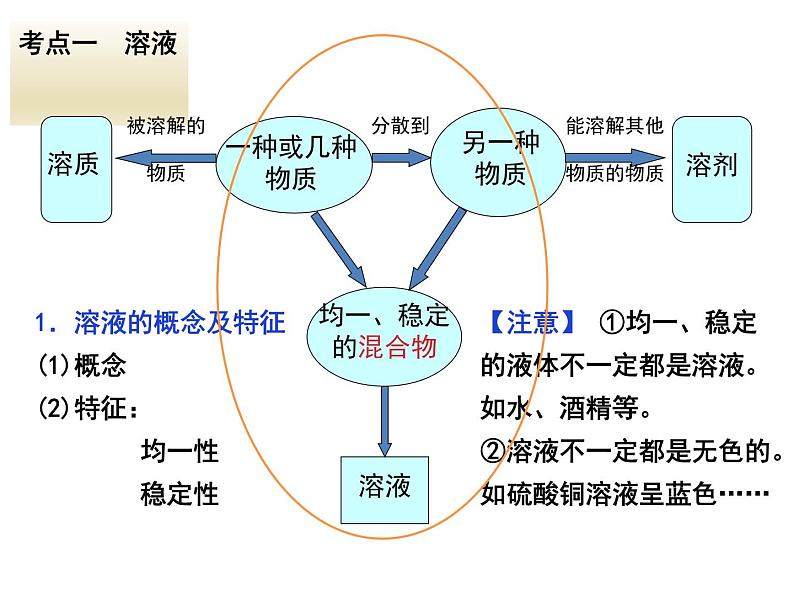
能溶解其他 物质的物质
1.溶液的概念及特征(1)概念(2)特征: 均一性 稳定性
【注意】 ①均一、稳定的液体不一定都是溶液。如水、酒精等。②溶液不一定都是无色的。如硫酸铜溶液呈蓝色……
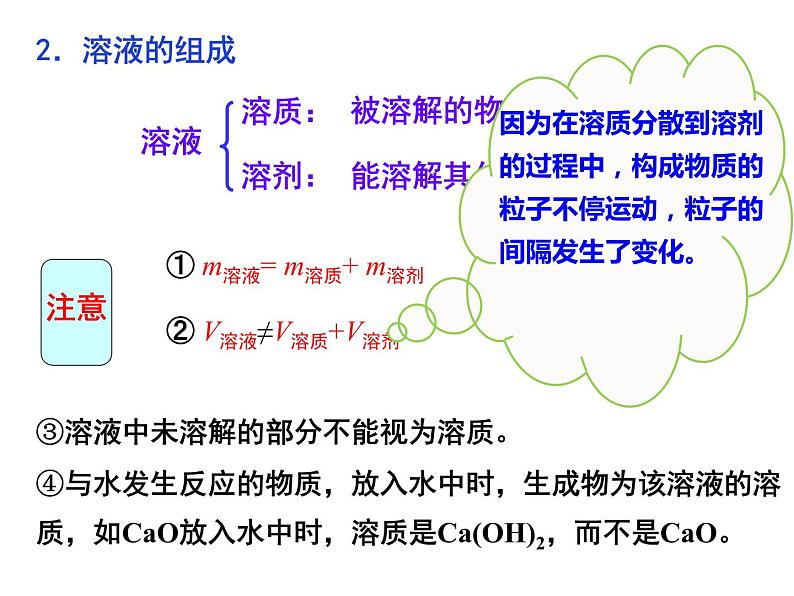
③溶液中未溶解的部分不能视为溶质。④与水发生反应的物质,放入水中时,生成物为该溶液的溶质,如CaO放入水中时,溶质是Ca(OH)2,而不是CaO。
① m溶液= m溶质+ m溶剂
② V溶液≠V溶质+V溶剂
因为在溶质分散到溶剂的过程中,构成物质的粒子不停运动,粒子的间隔发生了变化。
物质在溶解时常伴随有吸热、放热现象。如________溶解时会吸热,表现为溶液的温度降低;________溶解时会放热,表现为溶液的温度升高;_________溶于水时溶液的温度基本不变。
3.溶解时的吸热、放热现象
多数物质溶解于水只发生物理变化,但氧化钙遇水放出大量的热并非溶解放热,而是氧化钙与水反应放出的热。
当在植物油中加入洗涤剂后振荡,植物油就被分散成无数细小的油滴,而不能聚集成大的油珠,这种现象被称为_________。肥皂、洗涤剂等都具有乳化作用。
【注意】乳化与溶解的不同点在于,分散的物质在水中存在的状态不同。植物油被乳化后变成无数细小的油滴分散在水中,较稳定,但不是非常均匀;而溶质溶解在水中,是以分子或离子的形式存在的,具有均一、稳定的特征。
【例1】下列反应完毕后,不能得到溶液的是( )A.二氧化碳通入足量澄清石灰水 B.碳酸钙与足量的盐酸反应C.锌粒与足量的稀硫酸反应 D.碳酸钠与适量的盐酸反应
【练习1】加热氯酸钾和二氧化锰的混合物制取氧气至不再产生气体为止,将残留物溶于水,其溶质是 。
【练习2】向盛有Fe、Cu的烧杯中加入过量的稀硫酸,所得溶液中的溶质有( )A.1种 B.4种 C.2种 D.3种
考点二 饱和溶液与不饱和溶液
在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液
在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液
饱和与不饱和溶液如何转化呢?
一般规律:不饱和溶液 饱和溶液
降温、蒸发溶剂、加溶质
升温、蒸发溶剂、加溶质
特殊溶质:Ca(OH)2不饱和溶液 饱和溶液
①某物质的饱和溶液是指相应的溶质不能继续溶解的溶液,但还可以溶解其他物质。如饱和氯化钠溶液还可以继续溶解硝酸钾固体。
②通过降低温度实现由不饱和溶液向饱和溶液的转化,只是针对多数固体溶质而言,对气体和少数固体(如熟石灰)等不适用。
③对某饱和溶液进行降温或蒸发溶剂时,往往会有溶质从溶液中以晶体形式析出。
三.溶解度(S)及曲线固体 (1)概念的理解:
抓四点: ①条件:在一定温度下 ②标准:100克溶剂 ③状态:饱和状态 ④单位:克
2.气体的溶解度(1)概念:是指在一定温度下,压强为________ 时,某气体溶解在_____体积的水里达到________状态时的气体________。(2)影响因素:①内因:气体的性质。②外因:主要是温度和压强。温度越高,气体的溶解度_______;压强越大,气体的溶解度______。
(4)、固体溶解度曲线及意义
点:曲线上的点均表示某物质在该温度下的溶解度。
交点:曲线的交点表示这两种物质在该温度下的溶解度相同。
曲线:曲线越陡,该物质的溶解度受温度影响越大。
讨论:固体物质溶解度受温度变化影响情况?
大多数固体物质溶解度随温度升高而增大, 例如 硝酸钠、氯化铵等。
少数固体物质溶解度受温度影响不大, 例如食盐。
极少数固体物质溶解度随温度升高反而减小,例如熟石灰。
(4)溶解度曲线常见的考查形式(如图)
①t3℃时,a的溶解度为________g。②P点的含义是_________________________。
t2℃时,a和c的溶解度相等
③N点对应的溶液为t3℃时a的__________溶液,可通过____________________________________等方法使a的不饱和溶液变成饱和溶液。④t1℃时,a、b、c三种物质的溶解度由大到小的顺序为______________。
加入a物质(或降温,或恒温蒸发溶剂)
⑤从a溶液中获取a晶体可采用_______________________或__________________的方法。⑥从b溶液中获取b晶体可采用__________________的方法。
⑦t2℃时,a、b、c三种物质的饱和溶液各w g,降温至t1℃会析出晶体的是__________,此时所得溶液中溶质的质量分数由小到大的顺序是_________。⑧分离a与少量b 的混合物,可采用____________或____________________的方法。
甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里, 则下列说 法正确的是( ) A.甲溶液中溶质的质量分数增大 B.乙溶液中剩余的固体减少 C.试管里甲、乙物质的溶解度都增大 D.试管里甲、乙两溶液中的溶质都减少
再放进盛有冰水的烧杯里, 则下列说
考点四 溶质的质量分数
1.定义:溶质质量与溶液质量之比
①质量单位要统一②既适用于饱和溶液的计算,也适用于不饱和溶液的计算。③溶质的质量分数一般用百分数来表示,不能用分数表示。④未溶解的物质不能计入溶质质量。
2.一定温度下,某物质饱和溶液的溶质质量分数
点拨:一定温度下,某饱和溶液的溶质质量分数为定值。
3.关于溶液稀释问题的计算
溶液稀释前后,溶质的质量不变
点拨:溶质质量 = 溶液质量 × 溶质的质量分数
【例1】(2018新疆中考)某化学兴趣小组取12.5g的 大理石样品(杂质不与盐酸反应)加入到一定量的稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示。请计算:(1)生成CO2的质量是_____g;(2)该盐酸的溶质质量分数是多少?(列式计算,计算结果保留到0.1%)
(2)解:设该盐酸中溶质的质量为x。
73 44 x 4.4g
盐酸的溶质质量分数 =
答:该盐酸的溶质质量分数是7.3%。
CaCO3+2HCl==CaCl2+H2O+CO2↑
想一想:有没有别的解题方法?
考点五 一定溶质质量分数溶液的配制
配制50 g溶质质量分数为5%的氯化钠溶液
仪器:托盘天平(砝码盒)、量筒(10mL、50mL、100mL)、___________、烧杯、________、________、擦拭纸、称量纸。步骤:①计算:需氯化钠的质量为_____,需水的体积为_______②称量:分别在托盘天平左右两盘放上相同的称量纸,调节托盘天平平衡后,先将游码移动至______,然后逐渐往_____盘加氯化钠固体至天平平衡。
③量取:用________的量筒量取________的水。④溶解:用玻璃棒搅拌的目的是________________,溶解时________(填“能”或“不能”)在量筒中进行。⑤装瓶贴标签。
溶液-中考化学一轮复习课件PPT: 这是一份溶液-中考化学一轮复习课件PPT,共24页。PPT课件主要包含了思维导图,溶液的形成,被溶解,能溶解,溶解时吸放热,NH4NO3,NaCl,NaOH或浓硫酸,除污方法,乳化作用等内容,欢迎下载使用。
溶液-中考化学一轮复习课件PPT: 这是一份溶液-中考化学一轮复习课件PPT,共30页。PPT课件主要包含了知识网络·思维导图,溶液的形成,知识清单·主干回顾,溶液的组成及特征,乳化现象,生活中常见的去污原理,NH4NO3,浓硫酸,蔗糖等,溶解时的能量变化等内容,欢迎下载使用。
溶液及溶解度-中考化学一轮复习课件PPT: 这是一份溶液及溶解度-中考化学一轮复习课件PPT,共34页。PPT课件主要包含了快速抢答,硫酸铜溶液,葡萄糖注射液,稀盐酸,医用生理盐水,常见的溶液,溶解度,依然是不饱和溶液,质温饱,一定温度等内容,欢迎下载使用。












