





- 第八单元《金属和金属材料》复习课件 课件 6 次下载
- 第九单元《溶液》复习课件 课件 6 次下载
- 人教版化学九年级下册第十一单元《盐、化肥》复习课件 课件 7 次下载
- 人教版化学九年级下册第十二单元《化学与生活》复习课件 课件 5 次下载
初中化学人教版九年级下册第十单元 酸和碱综合与测试获奖复习ppt课件
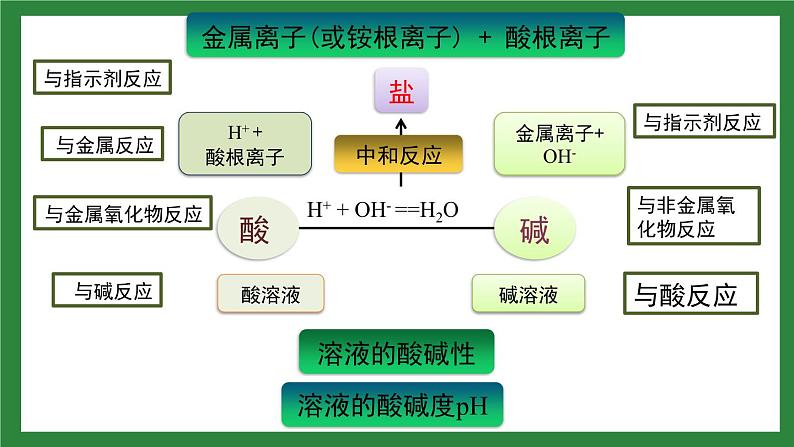
展开H+ + OH- ==H2O
金属离子(或铵根离子) + 酸根离子
口诀:紫石蕊,遇酸红,遇碱蓝;无酚酞,遇酸无,遇碱红
指示剂遇到酸性溶液或碱性溶液时,变色的是指示剂,而不是酸性溶液或碱性溶液。
考点二 常见酸的性质
(1)浓盐酸具有_______,在空气中能形成______,有腐蚀性。(2)浓硫酸易溶于水,具有______性、_____性(脱水性)。
1.浓盐酸、浓硫酸的性质
①稀释浓硫酸:酸入水、沿器壁、缓缓倒、不断搅。
②由于浓硫酸具有吸水性,故在实验室常用作干燥剂。
④如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量的水冲洗,然后再涂上3%~5%的碳酸氢钠溶液。
③敞口放置,浓盐酸因挥发性而使其质量减少;浓硫酸因吸水性而使其质量增加,所以它们都要密封保存。
【练习1】(湖南郴州中考)分别将一小瓶浓盐酸、浓硫酸露置在空气中一段时间后,发生的共同变化是( )A.溶液的质量减小B.溶液的浓度减小C.溶质的质量减小D.溶剂的质量增大
2.稀盐酸、稀硫酸的化学性质
由于盐酸、稀硫酸在水溶液中都能解离出______,所以具有相似的化学性质。
(1)酸能与指示剂反应
酸能使紫色石蕊溶液变__色,使无色酚酞溶液____。
(2)酸能与多种活泼金属反应,生成盐和氢气(氢前可换氢)
Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
Mg+H2SO4=MgSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
Fe+2HCl=FeCl2+H2↑
Fe+H2SO4=FeSO4+H2↑
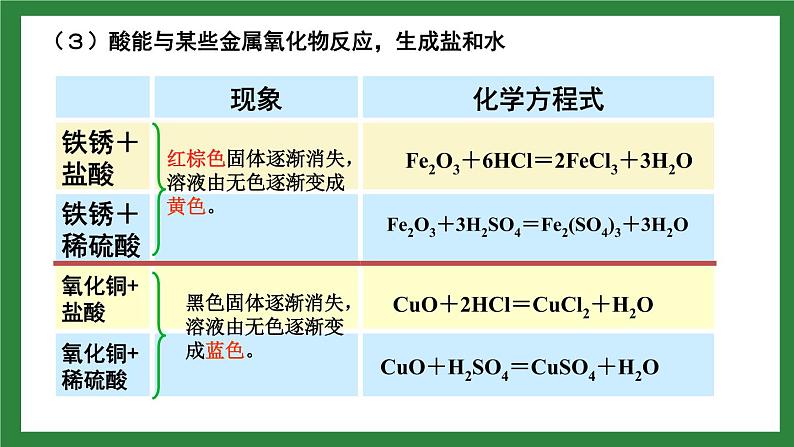
(3)酸能与某些金属氧化物反应,生成盐和水
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
CuO+2HCl=CuCl2+H2O
CuO+H2SO4=CuSO4+H2O
(4)酸和碱发生中和反应,生成盐和水
NaOH + HCl = NaCl + H2O
Ca(OH)2+ 2HCl = CaCl2 + 2H2O
2NaOH+H2SO4 = Na2SO4 + 2H2O
稀盐酸、稀硫酸的化学性质1 跟指示剂的反应2 跟金属的反应3 跟金属氧化物的反应4 跟碱的反应
酸能使石蕊溶液变红色,使酚酞溶液不变色。金属+酸==盐+氢气↑Zn+H2SO4=ZnSO4+H2↑Fe2O3+6HCl= 2FeCl3+3H2O金属氧化物+酸==盐+水NaOH+HCl= NaCl+H2O 碱+酸==盐+水
【练习2】(海南中考)向氧化铜和铁粉的混合物中加入一定量稀硫酸,充分反应后过滤,向滤渣 中再滴入稀硫酸,有气泡产生,则下列判断正确的是( )A.滤渣中可能含Cu B.滤渣中只含FeC.滤液中不含CuSO4 D.滤液中不一定含FeSO4
考点三 常见碱的性质
氢氧化钠:白色固体,______溶于水并放出大量的热;易吸收水分而____,有强烈的腐蚀性。俗称火碱、烧碱、苛性钠。氢氧化钙:白色粉末状固体,______溶于水,有腐蚀性。
①氢氧化钠固体不仅吸水潮解,而且还能与空气中的二氧化碳反应,使氢氧化钠转变为碳酸钠而变质,所以氢氧化钠必须密封保存。氢氧化钙也要密封保存。
1.氢氧化钠、氢氧化钙的物理性质
②氢氧化钙可用生石灰与水反应制得,此反应能放出大量的热,反应的化学方程式是CaO+H2O===__________。
③如果不慎将碱液沾到皮肤上,要用大量水冲洗,再涂上硼酸溶液。
④氧化钙、氢氧化钙、碳酸钙的俗称及相互转化:
碳酸钙(CaCO3)是大理石或石灰石等主要成分。
氧化钙(CaO)俗称:生石灰。氢氧化钙[Ca(OH)2]俗称:熟石灰、消石灰。
2.氢氧化钠、氢氧化钙的化学性质
由于氢氧化钠、氢氧化钙在水溶液中都能解离出______,所以具有相似的化学性质。
(1)碱溶液能与指示剂反应
碱溶液能使紫色石蕊溶液变___,使无色酚酞溶液变___。
(2)碱溶液能与某些非金属氧化物反应,生成盐和水。
2NaOH + CO2 = Na2CO3 + H2O
2NaOH + SO3 = Na2SO4 + H2O
(3)碱和酸发生中和反应,生成盐和水。
氢氧化钠、氢氧化钙的化学性质跟指示剂的反应碱溶液能使石蕊溶液变蓝色,使酚酞溶液变红色。跟非金属氧化物的反应碱溶液+非金属氧化物==盐+水2NaOH+CO2 =Na2CO3 + H2O跟酸的反应碱+酸==盐+水NaOH+HCl= NaCl+H2O
【练习3】(重庆中考)氢氧化钠溶液和氨水都能使酚酞溶液变红,其原因是二者的溶液中均含有 一种相同的粒子是( )A.H+ B.OH- C.H2O D.H
【练习4】(湖北恩施州中考)下列关于氢氧化钠的描述中错误的是( )A.可用于改良酸性土壤B.易溶于水,溶解时放出大量的热C.能去除油污,可作炉具清洁剂D.对皮肤有强烈的腐蚀作用
考点四 常见酸和碱的用途
酸和碱作用生成______和______的反应,叫作中和反应。反应的实质是酸中解离出的H+与碱中解离出的OH-反应生成水分子H++OH-===H2O
①不少中和反应没有明显的实验现象(如NaOH溶液与稀盐酸的反应),常需借助指示剂来判断反应的发生。如在碱溶液中先加入无色酚酞溶液,使溶液显红色,然后边滴加酸边振荡,当溶液由红色刚好变为无色时,酸碱恰好完全反应。
②发生中和反应时,会放出热量。
③中和反应属于将要学到的基本反应类型中的复分解反应。
(1)调节土壤的酸碱性根据土壤情况,可以利用中和反应,在土壤中加入酸性或碱性物质,调节土壤的酸碱性,以利于农作物生长。例如,用_________改良酸性土壤。
(2)处理工业废水生产过程中的污水,需进行一系列的处理。如硫酸厂的污水中含有硫酸等杂质,可以用熟石灰进行中和处理。
(3)用于医疗服用某些含有碱性物质[如Mg(OH)2]的药物以治疗胃酸过多;人们被蚊虫叮咬后肿起大包且痛痒,可以涂一些氨水、牙膏等碱性物质中和蚊虫分泌的蚁酸。
【练习5】(山东临沂中考)向NaOH溶液中滴入HC1溶液至恰好完全反应。
(1)右图表示该反应前后溶液中存在的主要离子,在右面横线上写出每种图形表示的离子(填离子符号)。
(2)反应的化学方程式是_________________________(3)下列物质中只有一种能与KOH溶液发生上述类似反应,应是_____(填序号)。 ①HNO3 ②CuSO4 ③CaCl2
NaOH + HC1== NaC1+ H2O
【练习6】(湖南益阳中考)某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,测得烧杯中溶液pH的变化如图所示。下列说法正确的是()A.a点所示溶液呈酸性B.向b点所示溶液中滴加石蕊溶液,溶液呈紫色C.该实验是将NaOH溶液逐滴滴入稀硫酸中D.c点所示溶液中,含有的溶质是Na2SO4和 NaOH
考点六 溶液酸碱度的测定及应用
1.溶液的酸碱度可用pH表示
(1)pH<7,溶液显____性,pH越____,酸性越强;(2)pH=7,溶液显____性;(3)pH>7,溶液显____性,pH越____,碱性越强。
2.pH与溶液酸碱性的关系
3.pH的测定方法:在___________上放一小片pH试纸,用干燥洁净的________蘸取待测液,滴到pH试纸上,把试纸显示的颜色与____________比较,读出pH(正整数)。
①用pH试纸测溶液的pH时,pH试纸不能用水润湿,否则会起到稀释待测溶液的作用,使结果不准确。
②不能将pH试纸直接放入待测溶液中,会污染试剂。
4.溶液酸碱度的重要意义
(1)化工生产中许多反应必须控制在一定pH范围内。(2)农作物适宜在pH为____或接近____的土壤中生长。(3)测定雨水的pH(酸雨的pH小于_____),可以了解空气的污染情况。(4)测定人体内或排出的液体的pH,可以了解人体的健康状况。
【练习7】(四川广安中考)一些食物的近似pH如下:
下列说法正确的是()A. 鸡蛋清和牛奶显碱性B. 要补充维生素可以多吃鸡蛋清C. 苹果汁的酸性比葡萄汁弱D. 胃酸过多的人应少饮葡萄汁和苹果汁
1.误认为酸性溶液就是酸溶液,碱性溶液就是碱溶液。另外酸性溶液和碱性溶液都能导电。2.滴入酚酞溶液显无色,误认为就是中性溶液。3.把酸碱指示剂在酸碱溶液中的变色,误认为是酸碱溶液的变色。4.中和反应一定生成盐和水,但有盐和水生成的反应不一定是中和反应。5.测溶液的酸碱度时,pH试纸不能用水润湿、不能直接插入待测液中,测得的pH只能为正整数,不能为小数。
1.常见酸(HCl、H2SO4)的反应
①______________________________②______________________________③______________________________④______________________________⑤______________________________⑥______________________________⑦______________________________
请写出稀硫酸与各物质反应的化学方程式
2.常见碱[NaOH、Ca(OH)2]的反应
人教版中考化学复习第十单元酸和碱第1课时常见的酸和碱练习课件: 这是一份人教版中考化学复习第十单元酸和碱第1课时常见的酸和碱练习课件,共32页。PPT课件主要包含了金属氧化物,稀硫酸,溶液由红色变为无色等内容,欢迎下载使用。
人教版中考化学复习第十单元酸和碱第1课时常见的酸和碱作业课件: 这是一份人教版中考化学复习第十单元酸和碱第1课时常见的酸和碱作业课件,共27页。PPT课件主要包含了稀盐酸,有气泡产生,气球膨胀,稀硫酸,CaOH2,有红褐色沉淀生成,酚酞溶液等内容,欢迎下载使用。
人教版化学中考复习 10.第十单元 酸和碱 PPT课件+练习: 这是一份人教版化学中考复习 10.第十单元 酸和碱 PPT课件+练习,文件包含第十单元酸和碱pptx、第十单元酸和碱docx等2份课件配套教学资源,其中PPT共60页, 欢迎下载使用。














