




高中化学鲁科版 (2019)必修 第二册第2节 元素周期律和元素周期表教课内容ppt课件
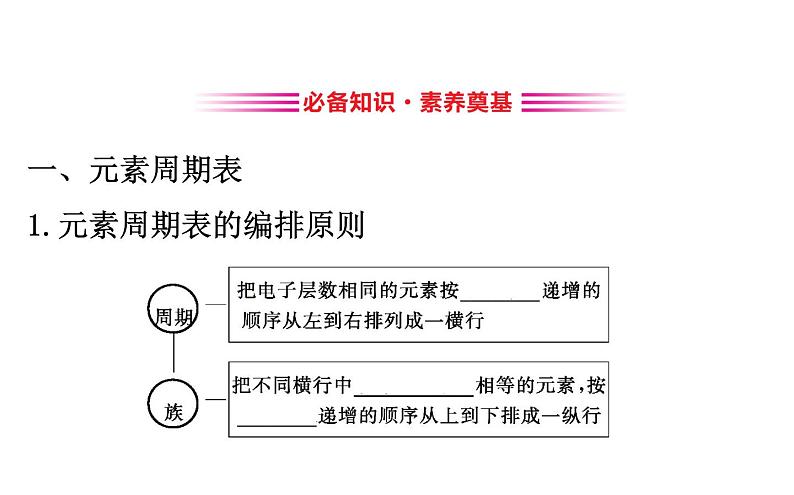
展开一、元素周期表1.元素周期表的编排原则
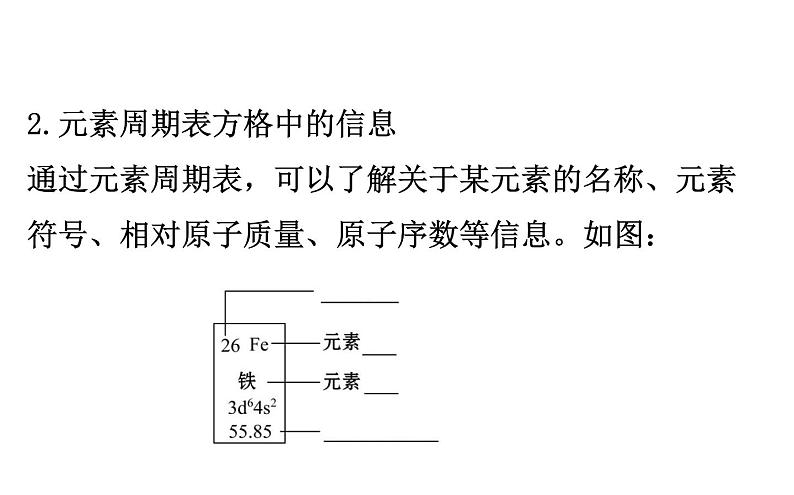
2.元素周期表方格中的信息通过元素周期表,可以了解关于某元素的名称、元素符号、相对原子质量、原子序数等信息。如图:
【巧判断】(1)元素周期表中共有18个纵行,16个族。( )提示:√。周期表中除第Ⅷ族为3个纵行,其余的每一纵行为一族。因此共有18个纵行,16个族。
(2)元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素。( )提示:×。镧系和锕系各含有15种元素,不是同位素,同位素的研究对象是核素而不是元素。
(3)0族、ⅡA族、Ⅷ族中都既有短周期元素,又有长周期元素。( )提示:×。第Ⅷ族元素只有长周期元素。
4.分区(1)元素周期表的分区。
(2)分界线附近元素的性质:既能表现出一定的________,又能表现出一定的_________。
二、周期表中部分重要的元素和焰色反应1.周期表中重要的元素
【情境·思考】铁是我们日常生活中应用最广的金属材料,你能在元素周期表中找到铁元素的位置吗?
提示:铁位于元素周期表中第4周期,第Ⅷ族,属于过渡元素。
2.焰色试验(1)定义:某些_______________________在灼烧时火焰呈现特征颜色的反应,如钠:黄色,钾:_______ 色。
【微思考】观察钾元素的焰色试验时,要透过蓝色钴玻璃进行,这是为什么?
提示:用蓝色的钴玻璃将黄色的光滤去,便于观察到紫色。
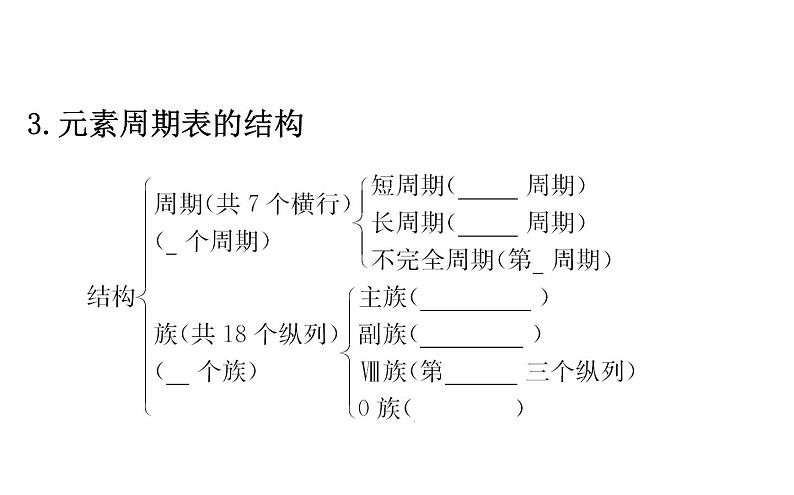
知识点一 元素周期表的结构1.元素周期表的结构
4.元素周期表结构中隐含的两条规律(1)同周期主族元素原子序数差的关系。①短周期元素原子序数差=族序数差。②两元素分布在过渡元素同侧时,原子序数差=族序数差。两元素分布在过渡元素两侧时,4或5周期元素原子序数差=族序数差+10,第6周期元素原子序数差=族序数差+24。
③4、5周期的ⅡA与ⅢA族原子序数之差都为11,第6周期为25。
(2)同主族邻周期元素的原子序数差的关系。①ⅠA族元素,随电子层数的增加,原子序数依次相差2、8、8、18、18、32。②ⅡA族和0族元素,随电子层数的增加,原子序数依次相差8、8、18、18、32。③ⅢA~ⅦA族元素,随电子层数的增加,原子序数依次相差8、18、18、32。
【记忆口诀】元素周期表结构巧记口诀横行叫周期,现有一至七,四长三个短,第七尚不满。纵列称为族,共有十六族,一八依次现①,一零再一遍②。一纵一个族,Ⅷ族搞特殊,三纵算一族,占去8、9、10。
镧系与锕系,蜗居不如意,十五挤着住,都属ⅢB族。说明:①指ⅠA、ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ;②指ⅠB、ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0。
【思考·讨论】(1)该元素周期表中的每种元素有很多信息,如氧元素 ,其中的8、O、16.00分别代表什么意义?
提示:分别代表原子序数、元素符号、相对原子质量。
(2)原子最外层有2个电子的元素一定是第ⅡA族元素吗?哪一族全部是金属元素?哪一族全部是非金属元素?提示:不一定。原子最外层电子数为2的元素包括ⅡA族、氦及部分过渡元素;第ⅡA族、Ⅷ族及全部副族元素全部为金属元素;第ⅦA族、0族全部为非金属元素。
【案例示范】【典例】(2020·芜湖高一检测)短周期元素A、B、C在周期表中的位置如图所示。已知B、C两元素的原子序数之和是A元素的4倍,则A、B、C是( )
A.Be、Na、Al B.B、Mg、Si C.O、P、Cl D.C、Al、P
【解题指南】解答本题时应注意以下两点:(1)短周期是指1~3周期;(2)短周期中第ⅡA与ⅢA族是不直接相邻的。
【解析】选C。短周期元素A、B、C,设A的原子序数为m,则B、C的原子序数分别为m+8-1和m+8+1,由题意知(m+8-1)+(m+8+1)=4m,则m=8,故选C。
【母题追问】(1)写出A、B、C三种元素在周期表中的位置。提示:A元素为O,位于第2周期ⅥA族;B元素为P,位于第3周期ⅤA族;C元素为Cl,位于第3周期ⅦA族。
(2)比较B、C元素原子的半径大小,A、C元素形成的简单离子的半径大小。提示:B、C位于同一周期,电子层数相同,而C的原子序数大,因此半径小,故r(P)>r(Cl)。A、C元素形成的简单离子分别为O2-和Cl-,二者最外层电子均为8个,Cl-的电子层数多,故半径大,因此r(O2-)
A.Y与Z的原子序数之和可能为2aB.Y的原子序数可能为a-17C.Z的原子序数可能为a+31D.X、Y、Z一定为短周期元素
【解析】选D。由题给信息可知,X、Y、Z只能位于元素周期表中过渡元素区域的右边,则若Y为第三周期元素,则由X的原子序数为a可知,Y的原子序数为a-18+1=a-17,Z的原子序数为a+18-1=a+17,A正确;若X为长周期非金属元素,Y为短周期非金属元素,则Y的原子序数可能为a-18+1=a-17,B正确;若Z为第6或第7周期元素,因存在镧系和锕系元素,则Z的原子序数可能为a+32-1=a+31,C正确。
【补偿训练】1.第ⅤA族元素中的A、B两种元素所在周期分别最多可排18和8种元素,且B在A的上一周期,当A的原子序数为x时,B的原子序数为( )A.x-18B.x-8C.x+8D.x+18
【解析】选A。B、A所在周期相邻,A、B最多可排18和8种元素,所以B在第3周期,A在第4周期,A、B为ⅤA族元素,其原子序数差为18。
2.(2020·镇江高一检测)甲、乙是周期表中同主族的相邻元素,若甲的原子序数为x,则乙的原子序数不可能是( )A.x+2B.x+4C.x+8D.x+18
【解析】选B。若元素在ⅠA、ⅡA族,则两种元素的原子序数之差应是上一周期元素种数,若元素在ⅢA~ⅦA族,则两种元素的原子序数之差应为下一周期元素种数。又因为每一周期所含元素种数可以是2、8、18、32,所以同主族相邻元素原子序数之差可能为2、8、18、32。
3.(2020·舟山高一检测)下列各表为周期表的一部分(表中数字为原子序数),其中正确的是( )
【解析】选D。A项中,2号元素应该位于周期表的最后一列,错误;B项中,2号、3号、4号元素不应该在同一周期,因为第1周期只有H、He两种元素,错误;C项中,6号、12号和24号元素不应在同一主族,因为同主族相邻元素原子序数之差为2、8、18等,不存在相差6或12的情况,错误;D项,完全符合元素周期表的排列规则,正确。
知识点二 原子结构与元素在周期表中的位置的关系1.由原子序数确定元素在周期表中的位置(1)原子结构示意图法。推断根据:周期数=原子电子层数,主族序数=原子最外层电子数。适用范围:主族元素,适合原子序数较小的元素位置推断。
(2)0族定位法。①0族元素原子序数与周期序数:
②比大小,定周期;求差值,定族数:若某元素原子序数比最邻近的0族元素的原子序数多1或2,则该元素处于相邻近0族元素下一周期的ⅠA族或ⅡA族。如元素X-87,87-86=1,则X在第7周期第ⅠA族;若某元素原子序数比最邻近的0族元素的原子序数少1~5时,则该元素处于相邻近0族元素所在周期的ⅢA~ⅦA族,如X-84应在第6周期第ⅥA族。
2.根据核外电子排布规律推断元素在周期表中的位置(1)“阴上阳下”规律。电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的下一周期。例如,A、B、C、D为短周期元素,其简单离子A+、B2+、C-、D2-具有相同电子层结构,则A、B、C、D在元素周期表的相对位置为
(2)奇偶规律。原子序数为奇(偶)数的主族元素位于奇(偶)数族,元素(F和O除外)的最高正价为奇(偶)数。
【易错提醒】(1)同主族相邻元素的原子序数的差值只能为2、8、18、32。(2)同周期ⅡA、ⅢA族的元素原子序数的差值可能为1、11、25。
(3)电子层结构相同的离子在周期表中的位置关系。①阳离子:几种阳离子具有相同的电子层结构,这些离子处于同一周期,离子所带电荷数值大的在电荷数值小的元素的右侧。
②阴离子:几种阴离子具有相同的电子层结构,这些离子处于同一周期,离子所带电荷数值大的在电荷数值小的元素的左侧。③阴、阳离子:阳离子和阴离子具有相同的电子层结构,阳离子对应元素的周期位于阴离子对应元素所处周期的下一周期,不同阴离子、阳离子的位置按照①、②方法确定。
【思考·讨论】(1)原子序数为x的元素位于元素周期表中的第ⅡA族,则原子序数为x+1的元素位于元素周期表的哪一族?
提示:ⅢA族或ⅢB族。原子序数为x+1的元素应位于ⅡA族右侧相邻的族,在短周期中为ⅢA族,长周期中为ⅢB族。
(2)同周期ⅡA族与ⅢA族元素的原子序数之差一定是1吗?请举例说明。
提示:不一定。具体举例如下:
(3)ⅠA族或ⅡA族元素相邻周期的原子序数之差,ⅢA~ⅦA族或0族元素相邻周期的原子序数之差各有什么特点?
提示:ⅠA和ⅡA族元素相邻周期的原子序数之差=原子序数小的元素所在周期的元素种类数。ⅢA~ⅦA族和0族元素相邻周期的原子序数之差=原子序数大的元素所在周期的元素种类数。
【案例示范】【典例1】(2020·唐山高一检测)已知某离子的结构示意图为 ,下列说法正确的是( )A.该元素位于第2周期ⅡA族B.该元素位于第2周期Ⅷ族C.该元素位于第3周期ⅡA族D.该元素位于第3周期0族
【思维建模】由电子层结构推断元素位置的思路为:
【解析】选C。该元素原子的结构示意图为 ,电子层数等于周期序数,最外层电子数等于主族序数,即该元素位于第3周期ⅡA族。
【典例2】(2020·莱芜高一检测)元素周期表是一座开放的“元素大厦”,元素大厦尚未客满。若发现119号元素,请你在元素大厦中安排好它的“房间”( )A.第7周期0族B.第6周期ⅡA族C.第8周期ⅠA族D.第7周期ⅦA族
【思维建模】由原子序数推断元素位置的思路为:
【解析】选C。0族第6周期元素的原子序数为86→第7周期若排满元素,种数为32→86+32=118<119→119号为第8周期ⅠA族。
【情境·迁移】据国外有关资料显示,在独居石(一种共生矿,化学成分为Ce、La、Nd……的磷酸盐)中,查明有116号元素和尚未命名的124、126号元素。思考116号元素在周期表中的位置。
提示:根据86Rn为第6周期稀有气体元素,推测出下一周期末的稀有气体元素为118号元素,再向前推,116号元素应位于第7周期ⅥA族。
【知识·巩固】1.某主族元素R的质量数为79,已知R离子含有45个中子和36个电子,下列关于R元素的叙述错误的是( )A.R元素属于ⅡA族B.R元素在周期表中处于第4周期
C.该离子可以表示为R2- D.R元素最高价氧化物的分子式为RO3
【解析】选A。R原子的质子数=79-45=34,原子核外电子数为34,故该离子为阴离子,符号为R2-,C对;质子数为36的稀有气体氪处于第4周期,故该元素也位于第4周期,R原子比氪原子质子数少2,R属于ⅥA族,故A错、B对;ⅥA族元素最高价为+6价(氧除外),最高价氧化物的分子式为RO3,D对。
2.(2020·北师大附中高一检测)据报道,某些花岗岩会产生氡 ),从而对人体产生伤害,元素Rn在周期表中的位置是( )A.第5周期Ⅷ族B.第6周期Ⅷ族C.第6周期0族D.第5周期ⅦA族
【解析】选C。Rn的原子结构示意图为 ,故为第6周期0族元素。
【补偿训练】 1.俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子成功合成第115号元素的原子。该原子生成数微秒后衰变成第113号元素。下列有关叙述正确的是( )A.115号元素在第6周期
B.113号元素在第7周期ⅢA族C.115号和113号元素都是非金属元素D.镅元素和115号元素不在同一周期
【解析】选B。根据同族元素原子序数的序差规律,可以推知稀有气体Rn的原子序数为86,Rn-86的同族下一周期元素原子序数为118,95号元素镅、115号元素、113号元素,原子序数都大于86而小于118,所以都在第7周期;115号比118号原子序数少3,应在第ⅤA族,同理,113号元素在第ⅢA族;113号元素和115号元素都是金属元素。
ml 中共有30 ml电子,则R在元素周期表中的位置是( )A.第2周期ⅤA族 B.第3周期ⅣA族 C.第2周期ⅥA族 D.第3周期ⅦA族
【解析】选B。设R的原子序数为x,则 核外共有电子数为x+3×8+2=x+26,由题意得(x+26)×0.75 ml=30 ml,则x=14,即R为硅元素,Si核外有3个电子层,最外层有4个电子,因此硅元素位于元素周期表中第3周期ⅣA族。
鲁科版 (2019)必修 第二册第1章 原子结构 元素周期律第2节 元素周期律和元素周期表备课课件ppt: 这是一份鲁科版 (2019)必修 第二册第1章 原子结构 元素周期律第2节 元素周期律和元素周期表备课课件ppt,共57页。PPT课件主要包含了元素周期律,化合态,铍Be,镁Mg,钙Ca,导电性,PAs,~12,浅紫色,元素周期表的结构等内容,欢迎下载使用。
化学必修 第二册第2节 元素周期律和元素周期表教案配套课件ppt: 这是一份化学必修 第二册第2节 元素周期律和元素周期表教案配套课件ppt,共37页。PPT课件主要包含了知识铺垫,新知预习,自主测试,2ⅤA族元素,3过渡元素,任务一,任务二,素养脉络,随堂检测,答案D等内容,欢迎下载使用。
鲁科版 (2019)必修 第二册第3节 元素周期表的应用课文内容ppt课件: 这是一份鲁科版 (2019)必修 第二册第3节 元素周期表的应用课文内容ppt课件,共60页。PPT课件主要包含了必备知识·自主学习,逐渐增多,逐渐增大,化合态,HClO4,HBrO4,HIO4,HCl,HBr,深红棕等内容,欢迎下载使用。













