

【化学】江西省南昌市进贤一中2019-2020学年高二上学期期末考试试卷
展开江西省南昌市进贤一中2019-2020学年高二上学期期末考试试卷
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Mg—24 P—31 S—32 Cl—35.5 Fe—56
第Ⅰ卷(选择题,共48分)
一、选择题(本题包括16小题,每小题只有一个选项符合题意,每小题3分,共48分)
1.下列与化学反应能量变化相关的叙述正确的是(( )
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下
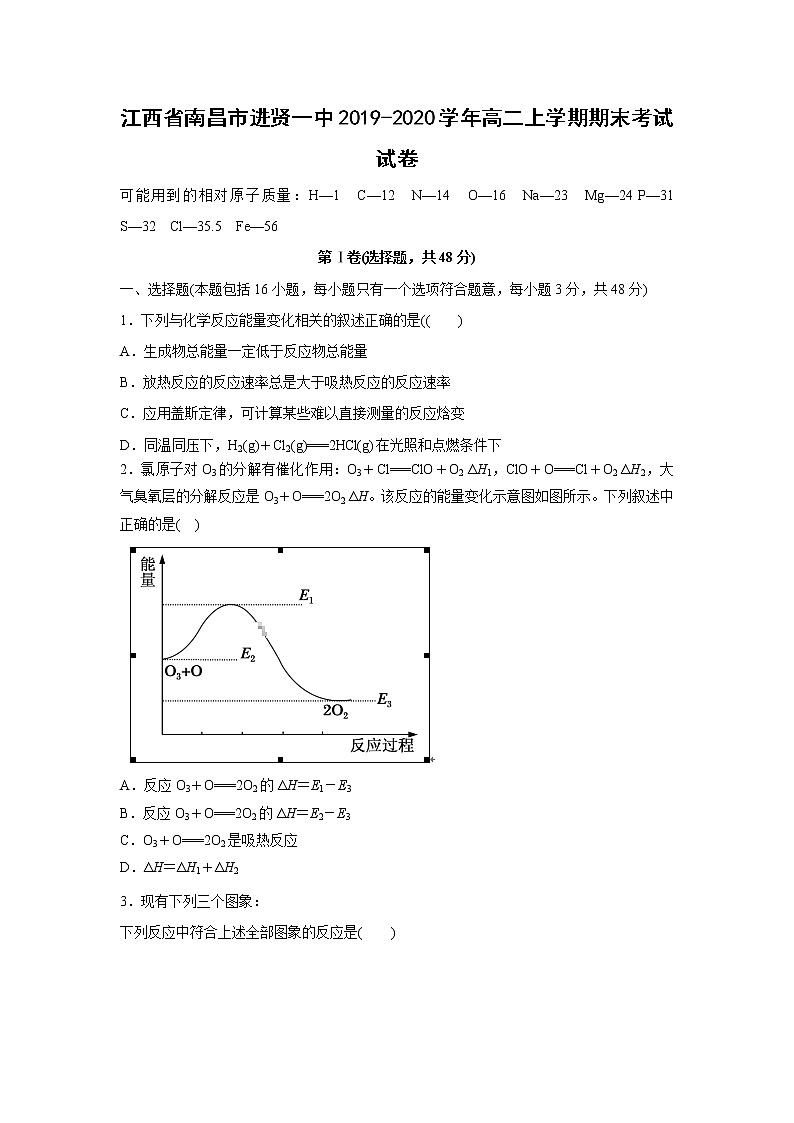
2.氯原子对O3的分解有催化作用:O3+Cl===ClO+O2 ΔH1,ClO+O===Cl+O2 ΔH2,大气臭氧层的分解反应是O3+O===2O2 ΔH。该反应的能量变化示意图如图所示。下列叙述中正确的是( )
A.反应O3+O===2O2的ΔH=E1-E3
B.反应O3+O===2O2的ΔH=E2-E3
C.O3+O===2O2是吸热反应
D.ΔH=ΔH1+ΔH2
3.现有下列三个图象:
下列反应中符合上述全部图象的反应是( )
A.N2(g)+3H2(g)⇌2NH3(g) ΔH<0
B.2SO3(g)⇌2SO2(g)+O2(g) ΔH>0
C.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH<0
D.H2(g)+CO(g)⇌C(s)+H2O(g) ΔH>0
4.在水中加入下列物质,可以促进水的电离的是( )
A.H2SO4 B.NaOH C.Na2CO3 D.KNO3
5.下列能说明醋酸是弱酸的是( )
A.醋酸能与NaOH反应 B.醋酸能使石蕊变红
C.醋酸溶液pH<7 D.常温下0.1 mol·L-1醋酸pH=3
6.有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是( )
A.Cu是原电池的负极
B.Al是原电池的负极
C.电子由Al沿导线流向铜
D.铝片上的电极反应式为:Al-3e-===Al3+
7.在一定条件下发生反应:2A(g) ⇌ 2B(g)+C(g);将2 mol A通入2 L容积恒定的密闭容器中,若维持容器内的温度不变,5 min末测得A的物质的量为0.8 mol,用B的浓度变化来表示该反应的速率为( )
A.0.24 mol/(L· min) B.0.08 mol/(L·min)
C.0. 06 mol/(L·min) D.0.12 mol/(L·min)
8.下列溶液中有关粒子的物质的量浓度关系正确的是( )
A.氯水中:2c(Cl2)=c(ClO-)+c(Cl-)+c(HClO)
B.25℃时,pH=12的NaOH溶液与pH=12的氨水:c(Na+)=c(NH4+)
C.pH=4的0.1 mol·L-1的NaHA溶液中:c(HA-)>c(H+)>c(H2A)>c(A2-)
D.在K2CO3溶液中:c(CO32-)+c(OH-)=c(HCO3-)+c(H+)
9.常温下在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH-离子浓度分别为A mol/L与B mol/L,则A和B关系为( )
A.A>B B.A=10-4B C.B=10-4A D.A=B
10.已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol
N2(g)+O2(g)===2NO(g) ΔH=+180 kJ/mol
则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH是( )
A. -386 kJ/mol B. +386 kJ/mol
C. -746 kJ/mol D. +746 kJ/mol
测定时刻/s | t1 | t2 | t3 | t4 |
c(A)/(mol·L-1) | 6 | 3 | 2 | 2 |
c(B)/(mol·L-1) | 5 | 3.5 | 3 | 3 |
c(C)/(mol·L-1) | 1 | 2.5 | 3 | 3 |
11.在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如下表。据此判断下列结论正确的是( )
A.在t3时刻反应已经停止
B.A的转化率比B的转化率低
C.在容器中发生的反应为:2A+B⇌2C
D.在t2~t3内A的平均反应速率为:[1/(t3-t2)] mol·L-1·s-1
相关化合物 | AgX | AgY | AgZ |
pKsp | a | b | c |
12.如表为有关化合物的pKsp,pKsp=-lgKsp。某同学设计实验如下:①向AgNO3溶液中加入适量NaX溶液,得到沉淀AgX;②向①中加NaY,则沉淀转化为AgY;③向②中加入NaZ,沉淀又转化为AgZ。则表中a、b、c的大小关系为( )
A.a>b>c B.a<b<c C.c<a<b D.a+b=c
13.下列事实不能用勒夏特列原理解释的是( )
A.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
B.增大压强可加快SO2转化为SO3的速率
C.黄绿色的氯水光照后颜色变浅
D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
14.α-AgI是一种固体导体,导电率很高。为研究α-AgI到底是Ag+导电还是I-导电,设计了如下实验,下列有关说法不正确的是( )
A.若α-AgI是Ag+导电,则通电一段时间后晶体质量不变
B.若α-AgI是Ag+导电,则通电一段时间后晶体质量减少
C.阳极反应为:Ag-e-===Ag+
D.阴极质量不断增加
15.下图为某化学反应速率一时间图象。在t1时刻升高温度和增大压强都符合下图所示变化的反应是( )
A.2SO2(g)+O2(g)⇌2SO3(g) ΔH<0
B.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH<0
C.H2(g)+I2(g)⇌2HI(g) ΔH>0
D.C(s)+H2O(g)⇌CO(g)+H2(g) ΔH>0
16.向盛有NaHSO4溶液的烧杯中不断滴加Ba(OH)2溶液,随着Ba(OH)2的不断滴入,溶液中产生的沉淀量与溶液pH变化情况正确的是( )
第Ⅱ卷(非选择题,包括6小题,共52分)
17.(4分)能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25 ℃、101 kPa时,16 g CH4完全燃烧生成液态水时放出的热量是890.31 kJ,则CH4燃烧的热化学方程式是_______________ _________________________________________________________。
(2)已知:C(s)+O2(g)===CO2(g);ΔH=-437.3 kJ·mol-1
H2(g)+
CO(g)+
则煤的气化主要反应的热化学方程式是:C(s)+H2O(g)===CO(g)+H2(g);ΔH=________kJ/mol。
18.(7分)常温下,用0. 1000 mol/LNaOH溶液分别滴定20.00 mL 0.1000 mol/L HCl溶液和20.00 mL 0.1000 mol/L CH3COOH溶液,得到2条滴定曲线,如下图所示:
(1)由A、C点判断,滴定HCl溶液的曲线是________(填“图1”或“图2”);
(2)a=________mL;
(3)c (Na+)=c (CH3COO-)的点是________;
(4)E点对应离子浓度由大到小的顺序为_________________。
19.(9分)二甲醚(CH3OCH3)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能。
Ⅰ.工业制备二甲醚的生产流程如下:
催化反应室中(压强2.0~10.0 MPa,温度230~280 ℃)进行下列反应:
CO(g)+2H2(g)⇌CH3OH(g) ΔH=-90.7 kJ/mol ①
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ/mol ②
CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH=-41.2 kJ/mol ③
(1)甲烷氧化可制得合成气,反应如下:CH4(g)+O2(g)⇌CO(g)+2H2(g) ΔH=-35.6 kJ/mol。该反应是________反应(填“自发”或“非自发”)。
(2)催化反应室中总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)的ΔH=________。830 ℃时反应③的K=1.0,则在催化反应室中反应③的K________1.0(填“>”、“<”或“=”)。
(3)上述反应中,可以循环使用的物质有________。
Ⅱ.如图为绿色电源“二甲醚燃料电池”的工作原理示意图.b电极是________极。
20.(12分)如图甲、乙是电化学实验装置。
若甲、乙两烧杯中均盛有NaCl溶液。
(1)①甲中石墨棒上的电极反应式为_______________________ ______。
②乙中总反应的离子方程式为__________ ____________________________________。
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2.若反应中Cl2和I2的物质的量之比为5:1,且生成两种酸,该反应的化学方程式为_______ ________________________________________________。
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为_____________________ ______________。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入________(填写物质的化学式)________g。
21.(7分)高炉炼铁过程中发生的主要反应为:
Fe2O3(s)+CO(g) ⇌ Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=________,ΔH________0(填“>”、“<”或“=”);
(2)在体积为10 L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。该时间范围内反应的平均反应速率v(CO2)= ,CO的平衡转化率为 ___。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________。
A.减少Fe的量 B.增加Fe2O3的量
C.移出部分CO2 D.提高反应温度
E.减小容器的容积 F.加入合适的催化剂
22.(13分)室温下,向20 mL 0.1 mol/L的醋酸溶液中逐滴加入0.1 mol/L的氢氧化钠溶液,直至氢氧化钠溶液过量。
(1)写出反应的离子方程式:_________________________。
(2)在实验的整个过程中,水的电离程度的变化趋势是
_____________________________________________________。
(3)请在下表的空格部分填上相应的内容,将表格补充完整(NaOH的体积、pH栏中填写“>”“<”或“=”)。
加入NaOH 的体积/mL | 离子浓度从大到小的顺序 | 溶液中所含溶质的化学式 | 溶液的pH |
①=10 mL |
|
| <7 |
②__20 mL |
|
| =7 |
③__20 mL |
| CH3COONa | ____7 |
④__20 mL |
| CH3COOH、 NaOH | ____7 |
【参考答案】
1——16 CDBCD, ADBBC; DBBBB, A
17.(4分)
(1)CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.31 kJ/mol(2分) (2)+131.5(2分)
18.(7分)
(1)图1(1分) (2)20.00(2分) (3)D(2分) (4)c(Na+)>c(CH3COO-)>c(OH-)>c(H+)(2分)
19.(9分)
Ⅰ.(1)自发(2分) (2) -246.1 kJ/mol(2分) >(2分) (3)CO、H2、甲醇和水(2分)
Ⅱ.正(1分)
20.(12分每空2分)(1)①2H2O+O2+4e-===4OH-
②2Cl-+2H2OH2↑+Cl2↑+2OH-
③5Cl2+I2+6H2O===10HCl+2HIO3
(2)①Fe-2e-===Fe2+ ②CuO(或CuCO3) 0.8(或1.24)
21.(7分)(1)(1分) <(1分)
(2)0.0060 mol/(L·min)(2分) 60%(2分) (3)C(1分)
22.(13分每空1分) (1)OH-+CH3COOH===CH3COO-+H2O
(2)先增大 后变小
(3)①c(CH3COO-)>c(Na+)>c(H+)>c(OH) CH3COOH、CH3COONa
②< c(CH3COO-)=c(Na+)>c(H+)=c(OH-) CH3COOH、CH3COONa
③= c(Na+)>c(CH3COO-)>c(OH-)>c(H+) >
④> c(Na+)>c(CH3COO-)>c(OH-)>c(H+) >








