苏教版专题1 化学家眼中的物质世界第一单元 丰富多彩的化学物质教学设计及反思
展开第一单元 丰富多彩的化学物质
学海导航
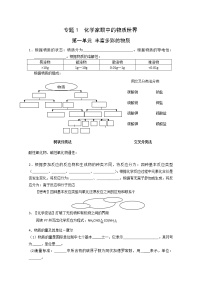
一、物质的分类
纯净物
物质
混合物
二、单质、氧化物酸、碱、盐等物质之间的相互转化关系注意:复分解反应的条件:有沉淀、气体、水生成。金属与盐溶液的置换条件:活泼性强的金属置换活泼性弱的金属。
三、有关物质的量、阿伏加德罗常数、摩尔质量、气体摩尔体积等概念
1.物质的量:物质的量是七个基本物理量之一,其单位是摩尔(mol),符号为n,注意:(1)物质的量度量的对象是微粒集体,微粒可以是分子、原子、离子、电子、中子、质子等。(2)使用物质的量一般用符号标明微粒,如1mol H2O,5mol H+等。摩尔作为物质的量的单位,不能用来表示宏观物体的多少,使用摩尔时必须指明微粒的种类。
2.阿伏加德罗常数:1mol任何微粒集体中所含有的微粒数叫做阿伏加德罗常数。用符号NA表示,通常使用近似值6.02×1023mol-1。
3.摩尔质量:1mol任何物质的质量,称为该物质的摩尔质量。用符号M表示,单位为g/mol。 1mol物质的质量以克为单位,在数值上等于该物质的相对原子质量或相对分子质量。物质的量与质量、摩尔质量的关系为:n=m/M
4.气体摩尔体积:单位物质的量的气体所占的体积叫做气体摩尔体积。用符号Vm表示,常用的单位为L/mol。标准状况下(0℃、101Kpa),1mol任何气体所占的体积都约为22.4L,即标况下的气体摩尔体积约为22.4L/mol
四、物质的聚集状态及分散系
1.物质的聚集状态:主要有气态、液态和固态三种。同一物质在不同温度和压力下物质的聚集状态不同。物质的体积由三个因素决定:微粒数目、微粒间距、微粒大小。固体、液体的体积主要决定于微粒数目和微粒大小;而气体的体积主要决定于微粒数目、微粒间距。
2.分散系:一种或几种物分散到另一种物质中形成的混合物叫分散系。被分散的物质叫分散质,分散其他物质的物质叫分散剂。可分为:溶液(粒子直径小于10-9m)、浊液(粒子直径大于10-7m)、胶体(粒子直径在10-9 ~ 10-7m)
3.胶体:胶体与溶液外观上没有区别,都是均一、稳定、透明的分散系。其特性:具有丁达尔效应,利用此特性可鉴别溶液和胶体。有些胶体具有吸附性,可作净水剂,除去水中不溶性杂质,使水澄清。比如氢氧化铝胶体、氢氧化铁胶体等。
例题解析
例1. 今有下列三组物质,每组中都有一种物质跟其他三种属于不同的种类。将此种物质(写化学式)和分类依据(选出的物质与其他物质不同之处)写在下面相应的表格内。三组物质分别为:(1)O2、F2、S、N2;(2)Fe、Na、Al、Si;(3)NO、CO2、SO2、P2O5。
组别 | 被选出的物质 | 挑选依据 |
第(1)组 |
|
|
第(2)组 |
|
|
第(3)组 |
|
|
解析:本题中,第(1)组物质可根据物质在通常状态下的聚集状态分类,第(2)组物质可根据物质的性质分成金属和非金属两种类型,第(3)组物质均为非金属氧化物,可根据它们在通常状态下的聚集状态分类。
故答案为:第(1)组:S 通常情况下,S是固体,其余均为气体。
第(2)组:Si 只有Si是非金属单质,其余是金属单质。
第(3)组:P2O5 均为非金属氧化物,但P2O5为固体,其余的通常情况下为气体。
例2. 同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1) 生石灰属于哪种类别的物质?
(2) 生石灰可做干燥剂的理由是什么?(用化学方程式表示)
(3) 生石灰还可以跟哪些类别的物质发生化学反应?列举两例,并写出化学方程式
(4) 小纸袋中的物质能否长期持续地做干燥剂?为什么?
(5) 在你所认识的化学物质中,还有哪些可以用作干燥剂?列举一例。
答案:(1)化合物、金属氧化物、固态物质等。
(2)CaO + H2O = Ca(OH)2
(3)与酸的反应:CaO + 2HCl = CaCl2 + H2O ;与非金属氧化物反应:CaO + CO2 = CaCO3
(4)不能,因为生石灰全部变为Ca(OH)2后,就不能持续起到干燥作用。
(5)浓硫酸、CaCl2、 P2O5 、碱石灰等
例3. 氯的原子序数为17,35Cl是氯的一种同位素,下列说法正确的是 ( )
A.35Cl原子所含质子数为18 B.1/18 mol的1H35Cl分子所含中子数约为
C.3.5g的35Cl2气体的体积为2.24L D.35Cl2气体的摩尔质量为70 g/mol
解析:该题以35Cl为背景,考查了35Cl原子所含质子数、1H35Cl分子所含中子数以及35Cl2气体的摩尔质量、气体摩尔体积、物质的量等之间的关系,其中1H是所有原子中唯一无中子的原子,“3.5g的35Cl2气体的体积为2.24L”中设置了状态未确定的陷阱。故答案为:B、D
例4. 在某温度时,一定量的元素A的氢化物AH3在一定体积密闭容器中可完全分解成两种气态单质,此时压强增加了75%。则A单质的一个分子中有_______个A原子,AH3分解反应的化学方程式为__________________________________________。
解析:由阿伏加德罗定律的推论:相同温度和压强时,p1/p2=N1/N2得反应前后气体的分子数之比为1:1.75=4:7,可理解为反应式左边气体和反应式右边气体系数之和比为4:7,再根据氢原子守恒不妨先将反应式写为4AH3==A(x)+6H2,再由A原子守恒得A右下角的数字为4。
答案:4,4AH3==A4+6H2。
习题精练
1.下列广告用语在科学性上没有错误的是( )
A.这种饮料中不含任何化学物质
B.这种蒸馏水绝对纯净,其中不含任何微粒
C.这种口服液含丰富的氮.磷.锌等微量元素
D.没有水就没有生命
2.“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅.铝制的易拉罐.铜导线等可以归为一类加以回收,它们属于( )
A. 氧化物 B. 盐 C. 金属或合金 D. 碱
3.下列物质属于纯净物的是( )
A.洁净的空气 B.食盐水 C.浮有冰块的水 D.糖水
4.经测定,一瓶气体中只含有C.H两种元素,通常情况下这瓶气体不可能是( )
A.一种化合物 B.一种单质和一种化合物的混合物
C.两种化合物 D.两种单质
5.“可燃冰”又称“天然气化合物”,它是在海底的高压.低温条件下形成的,外观像冰。1体积“可燃冰”可储藏100~200体积的天然气。下面关于“可燃冰”的叙述不正确的是( )
- “可燃冰”有可能成为人类未来的重要能源
- “可燃冰”是一种比较洁净的能源
- “可燃冰”提供了水可能变成油的例证
D.“可燃冰”的主要可燃成分是甲烷
6.下列叙述中正确的是( )
- 硝酸的摩尔质量63g
- 1mol CO的质量是28g
- 2g氢气所含原子数目为1mol
- 铁的摩尔质量在数值上等于铁原子的相对原子质量
7.相同质量的下列气体中,所含原子数最多的是( )
A.CH4 B.N2 C.CO D.O2
8.下列说法中错误的是( )
- 物质的聚集状态不同主要是构成物质的基本粒子间的距离不同
- 不同分散系其对应分散质的微粒直径不同
- 1mol O2与1mol O3所含的分子数目相等
- 1mol氢气所占体积约为22.4L
9.设NA为阿伏加德罗常数,下列说法中正确的是( )
- 1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
- 18g水含有电子数为8NA
- 标准状况下,22.4L氢气含有氢原子个数为2NA
- 11.2L氢气一定含有NA 个氢原子
10.能区分胶体和溶液的方法是( )
- 静置,有沉淀现象的是胶体
- 有丁达尔现象的是胶体
- 能透过滤纸的是溶液
- 用肉眼观察,均匀透明的是溶液
11.下列关于Fe(OH)3胶体的制备,正确的操作是 ( )
- 将FeCl3 溶液滴入蒸馏水中即可
- 将FeCl3 溶液滴入热水中,得到黄色液体即可
- 将FeCl3 溶液滴入沸水中,得到红褐色液体即可
- 将FeCl3 溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀即可
12.(1)1.5molH2SO4的质量是_____________,其中含有__________mol H,含有_______g氧元素。
(2)9.03×1023个氨分子含___________摩尔氨分子,____________摩尔氢原子,________摩尔质子,________________个电子。
(3)__________mol CO2中含有3g碳。标况下,___________L CO2中含有0.25mol 氧原子,____________mol CO2中含有3.01×1023个CO2分子,它的质量是______________。
13. 按下列化学反应基本类型依次填入四个化学方程式,要求后一个反应的反应物必须含有前一个反应的生成物:
(1) 分解反应:_______________________________________________________。
(2) 置换反应:_______________________________________________________。
(3) 化合反应:_______________________________________________________。
(4) 复分解反应:_____________________________________________________。
14. 同温同压下,某容器充满O2重16g,若充满CO2重22g,现充满某气体重44g,则某气体的摩尔质量为多少?
15. 实验室加热氯酸钾和二氧化锰的混合物制取氧气。若收集到标准状况下3.36L氧气,至少需要多少克氯酸钾?同时生成氯化钾的物质的量为多少?
习题精练答案:
1.D 2.C 3.C 4.D 5.C 6.BD 7.A 8.D 9.C 10.B 11.C
12.(1)147g, 3.0, 96 (2)1.5, 4.5, 15, 9.03×1024
(3)0.25, 2.8, 0.5, 22g
13.第一组:2H2O == 2H2 + O2 , H2 + CuO == Cu + H2O
CaO + H2O = Ca(OH)2 , Ca(OH)2 + 2HCl = CaCl2 + 2H2O
第二组:Cu2(OH)2CO3 == 2CuO + H2O + CO2 ,CO + CuO == Cu + CO2
2Cu + O2 = 2CuO , CuO + H2SO4 = CuSO4 + H2O
14.88g/mol
15.12.3g , 0.1mol
苏教版第一单元 丰富多彩的化学物质教学设计: 这是一份苏教版第一单元 丰富多彩的化学物质教学设计,共6页。
高中化学人教版 (新课标)选修5 有机化学基础第一章 认识有机化合物第一节 有机化合物的分类教案: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第一章 认识有机化合物第一节 有机化合物的分类教案,共5页。
苏教版第一单元 丰富多彩的化学物质第1课时教案: 这是一份苏教版第一单元 丰富多彩的化学物质第1课时教案,共3页。