

2024-2025学年天津市滨海新区高二上学期期末考试化学试卷(学生版)
展开 这是一份2024-2025学年天津市滨海新区高二上学期期末考试化学试卷(学生版),共7页。试卷主要包含了单选题,填空题,解答题等内容,欢迎下载使用。
1.化学与生产、生活密切相关,下列说法错误的是
A.在锅炉的内壁焊上一定数量的锌片可延长锅炉的使用寿命
B.工业废水中的Cu2+、Hg2+等重金属离子可用Na2S作沉淀剂,转化为沉淀除去
C.乙炔与氧气反应放出的热量可用于切割金属
D.农业生产中,草木灰和铵态氮肥混合施用,可以增加氮肥肥效
2.常温时,下列溶液中cH+=1×10-2ml⋅L-1的是
A.pH=2的醋酸B.0.1ml⋅L-1H2SO4
C.pH=12的NaOH溶液D.0.01ml⋅L-1氨水
3.铜锌原电池装置(如图),该原电池在工作时,下列说法正确的是
(含KCl饱和溶液的琼胶)
A.Zn极流出电子,发生还原反应
B.Cu极电极反应式为Cu+2e-=Cu2+
C.盐桥中Cl-移向ZnSO4溶液
D.盐桥的作用是传导电子,形成闭合回路
4.下列事实不能用化学平衡移动原理解释的是
A.工业合成氨时,把氨气液化后及时从平衡混合物中分离出去
B.高锰酸钾(KMnO4)溶液加水稀释后颜色变浅
C.实验室收集氯气时,常用排饱和食盐水的方法
D.配制FeCl3溶液时,常先将FeCl3晶体溶于较浓的盐酸中
5.在基态多电子原子中,下列说法正确的是
A.3d、4d、5d能级的轨道数依次增多
B.p能级的能量一定比s能级的能量高
C.2px、2py、2pz轨道相互垂直,能量相等
D.电子云图中的小黑点表示绕核做高速圆周运动的电子
6.T℃时,恒容密闭容器中发生反应PCl3g+Cl2g⇌PCl5g ΔH1
③10mL1ml⋅L-1HNO2溶液与10mL1ml⋅L-1NaOH溶液恰好完全反应
④常温下,HNO2溶液中存在的微粒有:H+、NO2-、HNO2、OH-、H2O
A.①④B.①③C.②③D.②④
9.已知下列两个反应的热化学方程式:
①H2g+12O2g=H2Ol ΔH=-285.8kJ⋅ml-1
②CH4g+2O2g=CO2g+2H2Ol ΔH=-890.3kJ⋅ml-1
下列说法错误的是
A.1 ml H2O(l)与1 ml H2O(g)所具有的内能不同
B.热化学方程式②可表示甲烷的燃烧热
C.反应CO2g+4H2g=CH4g+2H2Ol的ΔH<0
D.1 ml H2(g)生成1 ml H2O(g)放出的热量大于285.8 kJ
10.下列用于解释事实的方程式书写错误的是
A.用明矾[KAlSO42⋅12H2O]作净水剂:Al3++3H2O⇌AlOH3胶体+3H+
B.Na2CO3溶液呈弱碱性:CO32-+2H2O⇌H2CO3+2OH-
C.向K2Cr2O7溶液中滴加少量浓H2SO4(忽略热量变化),溶液橙色加深:Cr2O72-橙色+H2O⇌2CrO42-黄色+2H+
D.为了除去锅炉水垢中的CaSO4,可先用Na2CO3溶液处理:CaSO4s+CO32-aq⇌SO42-aq+CaCO3s
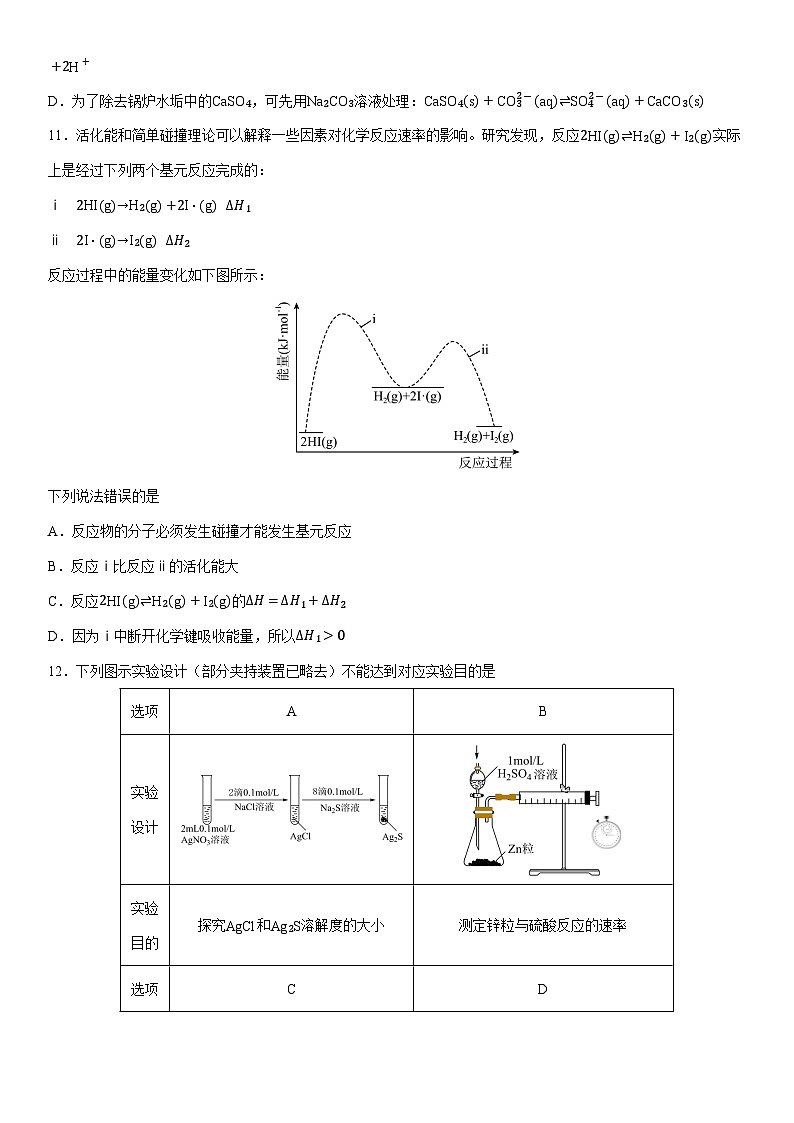
11.活化能和简单碰撞理论可以解释一些因素对化学反应速率的影响。研究发现,反应2HIg⇌H2g+I2g实际上是经过下列两个基元反应完成的:
ⅰ 2HIg→H2g+2I⋅g ΔH1
ⅱ 2I⋅g→I2g ΔH2
反应过程中的能量变化如下图所示:
下列说法错误的是
A.反应物的分子必须发生碰撞才能发生基元反应
B.反应ⅰ比反应ⅱ的活化能大
C.反应2HIg⇌H2g+I2g的ΔH=ΔH1+ΔH2
D.因为ⅰ中断开化学键吸收能量,所以ΔH1>0
12.下列图示实验设计(部分夹持装置已略去)不能达到对应实验目的是
二、填空题
13.下图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)上图中属于ds区的元素是 (填元素名称)。
(2)基态①原子中能量最高的电子,其电子云轮廓图的形状为 。
(3)基态②原子的核外电子有 种空间运动状态。
(4)②、③、④三种元素的原子半径由大到小的顺序为 (用元素符号表示)。
(5)③、④两种元素中第一电离能较大的元素是 (用元素符号表示)。根据“对角线规则”,与元素④性质相似的元素是 (用元素符号表示)。
(6)基态⑤原子的核外电子排布式为 。
(7)基态⑥原子中,其占据的最高能层的符号是 ,若基态⑥原子的电子发生电子跃迁形成激发态时, (填“吸收”或“释放”)能量。
(8)基态⑦原子的价层电子轨道表示式为 。
(9)元素①~⑧中,电负性最大的元素是 (用元素符号表示)。
(10)元素①~⑧中,某元素的原子逐级电离能如下图所示,该元素是 (用元素符号表示)。
三、解答题
14.降低大气中的CO2含量和有效开发利用CO2正成为研究的主要课题,CO2与氢气合成甲醇的反应为:CO2g+3H2g⇌CH3OHg+H2Og △H<0,请回答下列问题:
(1)该反应的自发条件是 (填“高温自发”“低温自发”或“任何温度下都自发”)。
(2)下列有利于提高CO2转化率的措施有______(填字母)。
A.缩小容器容积,增大压强 B.升温
C.使用催化剂 D.增大H2和CO2的初始投料比
(3)在容积为2 L的恒容密闭容器中,充入2 ml CO2和6 ml H2,在500 ℃时,发生上述反应,10 min后反应达到平衡,测得平衡时cCH3OH=0.75ml⋅L-1。
①达到平衡时CO2的转化率为 ,前10 min内用H2(g)的浓度变化来表示该反应的平均反应速率为v(H2)= ml⋅L-1⋅min-1。
②计算该温度下此反应的化学平衡常数K的值为 (保留两位小数)。
③保持温度不变,平衡后如果将容器的容积扩大到4 L,达到新平衡时,c(CH3OH) 0.375 ml/L(填“>”、“<”或“=”)。
(4)恒温恒容条件下,下列能说明反应CO2g+3H2g⇌CH3OHg+H2Og已达平衡的是______(填字母)。
A.3v正H2=v逆CH3OH
B.单位时间内生成1 ml H2O(g)的同时生成3 ml H2(g)
C.混合气体的密度不随时间而变化
D.容器中混合气体的压强不随时间而变化
(5)以CO2、H2为原料合成CH3OH时,还发生了副反应:CO2g+H2g⇌COg+H2Og
该反应的化学平衡常数(K)和温度(T)的关系如下表所示,请回答下列问题:
①该反应为 (填“吸热”或“放热”)反应。
②1000℃时,某时刻反应混合物中CO2、H2、CO、H2O的浓度分别为2 ml/L、2 ml/L、3 ml/L、3 ml/L,则此时上述副反应的平衡移动方向为 (“正反应方向”“逆反应方向”或“不移动”)。
四、填空题
15.如下图所示,其中甲池的总反应为2CH3OH+3O2+4KOH=2K2CO3+6H2O,请回答下列问题:
(1)甲池中负极的电极反应式为 。
(2)丙池中总反应的离子方程式为 。
(3)当乙池中B极质量增加4.32g时,甲池中理论上消耗O2的体积为 L(标准状况)。
(4)反应一段时间后,断开开关K,下列物质能使乙池恢复到反应前的浓度的是 (填字母)。
a.Ag b.AgOH c.Ag2O
(5)若丙池中电极不变,将其溶液换成滴有酚酞的NaCl溶液,开关闭合一段时间后,D极附近观察到的现象是 。
(6)若用丙池模拟铁制品表面镀铜,需要更换电极,则铁制品应放在 (填“C”或“D”)电极。
16.水溶液中的离子反应和平衡与生命活动、日常生活、工农业生产等息息相关,请根据水溶液中的离子反应与平衡知识及下表数据回答下列问题:
25℃时部分弱酸的电离平衡常数
(1)0.1ml⋅L-1NaCN溶液和0.1ml⋅L-1NaHCO3溶液中,cCN- cHCO3-(填“>”“”“
相关试卷
这是一份2024-2025学年天津市滨海新区高二上学期期末考试化学试卷(学生版),共7页。试卷主要包含了单选题,填空题,解答题等内容,欢迎下载使用。
这是一份天津市滨海新区2024-2025学年高二上学期化学期末试卷,共8页。
这是一份天津市滨海新区2024-2025学年高二上学期化学期末试卷,共8页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 









