


所属成套资源:2025-2026学年高二化学上学期寒假作业(Word版附解析)
2025-2026学年高二化学上学期寒假作业温故知新专题06沉淀溶解平衡(Word版附解析)
展开 这是一份2025-2026学年高二化学上学期寒假作业温故知新专题06沉淀溶解平衡(Word版附解析),文件包含专题06沉淀溶解平衡原卷版docx、专题06沉淀溶解平衡解析版docx等2份试卷配套教学资源,其中试卷共48页, 欢迎下载使用。
复习要点聚焦
1.难溶电解质的沉淀溶解平衡。
2.溶度积(Ksp)的含义,并能进行相关计算。
3.沉淀的生成、溶解与转化,并能应用化学平衡原理解释。
4.正确分析沉淀溶解平衡图像。
5.沉淀溶解平衡原理,分析图像中离子浓度的关系、Ksp的计算等。
知识网络聚焦
一、难溶电解质的沉淀溶解平衡
1、25 ℃时,溶解性与溶解度的关系
2、难溶电解质的沉淀溶解平衡
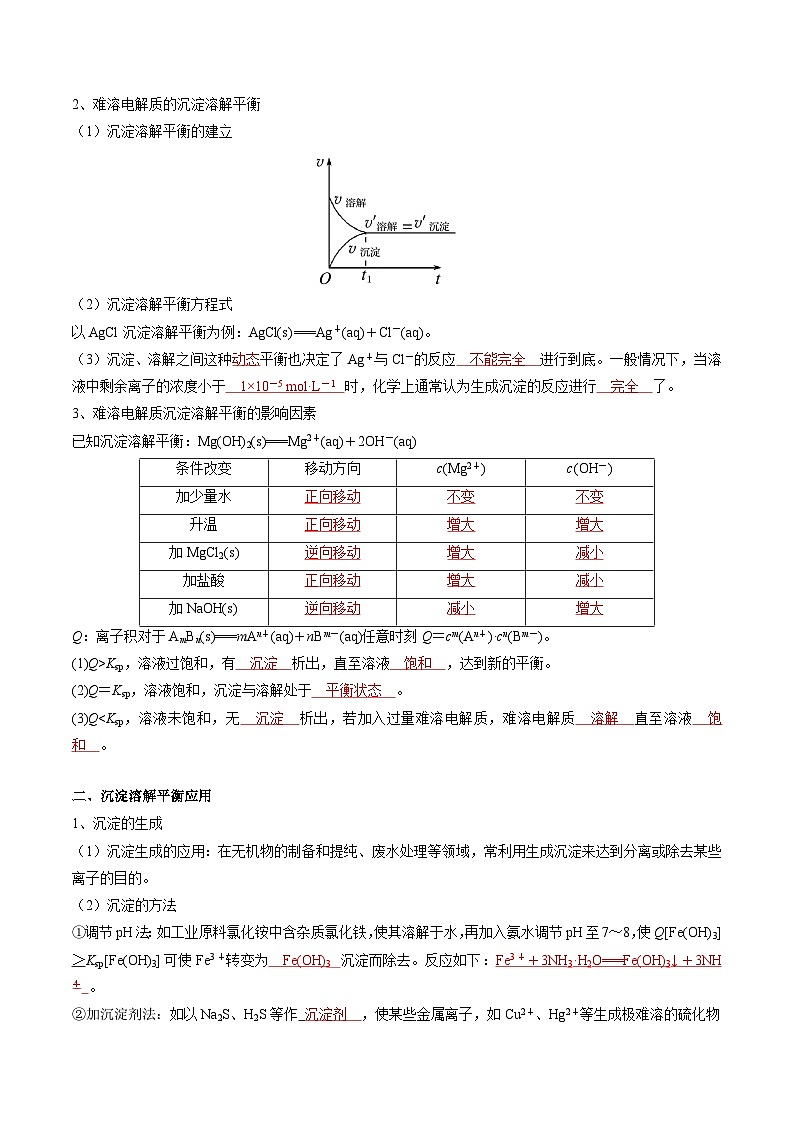
(1)沉淀溶解平衡的建立
(2)沉淀溶解平衡方程式
以AgCl沉淀溶解平衡为例:AgCl(s)===Ag+(aq)+Cl-(aq)。
(3)沉淀、溶解之间这种动态平衡也决定了Ag+与Cl-的反应 不能完全 进行到底。一般情况下,当溶液中剩余离子的浓度小于 1×10-5 ml·L-1 时,化学上通常认为生成沉淀的反应进行 完全 了。
3、难溶电解质沉淀溶解平衡的影响因素
已知沉淀溶解平衡:Mg(OH)2(s)===Mg2+(aq)+2OH-(aq)
Q:离子积对于AmBn(s)===mAn+(aq)+nBm-(aq)任意时刻Q=cm(An+)·cn(Bm-)。
(1)Q>Ksp,溶液过饱和,有 沉淀 析出,直至溶液 饱和 ,达到新的平衡。
(2)Q=Ksp,溶液饱和,沉淀与溶解处于 平衡状态 。
(3)Q105
【答案】D
【解析】A.由图可知,lgc(C2O)=-2.46时,-lgc(Ag+)=4,即c(C2O)=10-2.46ml/L,c(Ag+)=10-4 ml/L,则Ksp(Ag2C2O4)=c(C2O)×c2(Ag+)=10-2.46×(10-4 )2=10-10.46,所以Ksp(Ag2C2O4)的数量级等于10-11,故A错误;
B.由图可知,n点的c(Ag+)比AgCl溶解平衡曲线上对应点的c(Ag+)大,AgCl溶解平衡向形成AgCl的方向移动,即N点表示AgCl的过饱和溶液,故B错误;
C.由图可知,当阴离子浓度c(Cl-)=c(C2O)时,生成AgCl沉淀所需的c(Ag+)小,则向c(Cl-)=c(C2O)的混合液中滴入AgNO3溶液时,先析出AgCl沉淀,故C错误;
D.D.由图可知,lgc(Cl-)=5.75时,-lgc(Ag+)=4,即c(Ag+)=10-4 ml/L,c(Cl-)=10-5.75ml/L,Ksp(AgCl)=c(Ag+)×c(Cl-)=10-9.75,Ag2C2O4(s)+2Cl-(aq)2AgCl(s)+C2O (aq) 的平衡常数K=====109.04 >105,故D正确。
答案选D。
题型三 研究与实践了解水处理过程中的化学原理
典例7
7.(2023·全国·高二假期作业)是一种一元弱酸,与等浓度等体积的NaOH完全反应后生成,下列叙述正确的是
A.的溶液是酸式盐
B.溶液中存在电离平衡:
C.0.01 ml/L 水溶液加水稀,pH增大
D.溶液与NaOH溶液反应的离子方程式为
【答案】C
【解析】A.是一种一元弱酸,是正盐,A错误;
B.H3PO2是一种一元弱酸,所以只能发生,不存在第二次电离,B错误;
C.0.01ml/LH3PO2水溶液加水稀释,氢离子浓度减小,pH值增大,C正确;
D.溶液与NaOH溶液反应的离子方程式为,D错误;
故选C。
典例8
8.(2022上·湖北十堰·高二校联考期中)下列说法正确的是
A.常温下,0.1ml/LHA溶液和0.1ml/LNaOH溶液等体积混合后溶液的pH>7,则混合溶液中离子浓度的大小顺序为:c(A-)>c(Na+)>c(OH-)>c(H+)
B.常温下,0.1ml/L的下列溶液①NH4Al(SO4)2,②NH4Cl,③NH3•H2O,④CH3COONH4中,c(NH)由大到小的顺序是②>①>④>③
C.常温下,pH均为2的CH3COOH溶液和H2SO4溶液、pH均为12的氨水和NaOH溶液,四种溶液中由水电离的c(OH-)相等
D.常温下0.1ml/LpH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
【答案】C
【解析】A.两溶液中溶质物质的量相同,混合后完全反应,溶质为NaA,混合后溶液的pH>7,说明A- 在溶液中存在水解,根据NaA化学式以及A- 发生水解可知,c(Na+)>c(A-),溶液呈碱性,因此c(OH-)>c(H+),因A- 水解微弱,因此溶液中c(OH-)较小,故溶液中c(Na+)>c(A-) >c(OH-)>c(H+),A错误;
B.①NH4Al(SO4)2溶液中水解受到Al3+水解的抑制,②NH4Cl溶液中正常水解,④CH3COONH4溶液中水解受到CH3COO-水解促进,③NH3·H2O溶液中NH3·H2O电离程度低,浓度较低,因此相同浓度4种溶液中浓度由大到小的顺序是:①>②>④>③,B错误;
C.CH3COOH溶液、硫酸溶液、氨水、NaOH溶液中水的电离均受到抑制,pH=2酸溶液中OH- 均来自水的电离,酸溶液中c(H+)=10-2ml/L,根据KW= c(OH-)• c(H+)=10-14可知,水电离出c(OH-)=10-12ml/L= c(H+)水,同理可知,pH均为12的碱溶液中c(H+)= c(H+)水=10-12ml/L,C正确;
D.NaHB溶液呈酸性,说明HB- 电离程度大于水解程度,因此c(HB-)> c(B2-)> c(H2B),D错误;
故选C。
强化一 溶度积常数的计算技巧
强化二 常见三类沉淀溶解平衡图像
(1)两坐标为离子浓度的曲线型图像
已知:pCu=-lg c(Cu+),pX=-lg c(X-),式中X-表示卤素阴离子。298 K时,Ksp(CuCl)≈1.0×10-7,Ksp(CuBr)≈1.0×10-9,Ksp(CuI)≈1.0×10-12。298 K时 ,CuCl、CuBr、CuI的饱和溶液中pCu和pX的关系如图所示分析。
(3)沉淀滴定图像
强化三 沉淀溶解平衡曲线分析方法
[以BaSO4(s)Ba2+(aq)+SOeq \\al(2-,4)(aq)为例]。
真题感知
1.(2023·河北·统考高考真题)某温度下,两种难溶盐的饱和溶液中或与的关系如图所示。下列说法错误的是
A.
B.若混合溶液中各离子浓度如J点所示,加入,则平衡时变小
C.向固体中加入溶液,可发生的转化
D.若混合溶液中各离子起始浓度如T点所示,待平衡时
【答案】D
【分析】对于沉淀,存在沉淀溶解平衡,则,在图像上任找两点(0,16),(3,7),转化成相应的离子浓度代入,由于温度不变,所以计算出的不变,可求得x=3,;对于沉淀,存在沉淀溶解平衡,,按照同样的方法,在图像上任找两点(0,10),(3,7),可求得y=1,。
【解析】A.根据分析可知,x=3,y=1,,A项正确;
B.由图像可知,若混合溶液中各离子浓度如J点所示,此时,加入,增大,减小,则,,变小,B项正确;
C.向固体中加入溶液,当达到了的溶度积常数,可发生→的转化,C项正确;
D.若混合溶液中各离子起始浓度如T点所示,由于沉淀达到沉淀溶解平衡,所以不发生变化,而要发生沉淀,和的物质的量按1:y减少,所以达到平衡时,D项错误;
故选D。
2.(2023·江苏·统考高考真题)室温下,用含少量的溶液制备的过程如题图所示。已知,。下列说法正确的是
A.溶液中:
B.“除镁”得到的上层清液中:
C.溶液中:
D.“沉锰”后的滤液中:
【答案】C
【解析】A.溶液中存在电荷守恒:,A错误;
B.“除镁”得到的上层清液中为的饱和溶液,有,故,B错误;
C.溶液中存在质子守恒:,故,C正确;
D.“沉锰”后的滤液中还存在F-、等离子,故电荷守恒中应增加其他离子使等式成立,D错误。
故选C。
【点睛】
3.(2023·北京·统考高考真题)利用平衡移动原理,分析一定温度下在不同的体系中的可能产物。
已知:i.图1中曲线表示体系中各含碳粒子的物质的量分数与的关系。
ii.2中曲线Ⅰ的离子浓度关系符合;曲线Ⅱ的离子浓度关系符合[注:起始,不同下由图1得到]。
下列说法不正确的是
A.由图1,
B.由图2,初始状态,无沉淀生成
C.由图2,初始状态,平衡后溶液中存在
D.由图1和图2,初始状态、,发生反应:
【答案】C
【解析】A.水溶液中的离子平衡 从图1可以看出时,碳酸氢根离子与碳酸根离子浓度相同,A项正确;
B.从图2可以看出、时,该点位于曲线Ⅰ和曲线Ⅱ的下方,不会产生碳酸镁沉淀或氢氧化镁沉淀,B项正确;
C.从图2可以看出、时,该点位于曲线Ⅱ的上方,会生成碳酸镁沉淀,根据物料守恒,溶液中,C项错误;
D.时,溶液中主要含碳微粒是,,时,该点位于曲线Ⅱ的上方,会生成碳酸镁沉淀,因此反应的离子方程式为,D项正确;
故选C。
4.(2023·浙江·统考高考真题)草酸()是二元弱酸。某小组做如下两组实验:
实验I:往溶液中滴加溶液。
实验Ⅱ:往溶液中滴加溶液。
[已知:的电离常数,溶液混合后体积变化忽略不计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中时,溶液中
【答案】D
【解析】A.溶液被氢氧化钠溶液滴定到终点时生成显碱性的草酸钠溶液,为了减小实验误差要选用变色范围在碱性范围的指示剂,因此,实验I可选用酚酞作指示剂,指示反应终点,故A错误;
B.实验I中时,溶质是、且两者物质的量浓度相等,,,则草酸氢根的电离程度大于草酸根的水解程度,因此存在,故B错误;
C.实验Ⅱ中,由于开始滴加的氯化钙量较少而过量,因此该反应在初始阶段发生的是,该反应的平衡常数为,因为平衡常数很大,说明反应能够完全进行,当完全消耗后,再和发生反应,故C错误;
D.实验Ⅱ中时,溶液中的钙离子浓度为,溶液中,故D正确。
综上所述,答案为D。
5.(2023·湖南·统考高考真题)处理某铜冶金污水(含)的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的如下表所示:
②。
下列说法错误的是
A.“沉渣Ⅰ”中含有和
B.溶液呈碱性,其主要原因是
C.“沉淀池Ⅱ”中,当和完全沉淀时,溶液中
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
【答案】D
【分析】污水中含有铜离子、三价铁离子、锌离子、铝离子,首先加入石灰乳除掉三价铁离子和铝离子,过滤后,加入硫化钠除去其中的铜离子和锌离子,再次过滤后即可达到除去其中的杂质,以此解题。
【解析】A.根据分析可知氢氧化铁当pH=1.9时开始沉淀,氢氧化铝当pH=3.5时开始沉淀,当pH=4时,则会生成氢氧化铝和氢氧化铁,即“沉渣I”中含有Fe(OH)3和Al(OH)3,A正确;
B.硫化钠溶液中的硫离子可以水解,产生氢氧根离子,使溶液显碱性,其第一步水解的方程式为:S2-+H2O⇌HS-+OH-,B正确;
C.当铜离子和锌离子完全沉淀时,则硫化铜和硫化锌都达到了沉淀溶解平衡,则,C正确;
D.污水经过处理后其中含有较多的钙离子以及没有除净的铝离子,故“出水”应该经过阳离子交换树脂软化处理,达到工业冷却循环用水的标准后,才能使用,D错误;
故选D。
6.(2023·辽宁·统考高考真题)某废水处理过程中始终保持H2S饱和,即,通过调节pH使和形成硫化物而分离,体系中与关系如下图所示,c为和的浓度,单位为。已知,下列说法正确的是
A.B.③为与的关系曲线
C.D.
【答案】D
【分析】已知H2S饱和溶液中随着pH的增大,H2S的浓度逐渐减小,HS-的浓度增大,S2-浓度逐渐增大,则有-lgc(HS-)和-lg(S2-)随着pH增大而减小,且相同pH相同时,HS-浓度大于S2-,即-lgc(HS-)小于-lg(S2-),则Ni2+和Cd2+浓度逐渐减小,且,即当c(S2-)相同时,c(Ni2+)>c(Cd2+),则-lgc(Ni2+)和-lg(Cd2+)随着pH增大而增大,且有-lgc(Ni2+)小于-lg(Cd2+),由此可知曲线①代表Cd2+、②代表Ni2+、③代表S2-,④代表HS-,据此分析结合图像各点数据进行解题。
【解析】A.由分析可知,曲线①代表Cd2+、③代表S2-,由图示曲线①③交点可知,此时c(Cd2+)=c(S2-)=10-13ml/L,则有,A错误;
B.由分析可知,③为与的关系曲线,B错误;
C.由分析可知,曲线④代表HS-,由图示曲线④两点坐标可知,此时c(H+)=10-1.6ml/L时,c(HS-)=10-6.5ml/L,或者当c(H+)=10-4.2ml/L时,c(HS-)=10-3.9ml/L,,C错误;
D.已知Ka1Ka2==,由曲线③两点坐标可知,当c(H+)=10-4.9ml/L时,c(S2-)=10-13ml/L,或者当c(H+)=10-6.8ml/L时,c(S2-)=10-9.2ml/L,故有Ka1Ka2===10-21.8,结合C项分析可知Ka1=10-7.1,故有,D正确;
故答案为D。
7.(2023·全国·统考高考真题)一定温度下,AgCl和Ag2CrO4的沉淀溶解平衡曲线如图所示。
下列说法正确的是
A.a点条件下能生成Ag2CrO4沉淀,也能生成AgCl沉淀
B.b点时,c(Cl-)=c(CrO),Ksp(AgCl)=Ksp(Ag2CrO4)
C.Ag2CrO4+2Cl-2AgCl+CrO的平衡常数K=107.9
D.向NaCl、Na2CrO4均为0.1ml·L-1的混合溶液中滴加AgNO3溶液,先产生Ag2CrO4沉淀
【答案】C
【分析】根据图像,由(1.7,5)可得到Ag2CrO4的溶度积Ksp(Ag2CrO4)=c2(Ag+)·c(CrO)=(1×10-5)2×1×10-1.7=10-11.7,由(4.8,5)可得到AgCl的溶度积Ksp(AgCl)=c(Ag+)·c(Cl)=1×10-5×1×10-4.8=10-9.8,据此数据计算各选项结果。
【解析】A.假设a点坐标为(4,6.5),此时分别计算反应的浓度熵Q得,Q(AgCl)=10-10.5,Q(Ag2CrO4)=10-17,二者的浓度熵均小于其对应的溶度积Ksp,二者不会生成沉淀,A错误;
B.Ksp为难溶物的溶度积,是一种平衡常数,平衡常数只与温度有关,与浓度无关,根据分析可知,二者的溶度积不相同,B错误;
C.该反应的平衡常数表达式为K=,将表达式转化为与两种难溶物的溶度积有关的式子得K=====1×107.9,C正确;
D.向NaCl、Na2CrO4均为0.1ml·L-1的混合溶液中滴加AgNO3,开始沉淀时所需要的c(Ag+)分别为10-8.8和10-5.35,说明此时沉淀Cl-需要的银离子浓度更低,在这种情况下,先沉淀的是AgCl,D错误;
故答案选C。
8.(2023·山东·统考高考真题)盐湖卤水(主要含、和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备的工艺流程如下:
已知:常温下,。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的在水中存在平衡:(常温下,);与溶液反应可制备硼砂。常温下,在硼砂溶液中,水解生成等物质的量浓度的和,该水解反应的离子方程式为 ,该溶液 。
(2)滤渣Ⅰ的主要成分是 (填化学式);精制Ⅰ后溶液中的浓度为,则常温下精制Ⅱ过程中浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收外,还将增加 的用量(填化学式)。
(3)精制Ⅱ的目的是 ;进行操作时应选择的试剂是 ,若不进行该操作而直接浓缩,将导致 。
【答案】(1)
(2) 、Mg(OH)2 CaO
(3) 加入纯碱将精制Ⅰ所得滤液中的转化为(或除去精制Ⅰ所得滤液中的),提高纯度 盐酸 浓缩液中因浓度过大使得过早沉淀,即浓缩结晶得到的中会混有,最终所得的产率减小
【分析】由流程可知,卤水中加入盐酸脱硼后过滤,所得滤液经浓缩结晶后得到晶体,该晶体中含有Na+、Li+、Cl-、等,焙烧后生成HCl气体;烧渣水浸后过滤,滤液中加生石灰后产生沉淀,滤渣Ⅰ的主要成分为Mg(OH)2、;精制Ⅰ所得滤液中再加纯碱又生成沉淀,则滤渣Ⅱ为、Mg(OH)2;精制Ⅱ所得滤液经操作X后,所得溶液经浓缩结晶、过滤得到氯化钠,浓缩后的滤液中加入饱和碳酸钠溶液沉锂,得到。
【解析】(1)含硼固体中的在水中存在平衡:(常温下,);与溶液反应可制备硼砂。常温下.在硼砂溶液中,水解生成等物质的量浓度的和,该水解反应的离子方程式为,由B元素守恒可知,和的浓度均为,,则该溶液。
(2)由分析可知,滤渣I的主要成分是、Mg(OH)2;精制I后溶液中的浓度为2.0,由可知,则常温下精制Ⅱ过程中浓度应控制在以下。若脱硼后直接进行精制Ⅰ,若不回收HCl,整个溶液将呈强酸性,因此为达到除Mg2+离子所需的碱性pH首先需要额外多消耗CaO,同时多引入的Ca2+离子需要更多的纯碱除去,因此,还将增加生石灰(CaO)和纯碱()的用量。
(3)精制Ⅰ中,烧渣水浸后的滤液中加生石灰后产生的滤渣Ⅰ的主要成分为;由于微溶于水,精制Ⅰ所得滤液中还含有一定浓度的,还需要除去,因此,精制Ⅱ的目的是:加入纯碱将精制Ⅰ所得滤液中的转化为(或除去精制Ⅰ所得滤液中的),提高纯度。操作X是为了除去剩余的碳酸根离子,为了防止引入杂质离子,应选择的试剂是盐酸;加入盐酸的目的是除去剩余的碳酸根离子,若不进行该操作而直接浓缩,将导致浓缩液中因浓度过大使得过早沉淀,即浓缩结晶得到的中会混有,最终所得的产率减小。
9.(2023·湖北·统考高考真题)是生产多晶硅的副产物。利用对废弃的锂电池正极材料进行氯化处理以回收Li、C等金属,工艺路线如下:
回答下列问题:
(1)C位于元素周期表第 周期,第 族。
(2)烧渣是LiCl、和的混合物,“500℃焙烧”后剩余的应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因 。
(3)鉴别洗净的“滤饼3”和固体常用方法的名称是 。
(4)已知,若“沉钴过滤”的pH控制为10.0,则溶液中浓度为 。“850℃煅烧”时的化学方程式为 。
(5)导致比易水解的因素有 (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
【答案】(1) 4 Ⅷ
(2)
(3)焰色反应
(4)
(5)abd
【分析】由流程和题中信息可知,粗品与在500℃焙烧时生成氧气和烧渣,烧渣是LiCl、和的混合物;烧渣经水浸、过滤后得滤液1和滤饼1,滤饼1的主要成分是和;滤液1用氢氧化钠溶液沉钴,过滤后得滤饼2(主要成分为)和滤液2(主要溶质为LiCl);滤饼2置于空气中在850℃煅烧得到;滤液2经碳酸钠溶液沉锂,得到滤液3和滤饼3,滤饼3为。
【解析】(1)C是27号元素,其原子有4个电子层,其价电子排布为,元素周期表第8、9、10三个纵行合称第Ⅷ族,因此,其位于元素周期表第4周期、第Ⅷ族。
(2)“500℃焙烧”后剩余的应先除去,否则水浸时会产生大量烟雾,由此可知,四氯化硅与可水反应且能生成氯化氢和硅酸,故其原因是:遇水剧烈水解,生成硅酸和氯化氢,该反应的化学方程式为。
(3)洗净的“滤饼3”的主要成分为,常用焰色反应鉴别和,的焰色反应为紫红色,而的焰色反应为黄色。故鉴别“滤饼3”和固体常用方法的名称是焰色反应。
(4)已知,若“沉钴过滤”的pH控制为10.0,则溶液中,浓度为。“850℃煅烧”时,与反应生成和,该反应的化学方程式为。
(5)a.Si-Cl键极性更大,则 Si-Cl键更易断裂,因此,比易水解,a有关;
b.Si的原子半径更大,因此,中的共用电子对更加偏向于,从而导致Si-Cl键极性更大,且Si原子更易受到水电离的的进攻,因此,比易水解,b有关;
c.通常键能越大化学键越稳定且不易断裂,因此,Si-Cl键键能更大不能说明Si-Cl更易断裂,故不能说明比易水解,c无关;
d.Si有更多的价层轨道,因此更易与水电离的形成化学键,从而导致比易水解,d有关;
综上所述,导致比易水解的因素有abd。
提升专练
1.(2023上·四川广安·高二广安二中校考阶段练习)下列实验方案不能达到实验目的的是
【答案】B
【解析】A.向1mL0.1ml/LMgCl2溶液中滴加1~2滴0.1ml/LNaOH溶液,产生白色Mg(OH)2沉淀、且MgCl2过量,再滴加2滴0.1ml/LFeCl3溶液,若白色沉淀转化为红褐色沉淀,说明Mg(OH)2沉淀转化成更难溶于水的Fe(OH)3沉淀,则Ksp[Mg(OH)2]>Ksp[Fe(OH)3],A项能达到实验目的;
B.NaClO属于强碱弱酸盐,其水溶液呈碱性,但NaClO水解生成的HClO具有漂白性,能使pH试纸最终褪色,不能用pH试纸测NaClO溶液的pH,B项不能达到实验目的;
C.FeCl3溶液中存在水解平衡:FeCl3+3H2OFe(OH)3+3HCl,若直接加热蒸干FeCl3溶液,由于HCl的挥发,水解平衡正向移动,最终FeCl3完全水解,不能获得无水FeCl3,在HCl气流中加热蒸干,由于HCl抑制了FeCl3水解,最终能制备无水FeCl3晶体,C项能达到实验目的;
D.1mL0.1ml·L-1 FeCl3溶液和2mL0.1ml·L-1KI溶液充分反应,氯化铁少量,观察到滴加几滴KSCN溶液后变成红色,即含有Fe3+,则可证明FeCl3与KI的反应是可逆反应,D项能达到实验目的;
答案选B。
2.(2023上·广西柳州·高二柳铁一中校考期中)下列有关实验操作、现象和解释或结论都正确的是
【答案】B
【解析】A.与发生离子反应,加入固体,对该离子反应无影响,平衡不移动,溶液颜色不变,现象及解释都错误,A错误;
B.常温下,向等体积、等浓度的和溶液中分别滴加2滴酚酞,两份溶液变红,说明两份溶液都显碱性,、发生水解,溶液红色更深,则水解程度大,水解平衡常数大, 即,B正确;
C.向重铬酸钾溶液中加水,溶液体积增大,溶液中离子、浓度都减小,溶液颜色变浅,不能用存在平衡向右移动解释,溶液颜色变浅也不能说明该平衡向右移动,C错误;
D.向溶液中加入过量的溶液,发生反应,有浅黄色沉淀生成,有剩余,再加入溶液,发生反应,有黄色沉淀生成,不能证明更难溶于水,不能得出结论,D错误;
答案选B。
3.(2023上·北京西城·高二北师大实验中学校考期中)为研究沉淀的生成及转化,进行如下实验。
已知:Ksp(AgSCN)=1.0x10-12
下列关于该实验的分析不正确的是
A.①中产生白色沉淀的原因是
B.充分反应后①中浓度为
C.③中产生黄色沉淀可证明向沉淀转化
D.②中加入KI溶液后一定发生了反应
【答案】D
【解析】A.向硝酸银溶液中滴加硫氰化钾,银离子浓度与硫氰根离子浓度幂之积大于硫氰化银的溶度积,生成白色沉淀,A正确;
B.生成沉淀后溶液中剩余的银离子的浓度为,则溶液中浓度为,B正确;
C.向悬浊液中滴加硝酸铁,溶液未变红,加入以后,碘离子与中的银离子发生反应生成更难溶的,实现了向的转化,C正确;
D.硝酸根离子在酸辛条件下具有强氧化性,而KI具有强还原性,所以加入KI以后,也可能是硝酸根离子将碘离子氧化为碘单质,也会出现上述现象,D错误;
故选D。
4.(2022上·上海·高二复旦附中校考期末)下列实验中均使用了食盐水,针对实验目的,实验设计不严谨的是
【答案】A
【解析】A.向硝酸银溶液中滴加少量氯化钠溶液,生成氯化银白色沉淀,银离子过量,再加入少量碘化钾溶液,生成黄色的碘化银沉淀,不能说明碘化银是氯化银转化生成的,故A不合理;
B.CH4难溶于水、Cl2难溶于饱和食盐水,在光照下发生取代反应生成HCl溶于水,水沿着导管上升可验证,B合理;
C.向饱和氯化钠溶液中滴入浓盐酸,即增大了溶液中Cl-的浓度,使得氯化钠的溶解平衡逆向移动,故析出NaCl晶体,C合理;
D.通过饱和食盐水和控制分液漏斗的活塞来控制滴入溶液的速率,从而是产生的乙炔气流不快不慢,得到比较平稳的气流,D合理;
故选A。
5.(2023上·辽宁沈阳·高二沈阳二中校考阶段练习)已知常温下,,现有等体积的AgCl和AgI的饱和溶液的清液。下列说法错误的是
A.若向AgI清液加入固体,则溶液中增大,不变
B.若将等体积的两饱和清液混合,向其中加入溶液,当AgCl开始沉淀时,溶液中
C.若向溶液中滴加2滴溶液,产生白色沉淀;再向其中滴加4滴的KI溶液,有黄色沉淀产生,则可验证
D.若将等体积的两饱和清液混合,再加入足量固体,则AgCl和AgI都可沉淀,以AgI为主
【答案】D
【解析】A.Ksp与温度有关,温度不变,Ksp不变,因而向AgI的饱和溶液中加AgNO3,增大,不变,故A正确;
B.AgI的溶度积小于AgCl,加入溶液,AgI优先沉淀,当AgCl开始沉淀时,溶液中,故B正确;
C.Ag+少量、Cl-过量,先生成白色沉淀AgCl,后氯化银沉淀由白色转化为黄色的AgI沉淀,说明,故C正确;
D.饱和的AgCl溶液中:c(Ag+)=c(Cl-)==1.0×10-5,饱和的AgI溶液中:c(Ag+)=c(I-)==×10-9,由于c(Cl-)远大于c(I-),若AgNO3固体足量,沉淀以AgCl为主,故D错误;
故选D。
6.(2023上·湖北·高二荆州中学校联考期中)关于化学在生活中的应用,下列说法错误的是
A.热的纯碱溶液去油污,效果更好
B.BaCO3不溶于水,可用作医疗上检查肠胃的钡餐
C.常温下,NH4F溶液不能保存在玻璃试剂瓶中
D.使用含氟牙膏,可以使牙齿表面的羟基磷灰石转化成更坚固的氟磷灰石
【答案】B
【解析】A.纯碱水解显碱性,加热可以促进水解,去污效果更好,A正确;
B.BaCO3能溶于胃酸,引起重金属离子中毒,用作钡餐的是BaSO4,B错误;
C.常温下,NH4F溶液水解生成氢氟酸,可以与二氧化硅反应生成SiF4和水,所以NH4F溶液不能保存在玻璃试剂瓶中,C正确;
D.使用含氟牙膏,可以将羟基磷灰石转化成更坚固的氟磷灰石,D正确;
故选B。
7.(2023上·四川泸州·高二校考期中)已知,,。某溶液中含有、和,浓度均为0.010,向该溶液中逐滴加入0.010的溶液时,三种阴离子产生沉淀的先后顺序为
A.B.
C.D.
【答案】A
【解析】根据AgCl、AgBr、Ag2CrO4的Ksp,当Cl−开始沉淀时,c(Ag+)=ml·L−1=1.56×10−8 ml·L−1;当Br−开始沉淀时,c(Ag+)=ml·L−1=7.7×10−11 ml·L−1;当开始沉淀时,c(Ag+)=ml·L−1 =3×10−5 ml·L−1。沉淀三种阴离子时,所需c(Ag+)越小,产生沉淀越早,由计算结果可得出三种阴离子产生沉淀的先后顺序为,故选A。
8.(2023上·陕西榆林·高二榆林市第一中学校联考阶段练习)盐的水解及沉淀的溶解平衡是中学化学研究的重点之一。回答下列问题:
(1)已知常温下甲酸的电离常数。
①写出甲酸钠水解反应的离子方程式: ,若溶液中加入下列物质,促进水解的是 (填标号)。
A. B.NaOH C.NaCl D.
②常温下,向20 mL 0.1HCOOH溶液中加入0.1的NaOH溶液,溶液的pH变化曲线如图所示。d点溶液中 (保留两位有效数字);b点溶液中: (填“>”“
相关试卷
这是一份2025-2026学年高二化学上学期寒假作业温故知新专题06沉淀溶解平衡(Word版附解析),文件包含专题06沉淀溶解平衡原卷版docx、专题06沉淀溶解平衡解析版docx等2份试卷配套教学资源,其中试卷共48页, 欢迎下载使用。
这是一份2025-2026学年高二化学上学期寒假作业温故知新专题03化学平衡(Word版附解析),文件包含专题03化学平衡原卷版docx、专题03化学平衡解析版docx等2份试卷配套教学资源,其中试卷共38页, 欢迎下载使用。
这是一份(复习课)2024年人教版高二化学寒假提升学与练 专题06 沉淀溶解平衡(2份打包,原卷版+解析版),文件包含复习课2024年人教版高二化学寒假提升学与练专题06沉淀溶解平衡原卷版doc、复习课2024年人教版高二化学寒假提升学与练专题06沉淀溶解平衡解析版doc等2份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




