
2025-2026学年湖北省孝感市九年级(上)期末化学试卷(含答案)
展开 这是一份2025-2026学年湖北省孝感市九年级(上)期末化学试卷(含答案),共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
1.中华文化博大精深,下列成语或典故的本意主要涉及化学变化的是( )
A. 蜡炬成灰B. 风吹草动C. 滴水成冰D. 沙里淘金
2.2025年世界环境日中国主题是“美丽中国我先行”。下列做法不符合这一主题的是( )
A. 节约用水B. 使用节能家电C. 使用一次性餐具D. 垃圾分类处理
3.学习小组在劳动实践中用木材生火做饭,下列说法错误的是( )
A. 引燃木材——升高木材着火点B. 冒出黑烟——木材燃烧不充分
C. 架空木材——增大与空气接触面积D. 沙土盖灭——使木材与空气隔绝
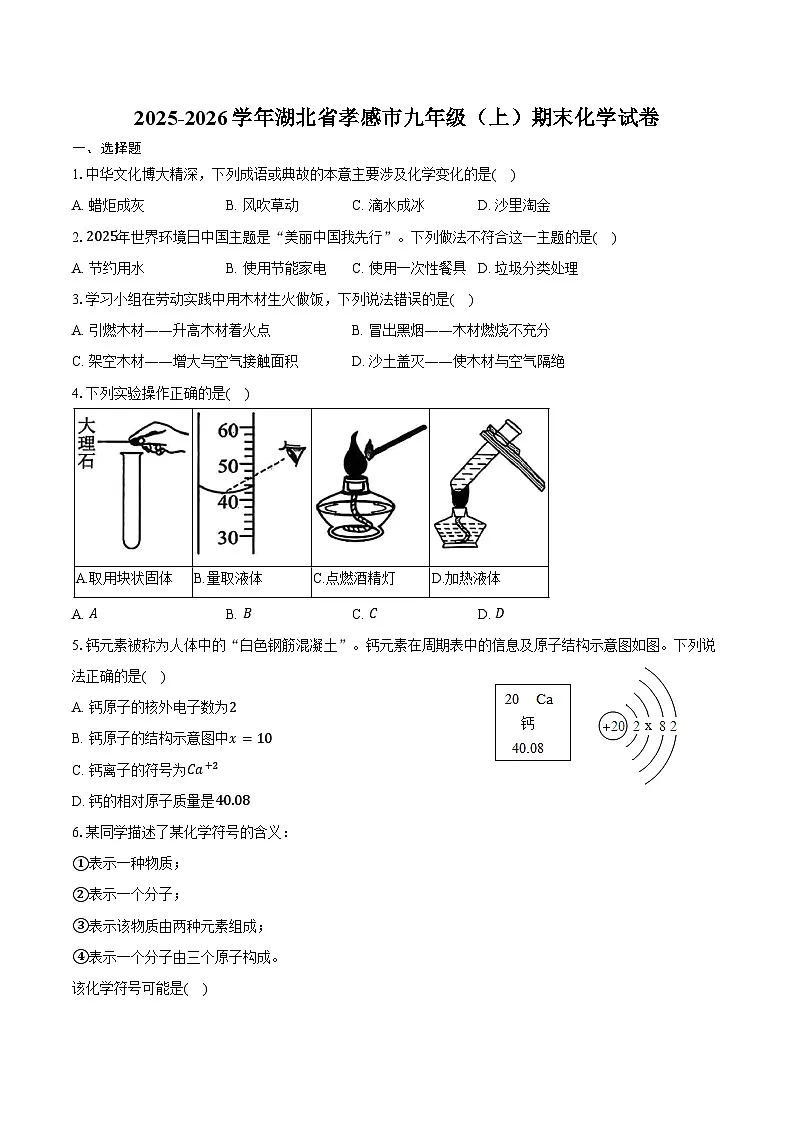
4.下列实验操作正确的是( )
A. AB. BC. CD. D
5.钙元素被称为人体中的“白色钢筋混凝土”。钙元素在周期表中的信息及原子结构示意图如图。下列说法正确的是( )
A. 钙原子的核外电子数为2
B. 钙原子的结构示意图中x=10
C. 钙离子的符号为Ca+2
D. 钙的相对原子质量是40.08
6.某同学描述了某化学符号的含义:
①表示一种物质;
②表示一个分子;
③表示该物质由两种元素组成;
④表示一个分子由三个原子构成。
该化学符号可能是( )
A. HeB. O3C. NaClD. CO2
7.分类是学习化学的常用方法。下列物质分类正确的是( )
A. 混合物:液态氧、海水B. 单质:氢气、汞
C. 氧化物:五氧化二磷、高锰酸钾D. 化合物:C60、白酒
8.物质的性质决定物质的用途,下列性质与用途不匹配的是( )
A. 稀有气体化学性质不活泼,可用作保护气B. CO具有可燃性,可用于冶炼金属
C. 干冰升华吸热,可用作制冷剂D. 石墨具有导电性,可用作电池电极
9.核桃中含有的亚麻酸(化学式为C18H30O2)具有降低血脂、软化血管、调节血压等功效。下列有关亚麻酸的说法正确的是( )
A. 亚麻酸属于氧化物B. 亚麻酸由碳原子、氢原子、氧原子构成
C. 亚麻酸中碳元素的质量分数最大D. 亚麻酸中氢、氧元素的质量比为15:1
10.如图为治理汽车尾气反应的微观示意图。下列有关说法正确的是 ( )
A. 图中只有两种氧化物B. 该反应中,氮元素的化合价升高了
C. 相对分子质量最大的是NOD. 生成丙和丁的质量比为7:22
11.已知白磷的着火点是40℃,红磷的着火点是240℃。如图所示为探究燃烧条件的实验装置,下列有关说法正确的是( )
A. 铜片上的白磷燃烧,产生大量白雾
B. 向80℃热水中的白磷通入氧气,白磷不能燃烧
C. 热水起提供热量和隔绝空气的作用
D. 该实验说明可燃物温度达到着火点即可燃烧
12.宏观辨识与微观分析是化学学科核心素养,下列对宏观事实解释正确的是( )
A. 金块制成金箔面积增大,是因为金原子数目增多
B. 水结成冰后不再流动是因为分子停止了运动
C. 水银温度计测量体温,是因为汞原子随温度升高而增大
D. 金刚石、石墨和C60物理性质差异大,是因为碳原子排列方式不同
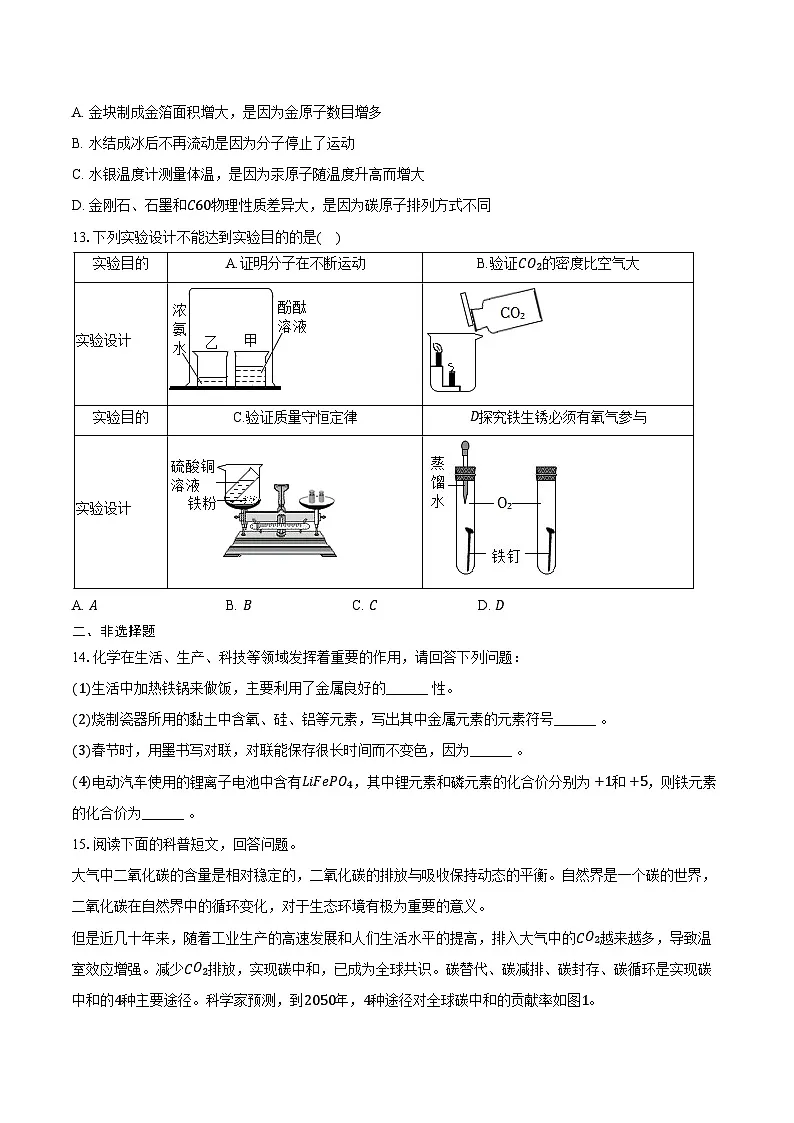
13.下列实验设计不能达到实验目的的是( )
A. AB. BC. CD. D
二、非选择题
14.化学在生活、生产、科技等领域发挥着重要的作用,请回答下列问题:
(1)生活中加热铁锅来做饭,主要利用了金属良好的______ 性。
(2)烧制瓷器所用的黏土中含氧、硅、铝等元素,写出其中金属元素的元素符号______ 。
(3)春节时,用墨书写对联,对联能保存很长时间而不变色,因为______ 。
(4)电动汽车使用的锂离子电池中含有LiFePO4,其中锂元素和磷元素的化合价分别为+1和+5,则铁元素的化合价为______ 。
15.阅读下面的科普短文,回答问题。
大气中二氧化碳的含量是相对稳定的,二氧化碳的排放与吸收保持动态的平衡。自然界是一个碳的世界,二氧化碳在自然界中的循环变化,对于生态环境有极为重要的意义。
但是近几十年来,随着工业生产的高速发展和人们生活水平的提高,排入大气中的CO2越来越多,导致温室效应增强。减少CO2排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的4种主要途径。科学家预测,到2050年,4种途径对全球碳中和的贡献率如图1。
CO2的吸收是碳封存的首要环节,在研究膜吸收法吸收CO2时,研究人员通过实验比较了一乙醇胺、二乙醇胺、氨基乙酸钾3种吸收剂对烟气中CO2的脱除效果,其结果如图2。我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。实现碳中和,人人有责,让我们从衣食住行点滴做起,低碳生活。
(1)自然界中吸收二氧化碳的主要途径是______ 。
(2)由图1可知,到2050年对全球碳中和贡献率最大的途径是______ 。
(3)对比图2中三条曲线,得出的结论是:在实验研究的烟气流速范围内,当烟气流速相同时,______ 的脱除率最高。
(4)中学生在生活中践行低碳生活理念的做法是______ (任写一条)。
16.CaCl2⋅2H2O(二水合氯化钙)可用于食品加工、制药等领域。工业上生产CaCl2⋅2H2O的主要流程示意图如图所示。
【查阅资料】CaCl2⋅2H2O受热(温度超过160℃)易分解。
(1)上述设备中,能将固体与液体进行分离的设备是______ 。
(2)流程中粉碎机和搅拌器所起的作用是______ 。
(3)反应器中发生反应的化学方程式为______ 。
(4)蒸发时温度不易过高的原因是______ 。
(5)无水氯化钙具有吸水性,可用作______ 。
17.工业上,高温煅烧碳酸钙(CaCO3)可制得生石灰(CaO)和二氧化碳。
(1)碳酸钙中碳、氧元素的质量比为______ (填最简比)。
(2)如果要制取2.8t氧化钙,需要碳酸钙多少吨?
18.根据如图装置回答问题。
(1)写出标有序号①的仪器名称:______ 。
(2)实验室用二氧化锰和双氧水制取并收集氧气,应选择的发生和收集装置是______ (填字母),发生反应的化学方程式为______ 。
(3)将一只充满CO2的试管倒扣在盛有澄清石灰水的烧杯中,观察到的现象是______ 。
19.天然气的主要成分是甲烷CH4,某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣。
【提出问题】:甲烷燃烧后生成哪些物质?
【查阅资料】:含碳元素物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】甲:CO2、H2O;乙:CO、H2O;丙:CO2、CO、H2O
【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:
(1)实验中用纯净O2.而不用空气的原因______ 。
(2)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中黑色粉末变成红色,由此推断______ 同学猜想成立。
(3)C中黑色粉末变成红色的化学方程式为______ 。
(4)【反思与交流】:为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是______ ;装置末端大气球的作用是______ 。
20.在日常生活中能看到很多精美的金属蚀刻画。兴趣小组利用废弃的金属片进行制作金属蚀刻画的项目活动,请你一起参与下列任务。
任务一:到垃圾回收站筛选金属底板
(1)区分铝片和铁片的物理方法是______ (写一种)。
任务二:预处理金属底板
用砂纸打磨掉铝片表面的氧化膜,用化学方法除去铁片表面的铁锈。
任务三:选择蚀刻液进行蚀刻
(2)首先将有镂空图案的不干胶保护膜(能隔绝蚀刻液与金属底板接触)分别贴到处理好的铝片和铁片上,然后将铝片浸入足量的甲蚀刻液中,将铁片浸入足量的乙蚀刻液中,一段时间后取出。小组同学看到铝片上有凹陷图案,没有附着物;铁片上出现红色附着物图案。则甲蚀刻液、乙蚀刻液分别是下列中的______ 、______ (填序号)。
①硫酸铜溶液ㅤㅤ②硝酸银溶液ㅤㅤ③稀盐酸ㅤㅤ④氯化亚铁溶液
任务四:金属蚀刻画的后处理
将蚀刻好的金属片清洗掉废液,去掉不干胶保护膜,进行装饰。
任务五:废液回收利用
(3)铝片蚀刻废液处理,可加入足量铝片,回收保存。铁片蚀刻废液处理,如图所示:
过程①加入的物质X是______ ,过程②加入稀硫酸反应的化学方程式是______ 。
参考答案
1.A
2.C
3.A
4.C
5.D
6.D
7.B
8.B
9.C
10.D
11.C
12.D
13.D
14.导热。
Al。
常温下,碳的化学性质稳定。
+2
15.绿色植物的光合作用 碳替代 氨基乙酸钾 骑自行车上学(或双面使用纸张)
16.过滤器 增大反应物的接触面积,使反应更快更充分 CaCO3+2HCl=CaCl2+H2O+CO2↑ 防止CaCl2⋅2H2O受热分解 干燥剂
17.1:4 5t
18.集气瓶 BD; 澄清石灰水变浑浊,试管内液面上升
19.空气中本身含有水蒸气和二氧化碳,会干扰对甲烷燃烧产物的检验 丙 提供充足的氧气;收集尾气,防止污染环境
20.用磁铁吸引,能被吸引的是铁片,不能被吸引的是铝片。
③;①。
铁;Fe+H2SO4=FeSO4+H2↑ A.取用块状固体
B.量取液体
C.点燃酒精灯
D.加热液体
实验目的
A.证明分子在不断运动
B.验证CO2的密度比空气大
实验设计
实验目的
C.验证质量守恒定律
D探究铁生锈必须有氧气参与
实验设计
相关试卷
这是一份2025-2026学年湖北省孝感市九年级(上)期末化学试卷(含答案),共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份2025-2026学年湖北省孝感市九年级(上)期末化学试卷(含答案),共7页。
这是一份2025-2026学年湖北省孝感市九年级上学期期末考试化学(含答案)试卷,共8页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)




