




广东省江门市第一中学2025-2026学年高二上学期第一阶段考试化学试卷(Word版附解析)
展开 这是一份广东省江门市第一中学2025-2026学年高二上学期第一阶段考试化学试卷(Word版附解析),文件包含广东省江门市第一中学2025-2026学年高二上学期第一阶段考试化学试卷原卷版docx、广东省江门市第一中学2025-2026学年高二上学期第一阶段考试化学试卷Word版含解析docx等2份试卷配套教学资源,其中试卷共34页, 欢迎下载使用。
本试卷满分 100 分,考试时间:75 分钟
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Fe-56 Cr-52
一、选择题:本题共 16 小题,共 44 分。第 1~10 小题,每小题 2 分;第 11~16 小题,每小题
4 分。在每小题给出的四个选项中,只有一项是符合题目要求的,
1. 在恒容条件下,能使 正反应速率增大且活化分子的数目也增大的措施是
A. 温度不变,增大 的浓度 B. 加入固体碳
C. 温度不变,通入 使气体的压强增大 D. 降低反应的温度
2. 对于可逆反应 A(g)+3B(s) 2C(g) +2D(g),在不同条件下的化学反应速率如下,其中反应速率最快的是
A. v(A)=0.3 ml/(L·s) B. v(B)=1.8 ml/(L·s)
C. v(D)=0.7 ml/(L·s) D. v(C)=1.5 ml/(L·min)
3. 硝酸盐污染已成为一个日益严重的环境问题,甲酸( )在纳米级磁性 (钯)表面
分解为活性 和 ,再经下列历程实现 的催化还原,进而减少污染。已知 Fe(Ⅱ)、Fe(Ⅲ)表
示 中二价铁和三价铁。下列说法错误的是
A. 该生产中 Fe(Ⅱ)起到催化作用
B. 分解时,只有极性共价键发生了断裂
C. 在整个历程中, 可将 完全还原成
D. 反应历程中生成的 可调节体系 pH,有增强 氧化性的作用
4. 对于反应 ,下列有关说法正确的
第 1页/共 12页
是
A. 恒温恒容密闭容器中充入 和 充分反应后放出热量为
B. 该反应反应物的键能之和大于生成物的键能之和
C. 断裂 键的同时,断裂 键,说明该反应达到平衡状态
D. 增大容器的体积,v(正)增加、v(逆)减小
5. 下列有关说法正确的是
A. 化学平衡发生移动,平衡常数必发生变化
B. 加入催化剂,单位体积内反应物分子中活化分子百分数不变
C. 合成氨时将氨液化分离,可提高原料的利用率,可以用勒夏特列原理解释
D. 恒温恒容容器中,N2(g)+3H2(g) 2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时 NH3 的体
积分数一定增大
6. 向澄清石灰水中不断通入二氧化碳气体的过程中,该溶液的导电性的变化是(纵坐标表示导电性,横坐标
表示二氧化碳气体)
A. B. C. D.
7. 可逆反应在密闭容器中进行,如图所示,反应在不同时间 t、温度 T 和压强 p 与生成物浓度的关系曲线,
下列反应中符合图像的是
A.
B.
C.
第 2页/共 12页
D.
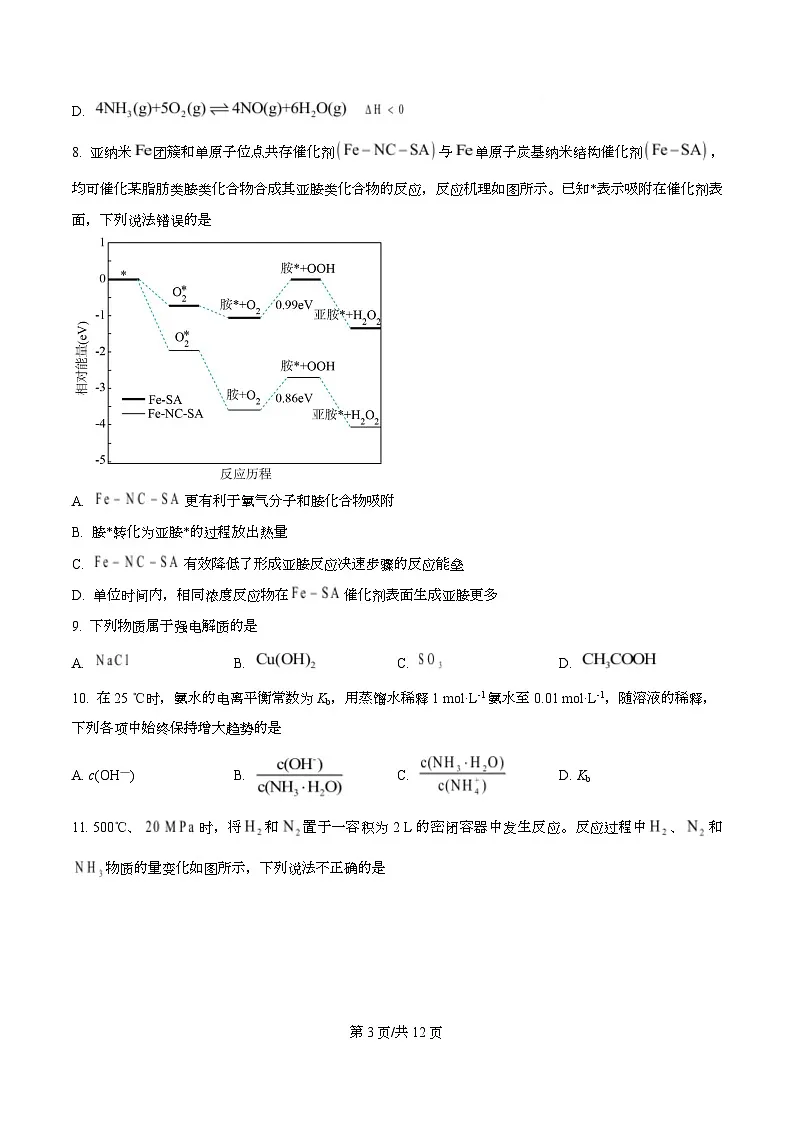
8. 亚纳米 团簇和单原子位点共存催化剂 与 单原子炭基纳米结构催化剂 ,
均可催化某脂肪类胺类化合物合成其亚胺类化合物的反应,反应机理如图所示。已知*表示吸附在催化剂表
面,下列说法错误的是
A. 更有利于氧气分子和胺化合物吸附
B. 胺*转化为亚胺*的过程放出热量
C. 有效降低了形成亚胺反应决速步骤的反应能垒
D. 单位时间内,相同浓度反应物在 催化剂表面生成亚胺更多
9. 下列物质属于强电解质的是
A. B. C. D.
10. 在 25 ℃时,氨水的电离平衡常数为 Kb,用蒸馏水稀释 1 ml·L-1 氨水至 0.01 ml·L-1,随溶液的稀释,
下列各项中始终保持增大趋势的是
A. c(OH—) B. C. D. Kb
11. 500℃、 时,将 和 置于一容积为 2 L 的密闭容器中发生反应。反应过程中 、 和
物质的量变化如图所示,下列说法不正确的是
第 3页/共 12页
A. 反应开始到第一次平衡时, 的平均反应速率为
B. 从曲线变化推测,反应进行到 10 min 至 20 min 时可能使用了催化剂
C. 从曲线变化推测,反应进行至 25 min 时,分离出 的氨气
D. 5 min 后,平衡向正反应方向移动,平衡常数不变
12. 25℃时,0.1 ml/L 醋酸溶液中电离平衡常数 Ka=1.75×10−5,下列说法正确的是
A 向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小
B. 向该溶液中加少量 CH3COONa 固体,平衡正向移动
C. 该温度下 0.01 ml/L 醋酸溶液 Ka<1.75×10−5
D. 升高温度,c(H+)增大,Ka 变大
13. 已知 催化加氢的主要反应有:
反应Ⅰ
反应Ⅱ
在恒温恒压反应器中通入 、 的平衡转化率及 的平衡产率随温度变化关系如下
图。已知: 产率 ; 的选择性 。下列
说法不正确的是
第 4页/共 12页
A.
B. 的平衡选择性随温度的升高而减小
C. 525 K 后,升高温度对反应Ⅰ的影响大于对反应Ⅱ的影响
D. 525 K 时,增大 的值或增大压强均能使 的平衡转化率达到 b 点的值
14. 已知 ,下列有关中和热和燃烧热的说法中,正
确的是
A. 反应热就是热量
B. 在稀溶液中, 和 完全中和时放出的热量小于
C. 溶液与稀 溶液恰好完全反应时,放出 的热量
D. 已知 ,所以,C 的燃烧热是
15. 下列实验中不能达到预期目的是
A.测定反应生成 的速率 B.探究温度对反应速率的影响
第 5页/共 12页
D.探究 和 对 分 C.探究浓度对反应速率的影响
解 催化效果
A. A B. B C. C D. D
16. 在固定容积的密闭容器中,按 与 的物质的量之比为 1∶3 进行投料,发生反应
,在 5MPa 下测得不同温度下平衡体系中各种气体物
质的量分数(n%)如图所示,已知曲线Ⅰ代表 。下列说法正确的是
A. 图中曲线交点 a、b 对应的平衡常数
B. 图中曲线交点 b 对应的 转化率为 40%
C. 平衡时,向体系中加入氢气,氢气转化率变大
D. 若其他条件相同,甲为恒温恒容,乙为绝热恒容,达到平衡时 产率:甲>乙
二、非选择题:本大题共 4 小题,共 56 分。
17. 某研究小组查阅资料发现 与 的反应具有可逆性,推测 与饱和碘水会反应生成 。设计实
验,探究 与饱和碘水能否反应生成 ,实验 1 如下图所示,发现滴加 后溶液未变红。该小
组对溶液未变红的原因进行了如下探究。
第 6页/共 12页
实验 1:
Ⅰ.初步探究
实验 2:用煮沸冷却后的蒸馏水重新配制两种饱和溶液进行实验,(反应时间与实验 1 相同)实验记录如下
表。
饱 和
编号 溶 饱和碘水 煤油 操作
液
2-1 1 滴 不加热
2-2 1 滴 加热一段时间后冷却
(1)写出 与 的反应的离子反应方程式:______。
(2)对比实验 1,实验 2 的目的是探究______、______对反应速率的影响
(3)实验 2 中,加入煤油的目的是______。
(4)小组同学做出推断:反应速率______(填“是”或“不是”)导致实验 1 中溶液未变红的主要原因。
Ⅱ.小组同学猜测,实验 1 未变红,可能与 氧化 反应的平衡限度有关。查阅资料,继续探究实验 3。
【资料】溶液中 较多时,会与 生成 , 为不溶于水的白色固体; 为不溶于
水的黄色固体。
实验 3:
第 7页/共 12页
(5)试管 a 的实验现象说明滤液 1 中含有______。
(6)甲同学对实验 3 提出了质疑,认为其实验现象并不能证明 氧化了 。他提出如下假设:ⅰ.可能
是 氧化了 ;ⅱ.可能是空气中的 氧化了 。
设计、实施了实验 4,实验记录如下表。
编号 实验操作 实验现象
在试管中加入 1 滴 溶液, 蒸馏 溶 液 不 变 4
红
水,1 滴试剂 a,一段时间后加入 1 滴 溶液
①试剂 a 是______。
②依据实验 4,假设ⅰ、ⅱ均不成立
(7)根据实验 1~4 可得结论,实验 1 溶液未变红的原因是______。
18. 的重整利用是当下环境保护的研究热点,对减少温室气体的排放具有重大意义。 合成甲醇涉
及以下三个反应:
Ⅰ.
Ⅱ.
Ⅲ
第 8页/共 12页
(1) ______(填“>”“=”或“=”) ,反应Ⅲ在______(填“高温”“低温”或“任何温度”)可自发进行。
(2)在恒容密闭容器中发生上述反应,下列说法正确的是______(填标号)。
A. 加入催化剂,降低了反应的 ,从而加快了反应速率
B. 混合气体的平均相对分子质量保持不变时,说明反应体系已达到平衡
C. 反应达平衡时,升高温度, 浓度增大
D. 平衡时向容器中充入少量惰性气体,甲醇的产率不变
(3)在一定条件下,发生上述反应Ⅰ和Ⅱ,达平衡时 的转化率随温度和压强的变化如图所示。温度一
定时,压强大小关系是______(从大到小排序)。压强一定时, 的平衡转化率先增大后减小的原因可能
是______;
(4)在保持压强为 的密闭容器中,分别按投料比[ ]为 和 通入气体,
发生反应Ⅰ和Ⅱ, 的平衡转化率 及 的选择性 S 随温度的变化曲线如图所示。
已 知 : ;
第 9页/共 12页
。
①图中的______(填“X”或“Y”)代表 。
②投料比为 3∶1,温度为 300℃时, 的转化率为______。
19. 颗粒大小达到纳米级的单质铁俗称“纳米铁”,可用于处理废水中的硝态氮。以铁屑(含少量 杂
质)为原料制备纳米铁粉流程如下:
(1)写出“酸溶”时发生的属于氧化还原反应的离子方程式除了 外,还有
________。
(2) 固体在空气中灼烧后得到红棕色固体和 、 混合气体,若 ,
则“灼烧”过程中发生反应的化学方程式为______。
(3)“还原”中使用的还原剂为 ,在“还原”过程中需要对装置保持干燥的原因是:______。(用化学
方程式表达)
(4)纳米铁粉被广泛应用于污染物的去除。催化剂协同纳米铁粉能将水体中的硝酸盐( )转化为
,其催化还原反应的过程如图所示。
①在该转化过程中,最终得到的还原产物为______。
②欲证明净化后的纳米铁粉转化为 ,实验操作为______。
③纳米铁粉中铁元素含量测定:准确称取 2.000 g 产品,加入足量盐酸溶解,过滤除去不溶性杂质,滤液移
入 容量瓶,定容至刻度线。取其中 溶液于锥形瓶中,用 溶液
与 反 应 ( ), 恰 好 完 全 反 应 时 , 消 耗 0.05000
第 10页/共 12页
溶液 ,放出 热量为 。问反应
______ (用含有 a 的计算式来表示)。
(5)能在酸性环境下将 氧化为 的氧化剂有 、 、 、 等。已知下列四种
氧化剂氧化 后对应的还原产物如下:
氧化剂
还原产物
若将等物质的量的四种氧化剂分别与足量的酸性 溶液反应,生成 最多的氧化剂是______(填化
学式)。
20. 弱电解质在自然界分布广泛,具有重要用途。
(1)室温下,各酸的电离常数如下:
酸
电离常数( )
①请写出 的电离方程式______。
②结合电离常数判断, 进行的程度较______(填“大”或“小”),其理由是______
。(从化学平衡常数角度回答)
(2)室温时, 某一元酸 HA 在水中有 0.1%发生电离,则此时: 的电离平衡常数。K=______。
(3)下列反应不能发生的是______(填序号)。
A.
B.
C.
D.
(4)用体积相同, 相同的① ;② ;③ 三种酸溶液分别和等浓度的 溶
第 11页/共 12页
液发生中和反应,消耗 溶液的体积由大到小的排列顺序是______(填序号)。
(5)25℃时,向 溶液中逐滴加入 溶液。溶液中 、
、 的物质的量分数随 pH 变化如图所示,则草酸的第二步电离常数 ______。
( )
第 12页/共 12页
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





