



安徽省阜阳市临泉县田家炳实验中学(临泉县教师进修学校)2024-2025学年高三下学期4月期中化学试题(Word版附解析)
展开 这是一份安徽省阜阳市临泉县田家炳实验中学(临泉县教师进修学校)2024-2025学年高三下学期4月期中化学试题(Word版附解析),文件包含安徽省阜阳市临泉县田家炳实验中学临泉县教师进修学校2024-2025学年高三下学期4月期中化学试题Word版含解析docx、安徽省阜阳市临泉县田家炳实验中学临泉县教师进修学校2024-2025学年高三下学期4月期中化学试题原卷版docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。
可能用到的相对原子质量: O 16 Li 7 Na 23 Mg 24 Zn 65
一、选择题:本大题共 14 小题,共 42 分。在每小题列出的四个选项中,只有一项符合题目
要求。
1. 岭南文化源远流长,其中文物是了解古代岭南文化的重要途径。下列是韶关、河源、清远、惠州四市博
物馆的重要馆藏文物,其主要成分不属于硅酸盐的是
A. 明青白釉开片瓷瓶 B. 清玉手镯 C. 东汉双系耳铜釜 D. 明三彩陶出行仪仗队
【答案】C
【解析】
【详解】A.明青白釉开片瓷瓶,为陶瓷器件,其主要成分属于硅酸盐,A 不符合题意;
B.玉手镯主要含阳起石、透闪石等矿物,其主要成分属于硅酸盐,B 不符合题意;
C.东汉双系耳铜釜,是合金,属于金属材料,C 符合题意;
D.明三彩陶出行仪仗队,是陶瓷制品,其主要成分属于硅酸盐,D 不符合题意;
故选 C。
2. 下列说法正确的是
A. “华龙一号”核电站投产,其反应堆所用铀棒含有的 U 与 U 互为同素异形体
B. 隐形战机 隐身涂层材料之一为石墨烯,石墨烯是一种化学纤维
C. 长征二号 F 运载火箭的燃料为偏二甲肼—四氧化二氮,四氧化二氮为酸性氧化物
D. “天舟 6 号”实验舱采用砷化镓(GaAs)太阳能电池,GaAs 是一种优良的半导体材料
【答案】D
【解析】
【详解】A.同素异形体是同一元素形成的不同单质, 与 U 互为同位素,A 错误;
第 1页/共 21页
B.石墨烯是碳的单质,而非化学纤维。化学纤维为高分子材料(如尼龙),B 错误;
C.四氧化二氮(N2O4)与碱反应生成硝酸盐、亚硝酸盐和水,不属于酸性氧化物,C 错误;
D.砷化镓(GaAs)是化合物、是半导体材料,广泛用于太阳能电池,D 正确;
故选 D。
3. 共享美好生活,衣食住行皆化学。下列说法错误的是
A. 合成布料涤纶( )的单体有两种
B. 合成氨工业是粮食生产的基础,合成氨选择较高温度是为了提高平衡产率
C. 照相机采用含 Pb 原料制造的光学玻璃作镜头
D. 青蒿素是治疗疟疾的药物,用乙醚提取青蒿中的青蒿素属于萃取操作
【答案】B
【解析】
【详解】A.涤纶是缩聚产物,合成涤纶有 和 两种单体,A
正确;
B.合成氨反应是放热反应,高温使平衡向逆反应方向进行,平衡产率降低,高温适合催化剂发挥催化效能,
同时有利于提高反应速率,B 错误;
C.玻璃生产过程中加入 Pb 制造具有特殊用途 光学玻璃,C 正确;
D.青蒿素难溶于水、易溶于乙醚等有机溶剂,用乙醚提取青蒿中的青蒿素属于固-液萃取操作,D 正确;
故选 B。
4. “为国育才,五育并举”,美育是五育重要组成部分。化学美随处可见。下列说法正确的是
A. 环己烷是正六边形的平面结构
B. 苯酚因其具有还原性,久置于空气中会变成粉红色
C. 五光十色的霓虹灯发生了放热发光的化学反应
D. 足球烯( )结构对称且含极性键和非极性键
【答案】B
【解析】
【详解】A.环己烷中碳原子均为 sp3 杂化,6 个碳原子不可能在同一平面,A 错误;
B.苯酚有还原性,易被氧气氧化,久置于空气中变成粉红色,B 正确;
第 2页/共 21页
C.霓虹灯中充入惰性气体,在高压电场下电子被激发,然后在回到基态的过程中释放出能量,其中一部分
能量被荧光粉吸收发出可见光,没有生成新物质,没有发生化学反应,C 错误;
D.足球烯是由 60 个碳原子构成的分子,碳原子之间的键属于非极性键,没有极性键,D 错误;
故选 B。
5. 学校积极开展劳动教育,以劳增智,以劳强体,以劳创新。下列化学知识说法不正确的是
选项 劳动活动 化学知识
A 烹饪活动:向沸汤中加入蛋液做蛋花汤 加热使蛋白质变性
B 学农活动:常见肥料可选择氮肥、磷肥、钾肥等 尿素 CO(NH2)2 是一种常见的氮肥
铁丝在 O2 中燃烧生成的 Fe3O4 是红砖的主要 C 摄影活动:南宁青瓦房红砖和青砖交相辉映
成分
有利于垃圾的针对性回收和处理, D 爱国卫生活动:对垃圾进行分类投放
减少环境污染,变废为宝
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.蛋液中含蛋白质,在加热条件下蛋白质会发生变性,A 正确;
B.尿素中含有 N 元素,能够被植物吸收,尿素是一种常见的氮肥,B 正确;
C.铁丝在 O2 中燃烧生成的 Fe3O4 是黑色的固体,红砖的主要成分应是 Fe2O3,C 错误;
D.垃圾是放错地方的资源,对垃圾进行分类投放,有利于垃圾的针对性回收和处理,减少环境污染,变废
为宝,D 正确;
故选 C。
6. 某实验小组利用微型实验装置进行氯气的制备和性质探究,装置如图所示,下列有关说法错误的是
第 3页/共 21页
A. 与浓盐酸反应,HCl 只体现还原性
B. 浸有淀粉 KI 溶液的脱脂棉变蓝,说明氧化性
C. 新鲜花瓣褪色是因为氯气与水反应生成的 HClO 有漂白性
D. 浸有 NaOH 溶液的脱脂棉可吸收过量氯气
【答案】A
【解析】
【详解】A. 与浓盐酸反应生成氯气、KCl、水,HCl 体现还原性和酸性,A 错误;
B.浸有淀粉 KI 溶液的脱脂棉变蓝,说明氯气和碘离子反应生成碘单质,氧化性 ,B 正确;
C.新鲜花瓣褪色是因为氯气与水反应生成的 HClO 能使有色物质褪色,HClO 有漂白性,C 正确;
D.氯气有毒,能和碱性物质反应,故浸有 NaOH 溶液的脱脂棉可吸收过量氯气减小污染,D 正确;
故选 A。
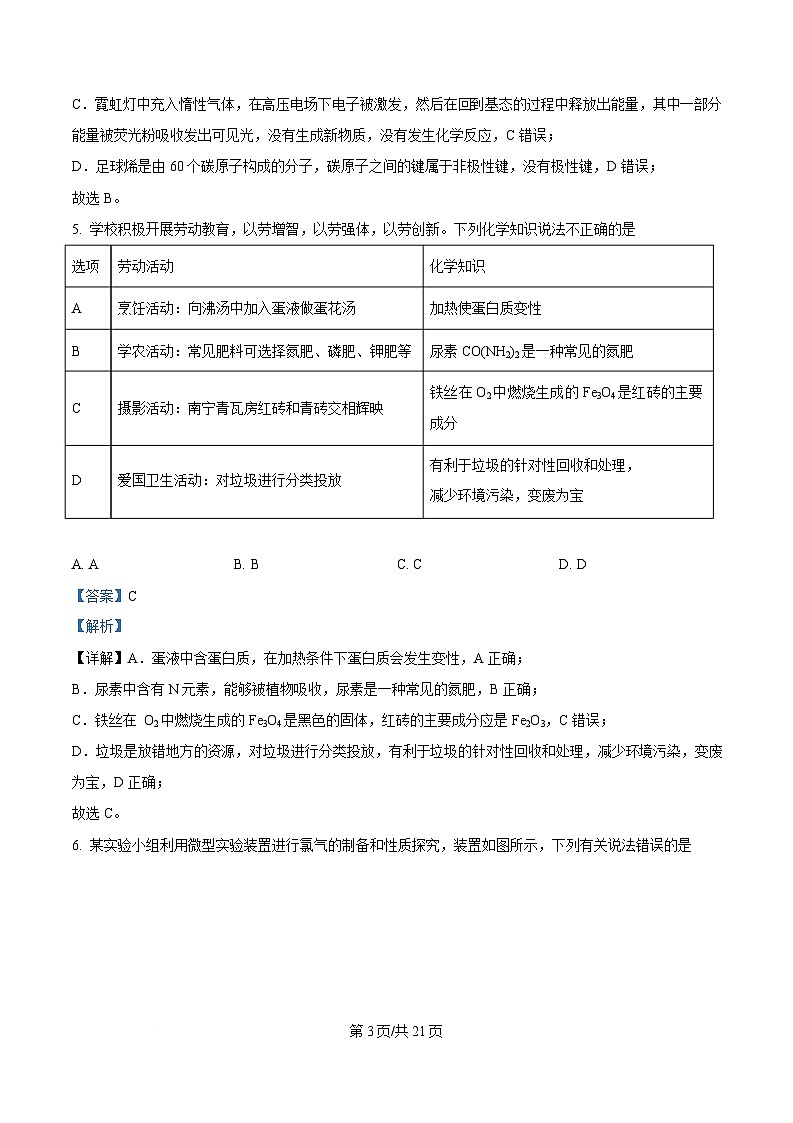
7. 表面喷淋水的活性炭可将溶解于水的氧气解离成活性氧原子,从而实现吸附氧化 ,其原理可用下图
表示。下列说法错误的是
A. 溶于水膜的 发生电离:
B. 水膜中发生反应:
第 4页/共 21页
C. 适当提高水膜 ,可增大 的去除率
D. 水膜越厚, 的去除率越大
【答案】D
【解析】
【详解】A.硫化氢为弱酸,在溶液中部分电离,A 正确;
B.由图可知,水膜中硫氢根离子和氧原子转化为氢氧根和水,发生反应: ,B 正确;
C.适当提高水膜 ,可促进硫化氢电离出硫氢根离子,增大 去除率,C 正确;
D.水膜越厚,则氧分子分解为氧原子难度加大, 的去除率会降低,D 错误;
故选 D。
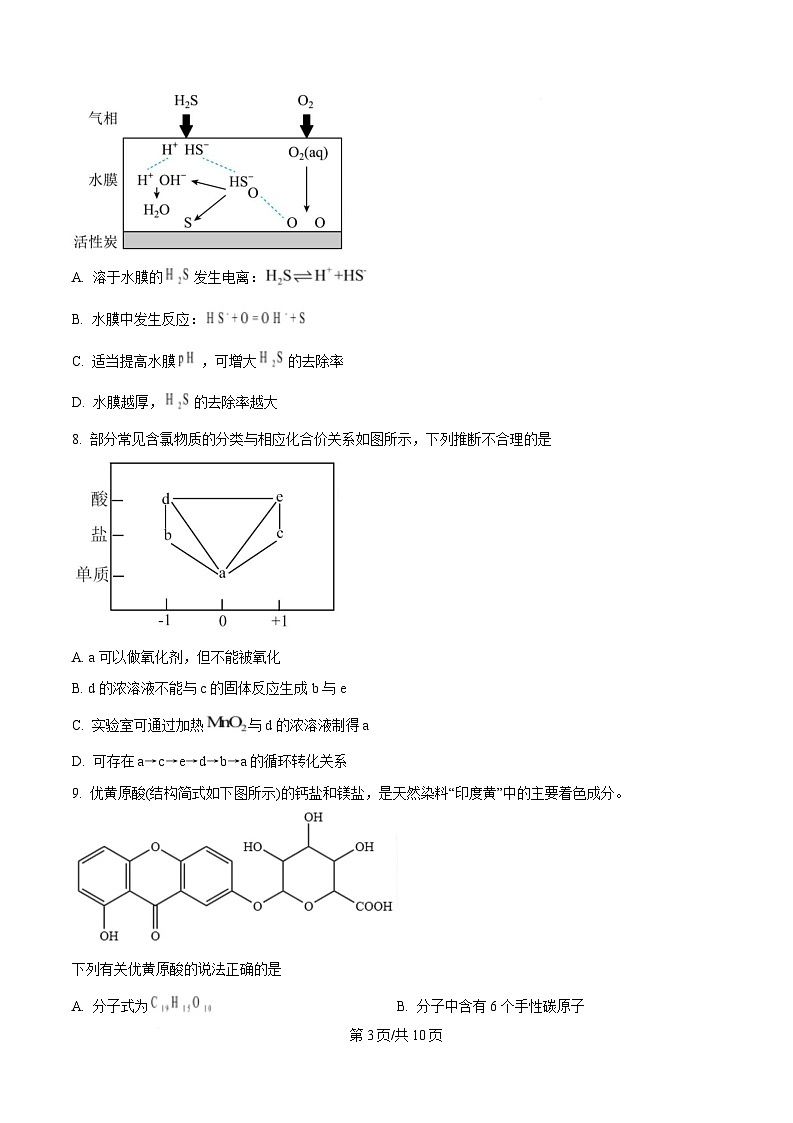
8. 部分常见含氯物质的分类与相应化合价关系如图所示,下列推断不合理的是
A. a 可以做氧化剂,但不能被氧化
B. d 的浓溶液不能与 c 的固体反应生成 b 与 e
C. 实验室可通过加热 与 d 的浓溶液制得 a
D. 可存在 a→c→e→d→b→a 的循环转化关系
【答案】A
【解析】
【分析】由图可知,a 为 Cl2,b 为盐酸盐,c 为次氯酸盐,d 为盐酸,e 为次氯酸。
【详解】A.由分析可知,a 为 Cl2,其中 Cl 元素的化合价为 0 价,既可以升高也可以降低,故既可被氧化,
也可被还原,故 A 错误;
B.浓盐酸和次氯酸盐发生归中反应生成氯气,不会生成盐酸盐和次氯酸,故 B 正确;
C.实验室可以通过加热 和浓盐酸制备氯气,故 C 正确;
第 5页/共 21页
D.可存在 a→c→e→d→b→a 的循环转化关系,即 Cl2 ClO- HClO HCl Cl-
Cl2,故 D 正确;
故答案选 A。
9. 优黄原酸(结构简式如下图所示)的钙盐和镁盐,是天然染料“印度黄”中的主要着色成分。
下列有关优黄原酸的说法正确的是
A. 分子式为 B. 分子中含有 6 个手性碳原子
C. 能与 溶液发生显色反应 D. 该物质最多消耗
【答案】C
【解析】
【详解】A.由优黄原酸的结构简式可知其分子式为 ,A 错误;
B.手性碳原子是指与四个各不相同原子或基团相连的碳原子,该分子中含有 5 个手性碳原子,位置为
,B 错误;
C.该分子中含有酚羟基,能与 溶液发生显色反应,C 正确;
D.该分子中含有 1 个酚羟基和 1 个羧基可以和 NaOH 反应,则 该物质最多消耗 ,D 错误;
故选 C。
10. 某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。下列说法不
正确的是
第 6页/共 21页
A. a、b、c 中依次盛装 70%硫酸、Na2SO3 固体、NaOH 溶液
B. 实验时,湿润的 pH 试纸、鲜花、品红溶液、KMnO4 溶液均褪色,Na2S 溶液出现淡黄色沉淀
C. 此设计可证明 SO2 水溶液的酸性,SO2 的氧化性、还原性、漂白性
D. 点燃酒精灯加热,品红溶液恢复原色,KMnO4 溶液不恢复原色
【答案】B
【解析】
【分析】根据 SO2 的制备以及 SO2 的性质(酸性氧化物、还原性、氧化性、漂白性)解答。
【详解】A.70%硫酸与亚硫酸钠反应生成 SO2,多余的 SO2 气体最后用 NaOH 溶液吸收,所以 a、b、c 中
依次盛装 70%硫酸、Na2SO3 固体、NaOH 溶液,A 正确;
B.SO2 不能漂白 pH 试纸,SO2 与水反应生成亚硫酸,使湿润的 pH 试纸显红色,所以湿润的 pH 试纸不褪
色,B 错误;
C.SO2 水溶液使 pH 试纸变红说明其水溶液具有酸性,SO2 能使鲜花、品红溶液褪色说明有漂白性,使高
锰酸钾溶液褪色说明有还原性,与 Na2S 反应生成 S 说明有氧化性,C 正确;
D.SO2 与品红溶液反应生成的无色物质不稳定,受热易分解,点燃酒精灯加热,品红溶液可恢复原色,KMnO4
溶液与 SO2 发生氧化还原反应,加热不恢复原色,D 正确;
故选 B。
11. 一种微生物燃料电池可将醋酸盐作为燃料转化为对环境友好的产物,其原理如下图所示。双极膜间的
解离为 和 并分别向两极迁移。
第 7页/共 21页
下列说法错误的是
A. 电极 b 的电势高于电极 a 的电势
B. 电池工作时,双极膜中 向电极 a 迁移
C. 电极 a 的反应为:
D. 理论上,消耗的醋酸根与氧气的物质的量之比为
【答案】B
【解析】
【分析】醋酸盐中的碳元素化合价升高,发生氧化反应,则电极 a 为电池的负极,电极反应式为:
,电极 b 为电池的正极,电极反应式为:Fe3++e-= Fe2+,据此分
析回答。
【详解】A.由分析可知,电极 a 为负极,电极 b 为正极,正极的电势高于负极的电势,故 A 项正确;
B.阳离子向原电池的正极迁移,则电池工作时,双极膜中 H+向电极 b 迁移,故 B 项错误;
C.由分析可知,电极 a 为负极,电极反应式为: ,故 C 项正确;
D.根据电极反应式: ,消耗 1ml ,转移 8ml 电子;
根据离子方程式:4Fe2++4H++O2= 4Fe3++2H2O,消耗1mlO2 转移4ml电子,当转移8ml电子时,消耗2mlO2,
则消耗醋酸根与氧气的物质的量之比为 1:2,故 D 项正确;
故本题选 B。
12. 设 为阿伏加德罗常数的值。四乙基铅[ ,熔点为-136℃]可用作汽油抗爆震剂,制备原理
为 。下列说法错误的是
A. 含有的价电子数目为
第 8页/共 21页
B. 中所含共价键的数目为
C. 中 杂化的原子数目为
D. 每消耗 ,反应转移的电子数目为
【答案】C
【解析】
【详解】A. 是第 IVA 族元素,价电子数为 4,故 含有的价电子数目为 ,A 正确;
B. 的结构式为 ,因此 中所含共价键的数目为 ,B 正确;
C.乙基中碳原子的价层电子对数都为 4,采取 杂化,而 与 4 个乙基中的碳原子分别形成 1 个配位键,
即 也采取 杂化,故 中 杂化的原子数目为 ,C 错误;
D.反应 中, 失去电子生成 , 元素化合价由 0 价
升高至+4 价,因此每消耗 ,反应中共转移 电子, 的物质的量为 ,则转移的
电子数目为 ,D 正确;
故选 C。
13. 下列实验操作能达到实验目的的是
选项 实验目的 实验操作
检验 中是否含 向 溶液中先加入过量稀硝酸,再加入几滴
A
有 杂质 溶液
向麦芽糖溶液中加入几滴稀硫酸,再向所得水解液中
探究麦芽糖水解产物是否
B
具有还原性 滴入少量新制 ,加热
将 1-溴丁烷和沸石加入 的乙醇溶液中,微热;
C 检验 1-溴丁烷的消去产物
将产生的气体通入酸性 溶液中
第 9页/共 21页
向 溶液中加入 2 滴 比较 和
D
溶液,再加入 4 滴 的大小
溶液
A A B. B C. C D. D
【答案】D
【解析】
【详解】A.硝酸可以将 氧化为硫酸根,加入几滴 溶液也会生成白色沉淀,不能达到实验
目的,故 A 错误;
B.没有加碱将溶液调节为碱性溶液,向所得水解液中滴入少量新制 ,加热,无红色沉淀,另外,
麦芽糖本身也是还原性糖,无法确定麦芽糖是否一定发生了水解,故 B 错误;
C.产生的 1-丁烯中混有乙醇蒸气,这两种气体都能使酸性高锰酸钾溶液褪色,故不能说明有 1-丁烯生成,
故 C 错误;
D.向 溶液中加入 2 滴 溶液,生成白色沉淀,而且硝酸银少量,
再加入 4 滴 溶液,白色沉淀变为黄色,说明氯化银转化为了碘化银,故说明
,故 D 正确;
故选 D。
14. 新型 Li-Mg 双离子可充电电池是一种高效、低成本的储能电池,其工作原理如图所示。放电时电极 a
的反应为: ;下列说法不正确的是
A. 充电时, 极为阴极
第 10页/共 21页
B. 放电时, 从 I 室向 II 室迁移
C. 放电时,II 室 溶液的浓度增大
D. 每消耗 ,电极 a 质量理论上增加
【答案】C
【解析】
【详解】A.放电时电极 a 的反应为: ,a 为正极, 为负极,所以充
电时 为阴极,A 正确;
B.放电时 I 室为负极区,II 室为正极区,阳离子向正极移动,所以向 II 室迁移,B 正确;
C.放电时电极 a 的反应为: ,消耗 ,同时锂离子通过透过膜进入 II
室,所以 溶液的浓度不变,C 错误;
D.放电时 发生反应: ,当有 发生反应时,转移 ,电极 a 质量理论上
增加 ,质量为: ,D 正确;
故选 C。
二、非选择题:本大题共 4 小题,共 58 分。考生根据要求作答。
15. CuCl2 是常见的化学试剂,学习小组开展了与 CuCl2 相关的系列实验。回答下列问题:
I.利用废铜屑制备 CuCl2(实验装置如下图所示)
(1)仪器 a 的名称为_______。
(2)“湿法”制备 CuCl2 的化学方程式为_______。
(3)①石英管内可能观察到的现象为_______。
②石英管直接伸入收集装置,该管较粗,其优点是_______。
(4)除上述两种方法外,实验室中还可先将铜粉_______(填试剂及操作),再加入适量稀盐酸反应得到 CuCl2
第 11页/共 21页
溶液。
II.探究 Al 与 CuCl2 溶液的反应
将铝片放入盛有 0.1ml·L-1CuCl2 溶液的试管中,观察到现象为:铝片表面析出疏松的紫红色固体,产生无
色无味气体,溶液颜色变浅。
(5)紫红色固体为_______(填化学式)。
(6)经检验产生的气体为 H2.在 CuCl2 溶液中存在 Cu2++2H2O=Cu(OH)2+2H+、2A1+6H+=2A13++3H2↑,小组
成员认为应产生 Cu(OH)2,但实际实验中并未观察到蓝色沉淀。于是他们提出了以下两种猜测并进行相关验
证。完成下列表格:
猜测 实验 现象 结论
i.① 取少量 Cu(OH)2 悬浊液,加入打磨 猜想 i
无明显现象
_______。 过的铝片,振荡 不成立
ii.Cu(OH)2
猜想 ii 与 Al3+发生 ②_______。 固体立即溶解,溶液呈浅绿色
成立 了反应
③在猜测 ii 成立的基础上,该小组成员查阅文献发现体系中可能存在反应:2A13
++3Cu(OH)2=2Al(OH)3+3Cu2+,列式计算平衡常数分析该反应进行的趋势___________________。(已知:Ksp
[Cu(OH)2]=2.2×10-20;Ksp[A1(OH)3]=1.3×10-33。一般认为,K>105 时反应进行较完全,K
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





