

河南省南阳市淅川县第一高级中学2024-2025学年高一下学期3月考化学试卷(原卷版+解析版)
展开 这是一份河南省南阳市淅川县第一高级中学2024-2025学年高一下学期3月考化学试卷(原卷版+解析版),共9页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
1. 化学知识与生活息息相关,下列说法正确是:
A. 早晨的雾气,牛奶,淀粉溶液的溶质微粒半径都在1~100nm之间,所以它们都是胶体
B. C60又叫富勒烯,在医学上有很多用途,它与航天器材上常用的碳纤维互为同素异形体
C. 奋斗者号潜水艇用到的氧化铝陶瓷属于无机非金属材料
D. 自古书契,多编以竹简,其用缣帛者谓之为纸”文中“纸”主要成分是纤维素
2. 下列实验不能作为判断依据的是
A. 钠和镁分别与冷水反应,判断钠和镁金属性强弱
B. 比较与的碱性强弱,判断镁与铝的金属性强弱
C. 往硅酸钠溶液中通入产生白色沉淀,判断碳酸与硅酸的酸性强弱
D. 根据和的水溶液的酸性强弱判断氟与氯的非金属性的强弱
3. X、Y、Z、W、M为原子序数依次增大的前20号主族元素,其中仅有一种金属元素,且只有两种元素处于同一周期。自然界中Z的单质主要存在于火山口附近,X和Y最外层电子数之和是M最外层电子数的3倍。下列说法一定正确的是
A. X与Y、Z、W均可形成18电子微粒
B 简单离子半径:
C. 稳定性:
D. 氧化物对应水化物的酸性:
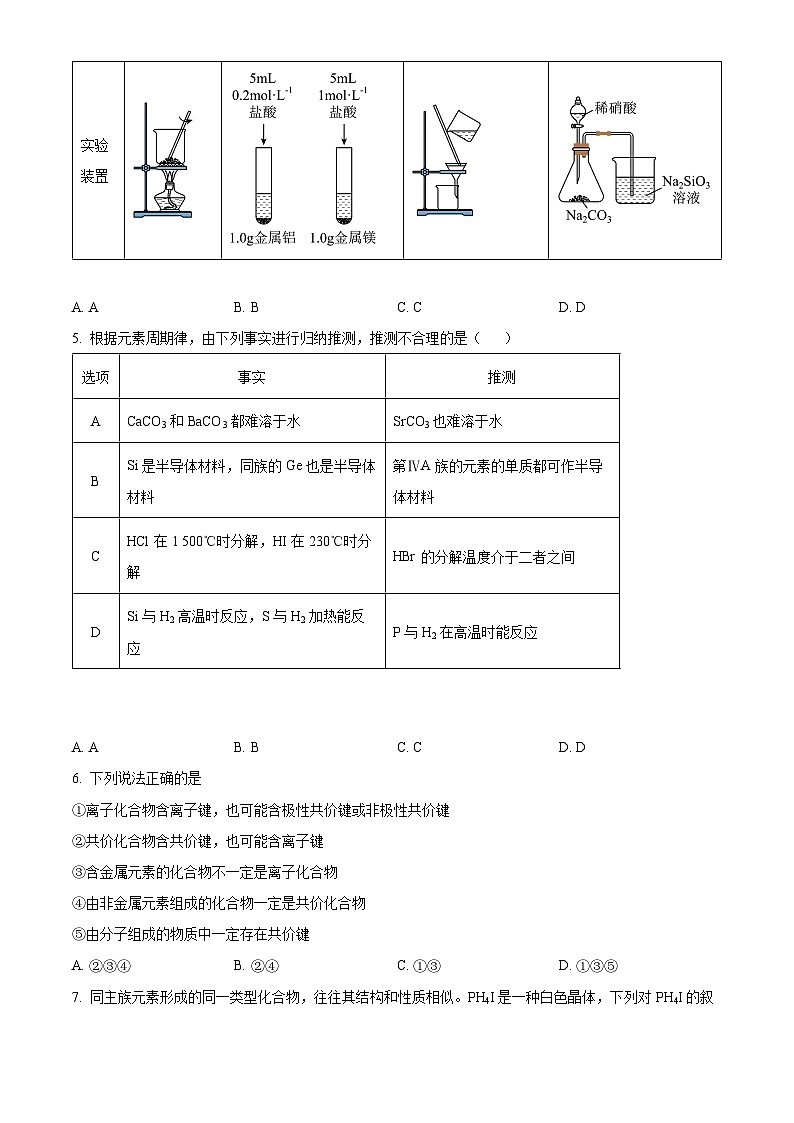
4. 利用图中实验装置进行相应实验,能达到实验目的的是
A. AB. BC. CD. D
5. 根据元素周期律,由下列事实进行归纳推测,推测不合理的是( )
A. AB. BC. CD. D
6. 下列说法正确的是
①离子化合物含离子键,也可能含极性共价键或非极性共价键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
A. ②③④B. ②④C. ①③D. ①③⑤
7. 同主族元素形成的同一类型化合物,往往其结构和性质相似。PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是
A. 它是一种共价化合物
B. 它既含离子键又含共价键
C. 它不可能与NaOH溶液反应
D. 它受热时,不易分解
8. 用“—”表示一对共用电子,省略未成键电子即可得到结构式,例如NH3的结构式为。已知一种麻醉剂的分子结构式如图所示,其中X、Y、Z、W、E为原子序数依次增大的短周期元素,元素E的原子比W原子多8个电子。下列说法不正确的是
A. XEZ是一种强氧化性弱酸
B. X与Z能形成含非极性键的化合物
C. 原子半径:Y>Z>W>X
D. 该分子中所有原子均满足最外层8电子稳定结构
9. 已知某化学反应A2(g)+2B2(g)=2AB2(g)(A2、B2、AB2的结构式分别为A=A、B-B、B-A-B),反应过程中的能量变化如图所示,下列有关叙述正确的是
A. 该反应的进行一定需要加热或点燃
B. 该反应若生成2mlAB2(g),则放出的热量为(E1-E2)kJ
C. 该反应断开化学键吸收的总能量大于形成化学键放出的总能量
D. 生成2mlB-A键放出E2kJ能量
10. 阳离子X2+含N个中子,X的质量数为A,则a g X的同价氧化物中含质子的物质的量是
A. (N-a) mlB. (A-N+10) mlC. (N+A) mlD. (A-N+8) ml
11. 海洋中有丰富“食品、矿产、能源、药物和水产资源”等,下列说法正确的是
A. 第①步中除去粗盐中的SO、Ca2+、Mg2+等杂质,加入药品的顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液、过滤后加盐酸
B. 工业上通过电解氯化钠溶液制取金属钠
C. 第③步到第⑤步的目的是为了富集溴元素
D. 第④步离子方程式为SO2+Br2+2H2O=2HBr+2H++SO
12. 高纯度晶体硅是典型的无机非金属材料,它的发现和使用曾引起计算机芯片上的一场伟大“革命”。工业上可以按下列方法制备:。下列说法正确的是
A. 硅的性质稳定,在自然界主要以单质形式存在
B. 步骤①的化学方程式为
C. 可用盐酸除去石英砂(主要成分为SiO2)中少量的碳酸钙
D. SiO2既可以与NaOH溶液反应,也可以与氢氟酸反应,因此SiO2属于两性氧化物
13. 短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中W的气态氢化物摩尔质量为34 g·ml-1,Y的最低价氢化物为非电解质,则下列说法中正确的是
A. X的最低价氢化物水溶液显酸性
B. Q元素氧化物的水化物的酸性比Y元素氧化物的水化物的酸性强
C. Na与Y能形成化合物Na2Y2,且与水反应后溶液呈碱性
D. 阴离子还原性:W>Q
14. 用四氯化碳萃取碘的饱和水溶液中的碘,下列说法中不正确的是
A. 实验使用的主要仪器是分液漏斗
B. 碘在四氯化碳中的溶解度比在水中的溶解度大
C. 碘的四氯化碳溶液呈紫红色
D. 分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出
15. X、Y、Z、W 为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断错误的是
A. 反应①、②、③都属于氧化还原反应
B. X、Y、Z、W四种元素中,Y的原子半径最小
C. Na 着火时,可用甲扑灭
D. 一定条件下,x与甲反应生成丁
二、填空题(本题共 4 小题,共 55 分)
16. 下表列出了①~⑦七种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素①气态氢化物的电子式是_______。
(2)在这七种元素中,元素⑥的离子结构示意图是_______。
(3)元素③和⑦可形成化合物,用电子式表示其形成过程:_______。
(4)比较元素②、③、④的离子半径大小:_______(用离子符号表示)。
(5)元素③单质与水反应的离子方程式为_______。
(6)这些元素最高价氧化物对应的水化物中,酸性最强的是(填化学式)_______,碱性最强的是(填化学式)_______。
(7)写出元素⑤的单质与氢氧化钠溶液反应的化学方程式:_______。
17. 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示:
(1)写出工业上由食盐制备的离子方程式:___________。
(2)步骤Ⅰ中已获得,步骤Ⅱ中又将转化为和,其目的是___________。
(3)步骤Ⅱ中通入热空气吹出,利用了的___________(填标号)。
A. 氧化性B. 还原性C. 挥发性D. 腐蚀性
(4)步骤Ⅱ中用纯碱溶液吸收,该反应的化学方程式为___________。
(5)从理论上考虑,下列物质也能吸收的是___________(填标号)。
A. B. NaCl溶液C. 溶液D. 溶液
(6)查阅资料知,的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是___________,蒸馏温度过高或过低都不利于生产,请解释原因:___________。
18. 实验室中药品的保存和实验的安全至关重要,药品的正确保存和实验的规范操作是进行科学实验的基础。
(1)下列关于药品保存或事故处理应对正确的是___________。
A. 金属钠着火时,用湿抹布覆盖
B. 氯水短期保存可以装在棕色细口瓶并置于阴凉处
C. 氢氟酸可以保存玻璃瓶中
D. 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
(2)氢氧化钠的保存不能用玻璃塞,原因是(用化学反应方程式表示)___________。
(3)Na2SiO3的水溶液俗称水玻璃,在空气中久置后会产生白色胶状沉淀,原因是(用化学反应方程式表示)___________。
(4)下列选用的试剂(括号内的物质)不正确的是___________。
A. 检验二氧化硫的漂白性(石蕊溶液)
B. 干燥氨气(无水)
C. 洗涤沾有硫磺的试管(热的溶液)
D 硫酸工业中吸收(浓硫酸)
(5)实验员小张想要熔融NaOH,他应选用的仪器是___________。
A. 蒸发皿B. 铁坩埚C. 氧化铝坩埚D. 石英坩埚
(6)实验员小周不小心将稀硫酸混入了稀硝酸,为确定其成分,做了如下实验:取该混合溶液100mL,将其平均分成两份。向其中一份逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。则原混合溶液中的物质的量为___________,如果向另一份混合溶液加入铜粉,则最多能溶解___________铜粉。
19. 为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程:Ⅰ.打开,关闭,,打开活塞a,滴加浓盐酸。
Ⅱ.关闭,打开,,当B和C中的溶液都变为黄色时,关闭。
Ⅲ. B中继续通气体,当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.…
回答下列问题:
(1)装置A中m的作用_______。
(2)能说明氯气的氧化性强于碘的实验现象是_______。
(3)用离子方程式解释过程Ⅱ中溶液变为黄色的原因_______。
(4)过程Ⅲ的实验目的是_______。
(5)请用原子结构的知识解释氯、溴、碘单质的氧化性还渐减弱的原因_______。
(6)利用下图装置也可以验证非金属性的变化规律。
若要证明非金属性:Cl > C >Si,则A中加入试剂_______、B中加Na2CO3、C中加入试剂_______。
选项
A
B
C
D
实验目的
将海带灼烧成灰
探究镁、铝的失电子能力强弱
从的悬浊液中分离出碘单质
验证得电子能力:N>C>Si
实验装置
选项
事实
推测
A
CaCO3 和 BaCO3 都难溶于水
SrCO3 也难溶于水
B
Si 是半导体材料,同族的 Ge 也是半导体材料
第ⅣA 族的元素的单质都可作半导体材料
C
HCl 在 1 500℃时分解,HI 在 230℃时分解
HBr 的分解温度介于二者之间
D
Si 与 H2 高温时反应,S 与 H2 加热能反应
P 与H2 在高温时能反应
X
Y
Z
W
Q
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





