所属成套资源:备战2025年高考化学抢押秘籍(山东专用)【精品】抢分秘籍
备战2025年高考化学抢押秘籍(山东专用)猜押工艺流程综合题(学生版+解析)练习
展开 这是一份备战2025年高考化学抢押秘籍(山东专用)猜押工艺流程综合题(学生版+解析)练习,文件包含备战2025年高考化学抢押秘籍山东专用猜押工艺流程综合题教师版docx、备战2025年高考化学抢押秘籍山东专用猜押工艺流程综合题学生版docx等2份试卷配套教学资源,其中试卷共41页, 欢迎下载使用。
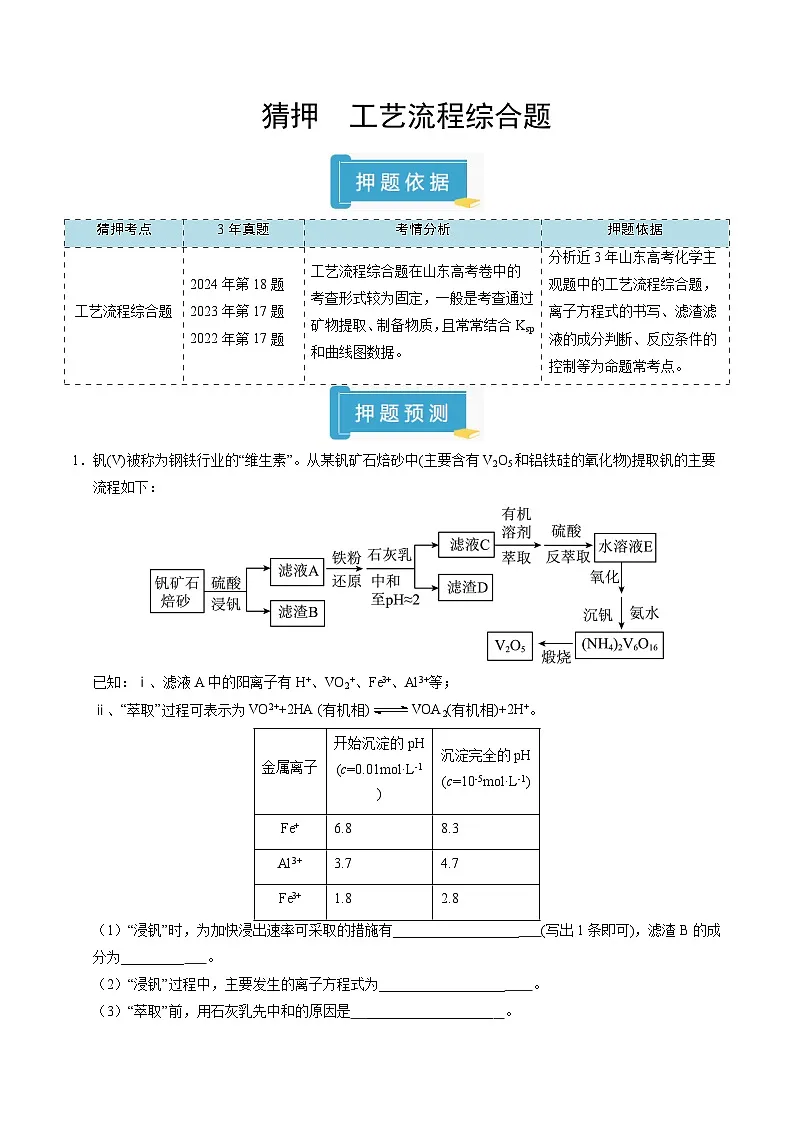
1.钒(V)被称为钢铁行业的“维生素”。从某钒矿石焙砂中(主要含有V2O5和铝铁硅的氧化物)提取钒的主要流程如下:
已知:ⅰ、滤液A中的阳离子有H+、VO2+、Fe3+、Al3+等;
ⅱ、“萃取”过程可表示为VO2++2HA (有机相)VOA2(有机相)+2H+。
(1)“浸钒”时,为加快浸出速率可采取的措施有__________________ (写出1条即可),滤渣B的成分为_________ 。
(2)“浸钒”过程中,主要发生的离子方程式为__________________ 。
(3)“萃取”前,用石灰乳先中和的原因是 __________________ 。
(4)“萃取”与“反萃取”的目的是 ,都需要用到的主要玻璃仪器是_________,假设“滤液C”中c(VO2+)=aml·L-1,“萃取”和“反萃取”每进行一次,VO2+萃取率为90%,4次“萃取和反萃取”后,“滤液C”中残留的c(VO2+)=__________ml·L-1。(萃取率=×100%)
(5)写出“煅烧”过程发生反应的化学方程式 __________________ 。
【答案】(1)适当增大硫酸浓度、适当升高温度、将矿石粉碎(合理即可) SiO2
(2) V2O5+2H+=2VO2++H2O
(3)若不用石灰乳中和,溶液中c(H+)较大,不利于平衡VO2++2HA (有机相)VOA2(有机相)+2H+正向移动,对VO2+萃取效果不好
(4)将VO2+与其他金属离子分离开 分液漏斗 a×10-4
(5) (NH4)2V6O162NH3↑+3V2O5+H2O
【解析】钒矿石焙砂用硫酸浸钒,滤液A中的阳离子主要有H+、VO2+、Fe3+、Al3+等,加铁粉把VO2+还原为VO2+、把Fe3+还原为Fe2+,加石灰乳调节pH=2;滤液C用有机溶剂萃取VO2+,VOA2(有机相)中加硫酸使VO2++2HA (有机相)VOA2(有机相)+2H+平衡逆向移动,反萃取VO2+,把VO2+氧化为VO2+,加氨水生成(NH4)2V6O16沉淀,(NH4)2V6O16煅烧得V2O5。(1)加快浸出速率可采取的措施有适当增大硫酸浓度、适当升高温度、将矿石粉碎等。结合原料和滤液A中的离子可知,滤渣B为SiO2,SiO2是酸性氧化物,与硫酸不反应。(2)“浸钒”过程中,V2O5转变为VO2+,反应方程式为V2O5+2H+=2VO2++H2O。(3)若不用石灰乳中和,溶液中c(H+)较大,不利于平衡VO2++2HA (有机相)VOA2(有机相)+2H+正向移动,对VO2+萃取效果不好。(4)“萃取”与“反萃取”是为了使VO2+进入有机相,与其他金属离子分离开,均需使用的仪器是分液漏斗。每进行一次,VO2+萃取率为90%,溶液中残留的VO2+为10%,故残留的。(5)(NH4)2V6O16煅烧产生NH3和V2O5,化学反应方程式为(NH4)2V6O162NH3↑+3V2O5+H2O。
2.(2025·山东省实验中学·一模)以铂钯精矿(含Se、Te、Au、Pt、Pd等)为原料,提取贵金属Au、Pt、Pd的工艺流程如图所示:
已知:①“氯化浸出”时,Au、Pt、Pd以AuCl、PtCl、PdCl形式存在;
②(NH4)2PtCl6和(NH4)2PdCl6难溶于水,(NH4)2PtCl4易溶于水;
③室温:Ksp[(NH4)2PtCl6]=5.7×10-6;571/2≈7.5。
(1)“焙烧”时,Se、Te转化为可溶于水的Na2SeO3和Na2TeO4.转化等物质的量的Se、Te时,消耗NaClO3的物质的量之比为 ;根据下图判断“焙烧”适宜的温度范围是 (填标号)。
A.300-350K B.350-400K C.400-450K D.450-500K
(2)一般条件下Au很难被Cl2氧化,但用浓盐酸作浸出液,可使Au被Cl2氧化,由此分析“氯化浸出”过程中浓盐酸的作用为 。
(3)“还原”得到金的离子方程式为 ;加入过量SO2的目的是 。
(4)“煅烧”时还生成N2、NH4Cl和一种气体,该气体用少量水吸收后可重复用于“ ”操作单元。
(5)“沉铂”先通入的气体X为 (填化学式)。“沉铂”中,若向c(PtCl)=0.125ml/L的溶液里加入等体积的NH4Cl溶液,使PtCl沉淀完全,则NH4Cl溶液浓度最小值为 ml/L(结果保留两位小数,忽略溶液混合后体积的变化)。
【答案】(1)2:3 B
(2)Cl-做配体,与金离子形成稳定的配合物,提高Au的还原性,将Au转化为,从而浸出Au
(3)2+3SO2+6H2O=2Au+8Cl-+3+12H+ 将全部转化为Au,将还原为
(4)氯化浸出
(5)Cl2 1.75
【分析】将铂钯精矿、碳酸钠、氯酸钠混合焙烧,将硒、碲转化为Na2SeO3和Na2TeO4,加水水浸、过滤得到含有Na2SeO3和Na2TeO4的滤液和滤渣;向滤渣中加入浓盐酸,通入氯气氯化浸出,将Au、Pt、Pd转化为、、,过滤得到滤渣和滤液;向滤液中通入过量二氧化硫,将溶液中的四氯合金酸根离子转化为金、六氯合铂酸根离子转化为四氯合铂酸根离子,过滤得到金和滤液;向滤液中加入氯化铵沉钯,将溶液中的六氯合钯酸根离子转化为六氯合钯酸铵沉淀,过滤得到六氯合钯酸铵和滤液;六氯合钯酸铵煅烧分解得到钯;向滤液中通入氯气,将溶液中的四氯合铂酸根离子转化为六氯合铂酸根离子,加入氯化铵沉铂,将溶液中的六氯合铂酸铵沉淀,过滤得到尾液和六氯合铂酸铵;六氯合铂酸铵经铂精炼得到铂。
【解析】(1)由得失电子数目守恒可知,硒、碲转化为Na2SeO3和Na2TeO4时,硒、碲化合价分别升高到+4价和+6价,则消耗氧化剂氯酸钠的物质的量比为4:6=2:3;由图可知,温度为350—400K时,硒、碲脱除率最高,所以“焙烧”适宜的条件为温度为350—400K,故答案为:2:3;温度为350—400K;
(2)一般条件下Au很难被Cl2氧化,用浓盐酸作浸出液,盐酸电离出的Cl-做配体,与金离子形成稳定的配合物,提高Au的还原性,将Au转化为,从而浸出Au;
(3)由分析可知,通入过量二氧化硫的目的是将溶液中的四氯合金酸根离子转化为金、六氯合铂酸根离子转化为四氯合铂酸根离子,得到金的反应的离子方程式为2+3SO2+6H2O=2Au+8Cl-+3+12H+;
(4)由图可知,六氯合钯酸铵煅烧分解得到钯、氮气、氯化铵和氯化氢,反应生成的氯化氢可以重复用于氯化浸出操作单元;
(5)由分析可知,沉铂时先通入气体氯气,目的是将溶液中的四氯合铂酸根离子转化为六氯合铂酸根离子,故答案为:Cl2;
(NH4)2PdCl62+,Ksp[(NH4)2PtCl6]=5.7×10-6,沉淀完全时浓度小于1×10-5ml/L,代入数据可得c()=,设原溶液体积为VL,则沉淀需要溶液的物质的量为2V×0.125,溶液等体积混合后,c()=,则加入溶液的浓度最小为;
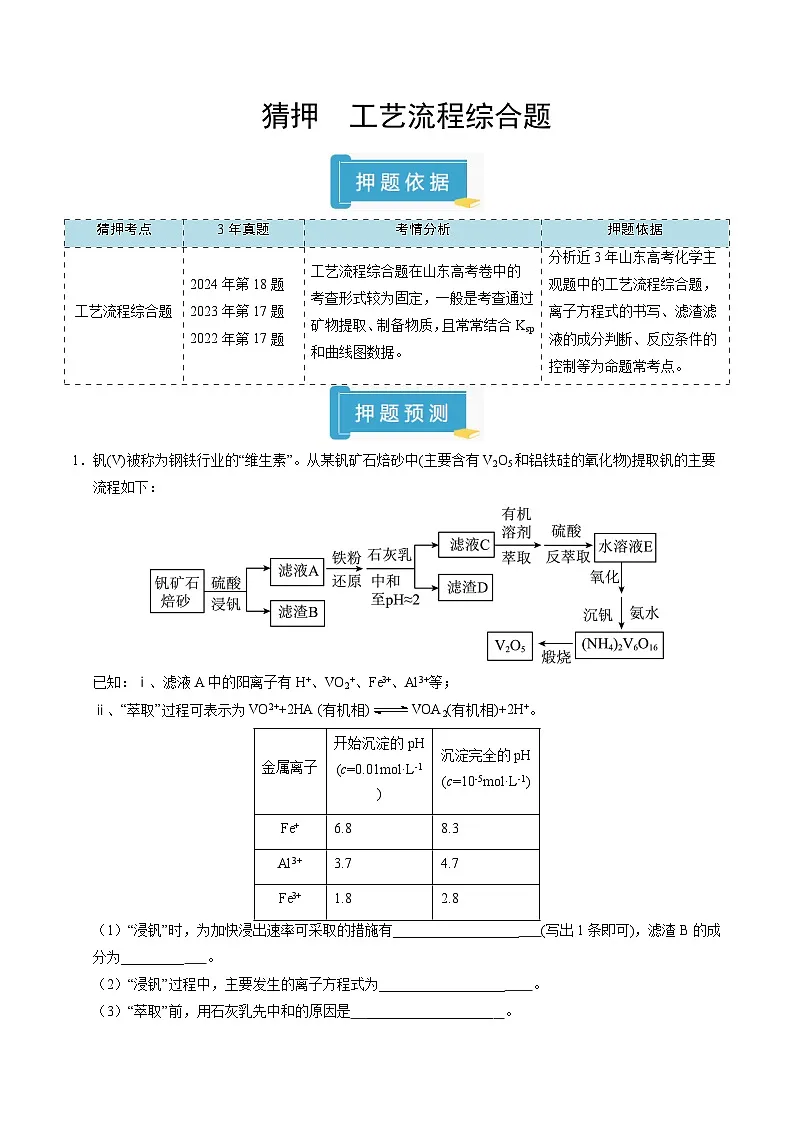
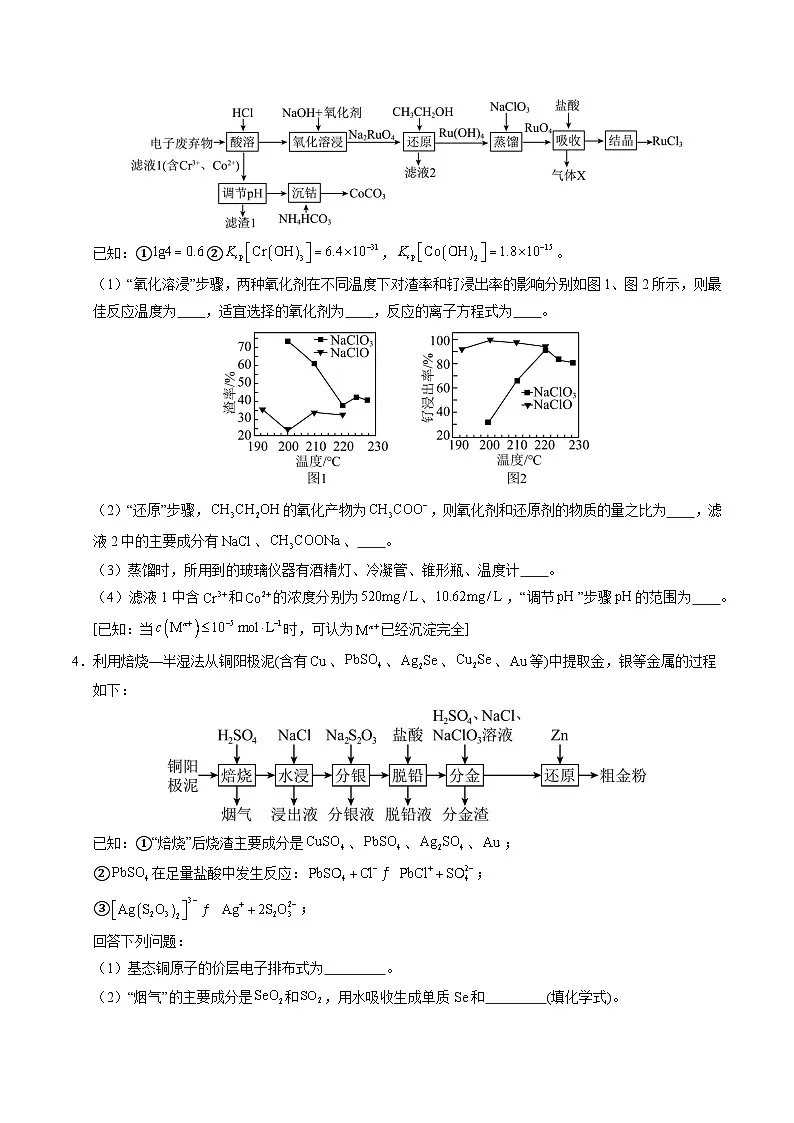
3.(2025·山东聊城·一模)铂族金属钌(Ru)广泛用于航天航空、石油化学、信息传感工业、制药等高科技领域。以下工艺实现了电子废弃物中铂族金属钌(Ru)的回收利用,电子废弃物主要成分为Ru、C、Cr、Si等物质。
已知:①②,。
(1)“氧化溶浸”步骤,两种氧化剂在不同温度下对渣率和钌浸出率的影响分别如图1、图2所示,则最佳反应温度为 ,适宜选择的氧化剂为 ,反应的离子方程式为 。
(2)“还原”步骤,的氧化产物为,则氧化剂和还原剂的物质的量之比为 ,滤液2中的主要成分有、、 。
(3)蒸馏时,所用到的玻璃仪器有酒精灯、冷凝管、锥形瓶、温度计 。
(4)滤液1中含和的浓度分别为、,“调节”步骤的范围为 。[已知:当时,可认为已经沉淀完全]
【答案】(1)200C NaClO Ru+2OH-+3ClO-=+3Cl-+H2O
(2)2:1 Na2SiO3
(3)蒸馏烧瓶和牛角管
(4)5.6≤pH
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 







.png)


