

2023~2024学年福建省宁德市九年级上学期期末教学质量检测化学试卷(解析版)
展开
这是一份2023~2024学年福建省宁德市九年级上学期期末教学质量检测化学试卷(解析版),共17页。试卷主要包含了在本卷上作答无效等内容,欢迎下载使用。
考生注意:1.选择题用2B铅笔在答题卡选择题的答题区域内填涂答案
2.非选择题用黑色签字笔在答题卡各题指定的答题区域内作答
3.在本卷上作答无效
可能用到的相对原子质量:H1 C12 O16 K39
第Ⅰ卷选择题
第Ⅰ卷共10小题,每小题3分,共30分。每小题只有一个正确的选项,请将正确选项涂入答题卡中。
1. 福安坦洋功夫红茶,历史悠久,驰名中外。制茶包含如下过程,其中发生化学变化的是( )
A. 鲜叶采摘B. 萎凋揉捻
C. 发酵初焙D. 拼配筛分
【答案】C
【解析】
【详解】A、采摘鲜叶过程中,没有新物质生成,属于物理变化,该选项不符合题意;
B、萎凋揉捻过程中,没有新物质生成,属于物理变化,该选项不符合题意;
C、发酵过程中,有新物质生成,属于化学变化,该选项符合题意;
D、拼配筛分过程中,没有新物质生成,属于物理变化,该选项不符合题意。
故选C。
2. 化学用语是学习化学的必备工具。下列化学用语表达正确的是( )
A. 氧化铝:A1OB. 正二价的镁元素:Mg+2
C. 2个氧原子:O2D. 氯离子Cl-
【答案】D
【解析】
【详解】A、化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零,化合价数值约到最简交叉写在元素右下角。氧化铝中铝元素显+3价,氧元素显-2价,其化学式为Al2O3,故A错误;
B、元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,数值为1时,不能省略。+2价镁元素表示为,故B错误;
C、原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字。2个氧原子表示为2O,故C错误;
D、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字。氯离子表示为Cl-,故D正确;
故选:D。
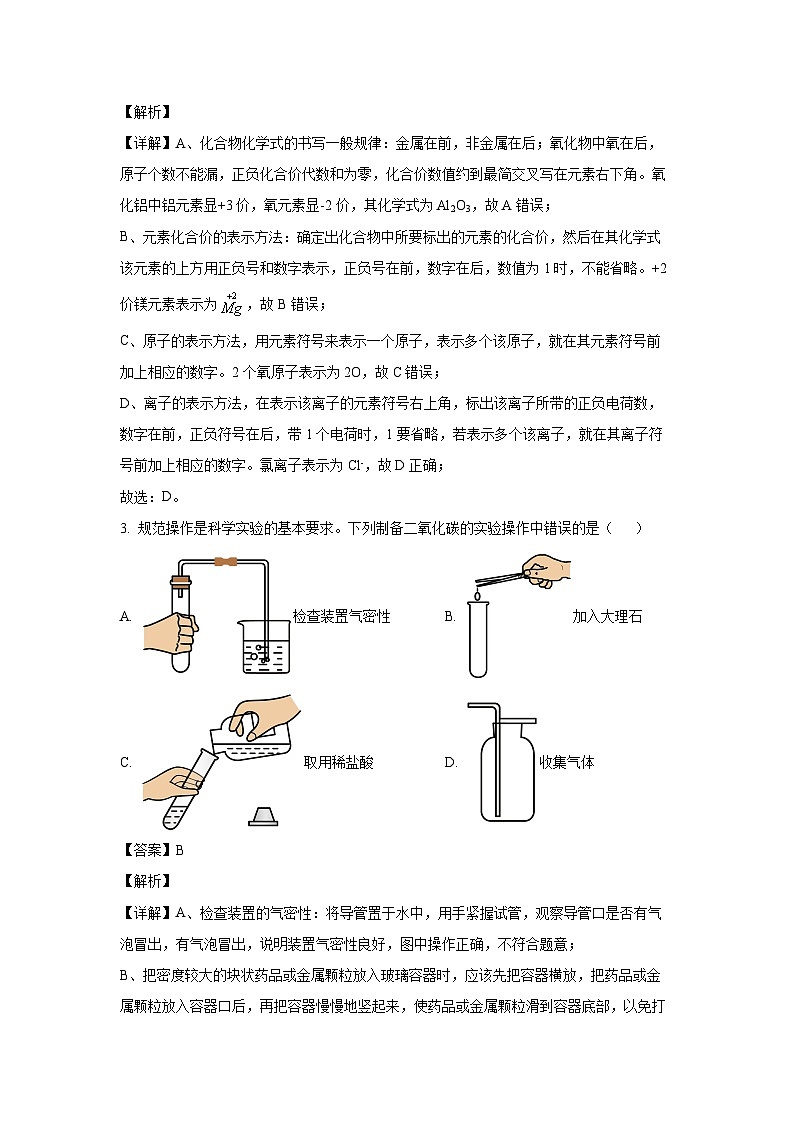
3. 规范操作是科学实验的基本要求。下列制备二氧化碳的实验操作中错误的是( )
A. 检查装置气密性B. 加入大理石
C. 取用稀盐酸D. 收集气体
【答案】B
【解析】
【详解】A、检查装置的气密性:将导管置于水中,用手紧握试管,观察导管口是否有气泡冒出,有气泡冒出,说明装置气密性良好,图中操作正确,不符合题意;
B、把密度较大的块状药品或金属颗粒放入玻璃容器时,应该先把容器横放,把药品或金属颗粒放入容器口后,再把容器慢慢地竖起来,使药品或金属颗粒滑到容器底部,以免打破容器,图中操作错误,符合题意;
C、倾倒液体时,瓶塞应倒放,瓶口应紧挨试管口,标签应朝向手心处,图中操作正确,不符合题意;
D、二氧化碳溶于水,密度比空气大,可用向上排空气法收集,不符合题意。
故选B。
4. 化学观念和科学思维是化学学科核心素养的重要内容。下列认识正确的是( )
A. 分类观念:高锰酸钾、二氧化锰、氧气都属于氧化物
B. 守恒观念:200g乙醇+200g水,总质量等于400g,符合质量守恒定律
C. 宏微结合:CO和CO2的分子构成不同,化学性质不同
D. 证据推理:金刚石和石墨都由碳元素组成,它们的性质相同
【答案】C
【解析】
【详解】A、高锰酸钾由锰、钾、氧元素组成,不属于氧化物,二氧化锰由锰、氧元素组成,属于氧化物,氧气由氧元素组成,属于单质,故选项错误;
B、200g乙醇+200g水,总质量等于400g,没有发生化学反应,不符合质量守恒定律,故选项错误;
C、CO和CO2的分子构成不同,因此化学性质不同,故选项正确;
D、金刚石和石墨都由碳元素组成,但是它们的物理性质不同,因为其碳原子的排列方式不同,故选项错误。
故选:C
5. 日前,中国商务部和海关总署发布公告,宣布限制镓锗两种战略性金属元素的出口。锗元素的元素符号为Ge,原子核外电子数为32,中子数为41,相对原子质量为72.64.甲图是镓元素的信息图,请模仿甲图,乙图的①处应填( )
A 41B. 72.64C. 32D. 40.64
【答案】C
【解析】
【详解】由元素周期表中的一格可知,①处左上角的数字表示原子序数,在原子中,原子序数=质子数=核外电子数,锗元素的元素符号为Ge,原子核外电子数为32,故锗运输的原子序数为32,故①处应填32;
故选:C。
6. 下图是以氧气为例形成的多角度认识物质思路和方法的示意图。下列说法中错误的是( )
A. 从组成角度:氧气由氧元素组成的单质
B. 从转化角度:
C. 从性质角度:氧气有助燃性可使燃着木条烧得更旺
D. 从应用角度:氧气可用于医疗急救、航空航天
【答案】B
【解析】
【详解】A、氧气是由氧元素组成的纯净物,属于单质,不符合题意;
B、氢气能与氧气在点燃的条件下反应生成水,该反应的化学方程式为:,符合题意;
C、氧气具有助燃性,能使燃着的木条燃烧的更旺,不符合题意;
D、氧气具有氧化性,能供给呼吸,可用于医疗急救,氧气具有助燃性,可用于航空航天,不符合题意。
故选B。
7. 为达到实验目的,后者所选的试剂或方法不正确的是( )
A. 测定空气中氧气的含量:用木炭代替红磷进行实验
B. 高锰酸钾制取氧气时防止冷凝水倒流使试管炸裂:试管口略向下倾斜
C 鉴别双氧水和蒸馏水:二氧化锰
D. 比较人体吸入气体和呼出气体中氧气的含量:燃着的木条
【答案】A
【解析】
【详解】A、木炭燃烧生成二氧化碳气体,装置中的压强几乎不变,则不能用于验证质量守恒定律,该选项不正确;
B、加热高锰酸钾时,为了防止冷凝水倒流,试管口应略向下倾斜,该选项正确;
C、双氧水在二氧化锰催化作用下生成水和氧气,则能鉴别,该选项正确;
D、氧气具有助燃性,燃着的木条在吸入气体中正常燃烧,但在呼出气体中很快熄灭,说明吸入气体中氧气含量较高,该选项正确。
故选A。
8. 过氧化氢可用于消毒杀菌,具有不稳定性。水蒸气在硅材料表面冷凝,部分水分子会转化为过氧化氢分子。过氧化氢的浓度随温度变化关系如图所示,下列说法错误的是( )
A. 过氧化氢能消毒杀菌体现了它的化学性质
B. 过氧化氢不稳定是因为过氧化氢易分解
C. 水蒸气随温度升高在硅材料表面冷凝产生过氧化氢的量增加。
D. 图中a点(-2.8℃)未生成过氧化氢的原因可能是温度过低,水蒸气冷凝后直接凝固为固体
【答案】C
【解析】
【详解】A、消毒杀菌过程中有新物质生成,属于化学变化,则该性质需要在化学反应中才能体现,属于化学性质,选项正确;
B、过氧化氢不稳定是因为过氧化氢易分解产生氧气和水,选项正确;
C、由图可知,温度在2.8℃至4℃之间温度升高在硅材料表面冷凝产生过氧化氢的量增加,温度在4℃至12℃之间温度升高在硅材料表面冷凝产生过氧化氢的量减小,选项错误;
D、水的凝固点为0℃,则a点没有生成过氧化氢的原因可能为:温度过低,水蒸气冷凝后直接凝固成冰,选项正确。
故选C。
9. 在密闭容器内,有甲、乙、丙、丁四种物质,在一定条件下充分混合反应一段时间,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
A. 甲一定是化合物B. 乙可能是生成物
C. 丙一定是单质D. 丁一定是催化剂
【答案】A
【解析】
【分析】由反应前后各物质的质量分数可知,甲质量分数减少,为反应物,乙质量分数增加,为生成物,丙质量分数增加,为生成物,丁质量分数不变,可能为催化剂或没有参加反应,反应为甲生成乙和丙。
【详解】A、反应为甲生成乙和丙,甲一定是化合物,故A正确;
B、乙质量分数增加,为生成物,故B不正确;
C、丙质量分数增加,为生成物,丙不一定是单质,故C不正确;
D、丁质量分数不变,可能为催化剂或没有参加反应,故D不正确。
故选A。
10. 近代科学家利用铁的氧化物捕捉CO2的流程如图所示,下列说法错误的是( )
A. 该流程中可循环利用的物质是FeOB. 若A为黑色固体则A为铁粉
C. 该流程可以缓解温室效应D. 该流程有涉及分解反应
【答案】B
【解析】
【详解】A、由图可知,FeO既是反应物又是生成物,可循环利用,故A说法正确;
B、若A为黑色固体,根据质量守恒定律,化学反应前后元素种类不变,反应物中含有碳、氧、铁元素,生成物Fe3O4中含有铁元素和氧元素,则A中一定含有碳元素,不可能是铁粉,故B说法错误;
C、该流程有效利用二氧化碳气体,可缓解温室效应,故C说法正确;
D、Fe3O4在太阳能和≥2300K条件下可生成FeO和O2,该反应符合“一变多”的特点,属于分解反应,故D说法正确;
故选:B。
第Ⅱ卷非选择题(共70分)
第Ⅱ卷共8题,共70分。
11. “故人具鸡黍,邀我至田家”。宁德某校初三学生开展古村落研学活动。
(1)古村古道。古道是由花岗岩石铺就,其化学成分如下表:
花岗岩石中一共含有______种金属元素,它属于______(“纯净物”或“混合物”)
(2)古厝民居。民居的夯土墙由黏土、砂石和生石灰(氧化钙)按一定比例夯筑而成。写出石灰石(碳酸钙)高温煅烧生产生石灰的化学方程式______。
(3)柴火土灶。如图为柴火灶的示意图,土灶的通风口和烟囱形成气体对流,提供了充足_____。
【答案】(1)①. 5##五 ②. 混合物
(2)
(3)氧气##空气
【解析】(1)根据表格可知,花岗岩石中含有SiO2、Al2O3、K2O、Na2O、CaO、FeO、Fe2O3等,含有钠、钾、铝、铁、钙5种金属元素,由多种物质组成,属于混合物;
(2)碳酸钙在高温条件下分解生成氧化钙和二氧化碳,反应的化学方程式为:;
(3)土灶的通风口和烟囱形成气体对流,提供了充足充足的氧气或氧气,有利于燃料充分燃烧。
12. 水乃万物之源。学习小组开展对水的探究活动。
活动1:淡水的水质检测
(1)明清时期的水井井底和井壁用石块铺好,上方铺一层竹炭,最后在竹炭外围再铺好石块。其竹炭的作用_____;生活中采用____进行硬水软化。
(2)为完成“水质检测”实践性作业,学习小组买了不同型号的滤纸开展活动。根据资料回答问题:
表一
表二
根据上表信息,若要过滤掉泥砂,应选用滤纸型号为___;分析表二数据,你能得出的信息是____;过滤后的淡水能否直接饮用____(填“能”或“不能”)。
活动2:学习小组利用下图装置探究添加不同浓度NaOH溶液对电解水的影响,数据如下表所示(相同时间内):
(3)a管内产生的气体化学式_____,检验b管内气体的方法(步骤、现象和结论)_____。
(4)由表可知:当-NaOH溶液的质量分数为____%时,氢气、氧气体积比最不接近理论值,实验效果最差。
【答案】(1)①. 吸附 ②. 煮沸
(2)①. 204 ②. 孔径越小滤速越慢等 ③. 不能
(3)①. H2 ②. 将带火星的木条靠近b管导管口,打开旋塞(开关),木条复燃则为氧气
(4)10
【解析】(1)竹炭的结构疏松多孔,具有吸附性,能除去色素和异味,生活中常用煮沸的方法价降低水的硬度,故填:吸附、煮沸;
(2)泥砂的直径大于10微米,若要过滤掉泥沙,则所选滤纸的直径应比10微米小,故选204型号滤纸,其直径小于10微米,比泥沙直径小,能过滤掉泥沙,由表二可知,孔径直径越小,过滤所需时间越长,速度越慢,过滤除去了难溶性杂质,仍有可溶性杂质和细菌病毒等溶在水中,不能直接饮用,故填:204、孔径越小滤速越慢等、不能;
(3)电解水实验中,根据“正氧负氢、氧一氢二”,b管与电源的正极相连,产生的是氧气,a管与电源的负极相连,产生的是氢气,化学式为H2,氧气具有助燃性,将带火星的木条靠近b管导管口,打开旋塞,木条复燃则为氧气,故填:H2、将带火星的木条靠近b管导管口,打开旋塞,木条复燃则为氧气;
(4)电解水实验中,氢气和氧气的体积比约为2:1,当NaOH溶液的质量分数为10%时,氢气的体积:氧气的体积=5:2.1≈2.38:1,当NaOH溶液的质量分数为12%时,氢气的体积:氧气的体积=6.2:3.2≈1.94:1,当NaOH溶液的质量分数为14%时,氢气的体积:氧气的体积=7.5:3.7≈2:1,当NaOH溶液的质量分数为16%时,氢气的体积:氧气的体积=8.2:4.3≈1.91:1,计算可知,当NaOH溶液的质量分数为10%时,氢气、氧气体积比最不接近理论值,实验效果最差,故填:10。
13. 二氧化碳是一种与人类生产生活密切关系的气体。
(1)下图是自然界中部分碳、氧循环图(X为H2CO3;Y为葡萄糖C6H12O6)。
①转化2的化学反应类型为______,绿色植物通过光合作用,将太阳能转化为______能。
②转化2和转化3反应物相同但生成物不同的原因是______。
(2)我国科学家在二氧化碳电催化还原研究方面取得新进展,实现了二氧化碳电催化还原高效制备乙烯(C2H4)等化学产品,为二氧化碳资源化利用提供了新思路。(下列图分别为反应微观过程,“几何分电流密度”,其大小用来表征催化剂性能的优劣。)
①请根据上述图示写出催化反应过程的化学方程式_______。
②二氧化碳电催化还原高效制备乙烯选用Cu-CuI复合催化剂的原因是_______。
【答案】(1)①. 化合反应 ②. 化学 ③. 化学反应条件不同
(2)①. ②. Cu-CuI复合催化剂性能最优
【解析】(1)①转化2是二氧化碳和水反应生成碳酸,化学反应的基本反应类型为化合反应;绿色植物通过光合作用,将太阳能转化为化学能。故填:化合反应;化学。
②转化2是二氧化碳和水在常温常压下反应生成碳酸,转化3是二氧化碳和水在光照和叶绿素条件下反应生成葡萄糖和氧气,所以转化2和转化3反应物相同但生成物不同的原因是:化学反应条件不同。故填:化学反应条件不同。
(2)①由反应微观图可知,二氧化碳和水在Cu-CuI复合催化剂条件下反应生成乙烯和氧气,该反应化学方程式为:。故填:。
②由图可知,二氧化碳电催化还原高效制备乙烯选用Cu-CuI复合催化剂的原因是催化剂性能最优。故填:Cu-CuI复合催化剂性能最优。
14. 火炬燃料变迁的背后是一场能源革命。1936年柏林奥运会起,火炬燃料随着科技的发展一直在不断变迁。
(1)镁粉燃烧生成的氧化镁化学式为___________。
(2)液化石油气加压后贮存在钢瓶中,从微观角度说明原因___________。
(3)丙烷(C3H8)中碳、氢元素的质量比为___________。
(4)上述火炬燃料中最清洁环保的燃料是___________。
(5)我国体育大赛火炬燃料经历了以下三个阶段,这与我国实施的低碳战略相吻合。
每生产一吨甲醇可以吸收1.375吨的CO2,这一项成果有何意义是___________。
【答案】(1)MgO
(2)分子间隔变小
(3)9:2
(4)氢气##H2
(5)实现二氧化碳的资源化利用和废碳利用等
【解析】(1)镁粉燃烧生成的氧化镁,氧化镁的化学式为:MgO;
(2)液化石油气加压后贮存在钢瓶中,是因为分子间有间隔,气体受压后,分子间的间隔变小;
(3)丙烷(C3H8)中碳、氢元素的质量比为(12×3):(1×8)=9:2;
(4)镁粉燃烧生成氧化镁,液化石油气燃烧生成二氧化碳和水,丙烷丁烷燃烧生成二氧化碳和水,氢气燃烧生成水,甲醇燃烧生成水和二氧化碳,因此火炬燃料中最清洁环保的燃料是氢气;
(5)每生产一吨甲醇可以吸收1.375吨的CO2,能消耗二氧化碳,该项成果能实现二氧化碳的资源化利用和废碳利用等。
15. 铜是一种重要金属。实践小组开展“了解铜、回收铜”项目式学习。
活动一:了解古代火法炼铜,感受我国劳动人民智慧。
【查阅资料】:1 铜生锈表面形成铜绿,其成分是。
2 古籍《大冶赋》中记载火法炼铜技术,其生产流程如下:
(1)煅烧孔雀石可观察到的现象是___________。
(2)写出木炭还原氧化铜的化学方程式___________。
活动二:开展从回收的废旧铜料中提取铜实践活动,其流程如下:
(3)写出步骤③中化学方程式___________。
(4)请补充完善由固体Y得到铜粉的实验方案:向固体Y中加入___________(填试剂名称),经过过滤、洗涤、干燥得到铜粉。
【答案】(1)绿色固体变成黑色
(2)
(3)
(4)稀盐酸或稀硫酸等
【解析】(1)孔雀石的主要成分是Cu2(OH)2CO3,铜绿煅烧生成氧化铜、水和二氧化碳,氧化铜为褐色,因此煅烧孔雀石可观察到的现象是绿色固体变成黑色;
(2)木炭和氧化铜在高温下反应生成铜和二氧化碳,反应的化学方程式为:;
(3)根据流程图可知,铜在空气中灼烧反应生成氧化铜,氧化铜酸浸,氧化铜和硫酸反应生成硫酸铜和水,步骤③反应生成固体Y和硫酸锌,固体Y最后进过反应得到铜,因此步骤③中加入过量的固体是锌,锌和硫酸铜反应生成铜和硫酸锌,反应的化学方程式为:;
(4)固体Y中含有铜和过量的锌,锌和稀盐酸或稀硫酸能反应生成氢气,从而除去锌,经过过滤、洗涤、干燥能得到铜粉。
16. 青少年吸烟会致使气管内分泌物增多,导致慢性阻塞性肺部疾病。课外实践小组对烟丝燃烧是否产生一氧化碳进行初步探究。
【查阅资料】新鲜的血液遇一氧化碳由鲜红变为暗红。
(1)写出实验室制取氧气的化学方程式______。
(2)实验开始后,D装置中新鲜的鸡血变为暗红色,说明烟丝一定含有______元素。
(3)B装置中产生白色沉淀,发生反应的化学方程式为_____。
(4)课外实践小组同学设计的这套装置不足之处是______,请你设计解决的方法______。
(5)烟叶对人体有麻醉和镇痛作用,但吸烟有害健康。从物质用途的角度,你认为理性处理这类物质的方法是______。
【答案】(1)######
(2)碳
(3)
(4)①. 未进行尾气处理 ②. 在D装置导管口放置一盏燃着酒精灯
(5)青少年不宜吸烟或拒绝吸二手烟
【解析】(1)实验室制取氧气可以选用氯酸钾和二氧化锰的混合物、过氧化氢溶液和二氧化锰的混合物或高锰酸钾,方程式为:、、;
(2)D装置中新鲜的鸡血变为暗红色,说明烟丝燃烧产生了一氧化碳,氧气只能提供氧元素,根据反应前后元素种类不变可知,烟丝中一定含有碳元素;
(3)B装置中产生白色沉淀,是产生的二氧化碳与石灰水中的氢氧化钙反应生成了碳酸钙和水,方程式为:;
(4)实验过程中有一氧化碳排出,一氧化碳有毒,会污染空气,故应有尾气处理装置;一氧化碳具有可燃性,可以在D装置导管口放置一盏燃着酒精灯,将一氧化碳点燃;
(5)吸烟有害健康因此青少年不宜吸烟或拒绝吸二手烟
17. 硫是一种常见的非金属元素,其化合价与物质类别之间的关系如图。
【查阅资料】1 SO2:熔点-72℃,沸点:-10℃;SO3熔点:16.8℃,沸点:44.8℃
2 同温同压下,气体体积比等于分子个数比
【提出问题】硫与足量的O2反应是否生成:SO3?
【猜想与假设】
猜想1:硫与足量的O2反应会生成SO3
猜想2:硫与足量的O2反应不会直接生成SO3。
(1)从图的“价类”二维图中,SO2和SO3对应的点是_____、____(选填“A、B、C、D、E”)。
(2)从碳与氧气反应的角度,阐述猜想1的合理性______。
【实验验证】
取0.1g硫粉放入500mL圆底烧瓶中(保证氧气充足且容器压强在安全值内),实验装置如图1。加热,用传感器测得烧瓶内压强的变化,测得数据如图2。
(3)本实验取得成功的关键操作是______。
(4)图2中加热至B点(硫即将完全气化)熄灭酒精灯,到C点时间压强达到峰值,可判断该反应是_____(选填“吸热”或“放热”)反应。
(5)通过图2数据分析,可认为没有SO3产生,其依据是______。
(6)写出硫在氧气中燃烧的化学方程式_______。
【拓展延伸】
(7)空气中的SO2在粉尘等催化作用下生成SO3,SO3与雨水结合形成酸雨,写出SO2转化为SO3的化学方程式______。
【答案】(1)①. B ②. C
(2)碳与氧气在不同条件下可生成不同的氧化物,所以猜想1合理
(3)检查装置气密性
(4)放热
(5)反应前后密闭容器中气压不变
(6)
(7)
【解析】(1)二氧化硫和三氧化硫均为氧化物,设二氧化硫中硫元素化合价为x,根据“化合物中各元素化合价代数和为零”,则x+(-2)×2=0,解得x=+4,同理可知三氧化硫中硫元素化合价为+6价,则二氧化硫和三氧化硫对应的点分别为B、C。
(2)碳充分燃烧时生成二氧化碳,不充分燃烧时生成一氧化碳,即碳与氧气在不同条件下可生成不同的氧化物,则硫在氧气充足时可能生成三氧化硫。
(3)本实验要测定装置内的压强变化,则装置气密性必须良好,即实验前一定要进行气密性的检查。
(4)停止加热后,温度还在升高,说明该反应放热。
(5)由图可知,反应前后压强不变,若生成三氧化硫,常温时三氧化硫为液体,则冷却至常温后,压强应减小,则说明没有三氧化硫产生。
(6)硫燃烧生成二氧化硫,反应的化学方程式为:。
(7)SO2在粉尘等催化作用下和氧气反应生成SO3,反应的化学方程式为:。
18. 某品牌化学供氧自救器生氧罐中产生氧气的反应原理为:。若要生成48g氧气,需要称取多少克的KO2?
【答案】解:设需要称取KO2的质量为x。
x=142g
答:需要称取KO2质量为142g。
【解析】
【详解】见答案。
组成成分
SiO2
Al2O3
K2O
Na2O
CaO
FeO
Fe2O3
质量分数
72.04%
14.42%
4.12%
3.69%
1.82%
1.68%
1.22%
杂质类别
颗粒直径
悬浮物质
大于0.1微米
泥砂
粘土
藻类、细菌
部分病毒
大于10微米
0.1微米~2微米
约0.2微米
最小的病毒0.01微米
胶体颗粒
0.1~0.001微米
主要是含铁元素、铝元素和硅元素的化合物,动植物的肢体腐烂和分解而生成的腐殖物。
滤纸型号
孔径/微米
波速/秒
201
20-25
相关试卷
这是一份福建省宁德市蕉城区宁德市第一中学2023-2024学年九年级上学期开学化学试题(解析版),共20页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份福建省宁德市2023-2024学年九年级上学期期末质量检测化学试卷(含答案),共17页。试卷主要包含了单选题,填空题,实验题,计算题等内容,欢迎下载使用。
这是一份37,福建省宁德市2023-2024学年九年级上学期期末考模拟化学试卷,共7页。








