







所属成套资源:初中化学九年级下册同步教学课件+同步练习(沪教版2024)
化学九年级下册(2024)基础实验8 常见酸、碱的化学性质优质教学ppt课件
展开
这是一份化学九年级下册(2024)基础实验8 常见酸、碱的化学性质优质教学ppt课件,文件包含基础实验8常见酸碱的化学性质-初中化学九年级下册同步教学课件沪教版2024pptx、基础实验8常见酸碱的化学性质练习含答案解析docx、基础实验8常见酸碱的化学性质练习docx等3份课件配套教学资源,其中PPT共21页, 欢迎下载使用。
学会使用酸碱指示剂与pH试纸检测溶液酸碱性的基本方法和实验操作。
通过探究,认识酸碱中和反应。
比较常见酸的化学性质,认识其特征。
认识常见碱的一些化学性质。
稀盐酸、稀硫酸、稀氢氧化钠溶液、石灰水、镁条、铝片、铜片、碳酸钠粉末、石灰石(或大理石)、生锈铁钉、硫酸铜溶液、石蕊溶液、酚酞溶液、pH试纸、蒸馏水等;
点滴板、表面皿、试管、烧杯、胶头滴管、玻璃棒等。
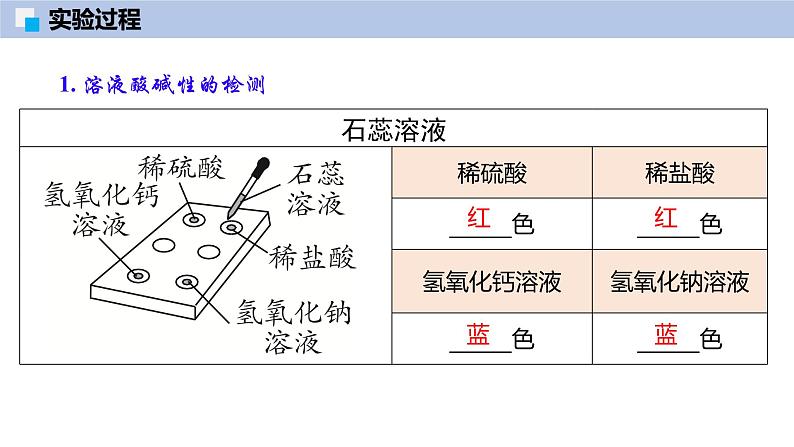
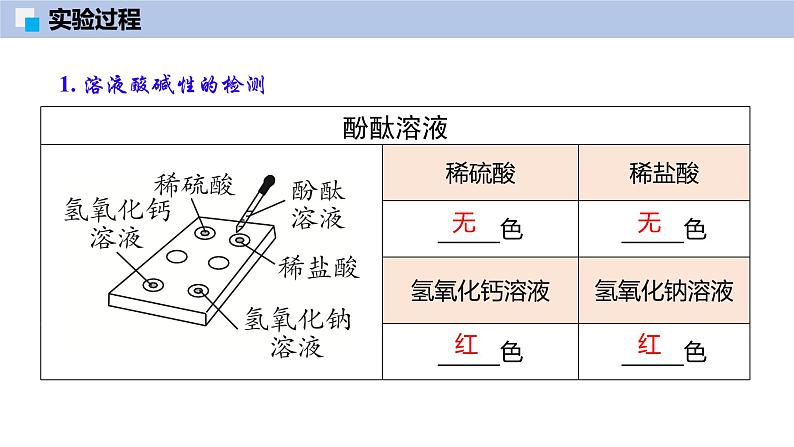
1. 溶液酸碱性的检测
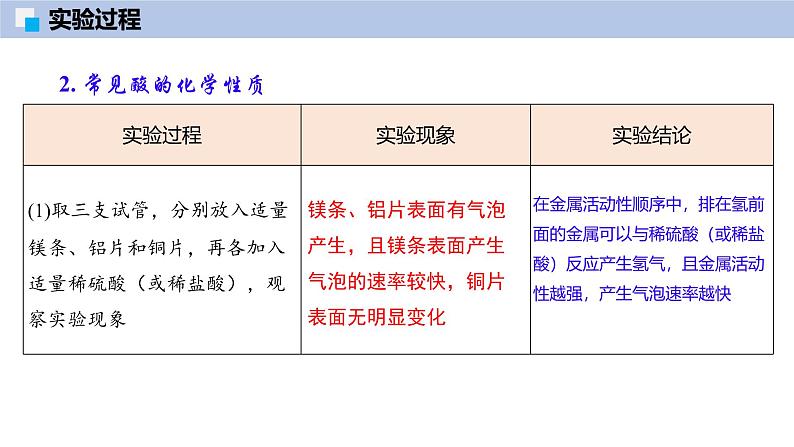
镁条、铝片表面有气泡产生,且镁条表面产生气泡的速率较快,铜片表面无明显变化
在金属活动性顺序中,排在氢前面的金属可以与稀硫酸(或稀盐酸)反应产生氢气,且金属活动性越强,产生气泡速率越快
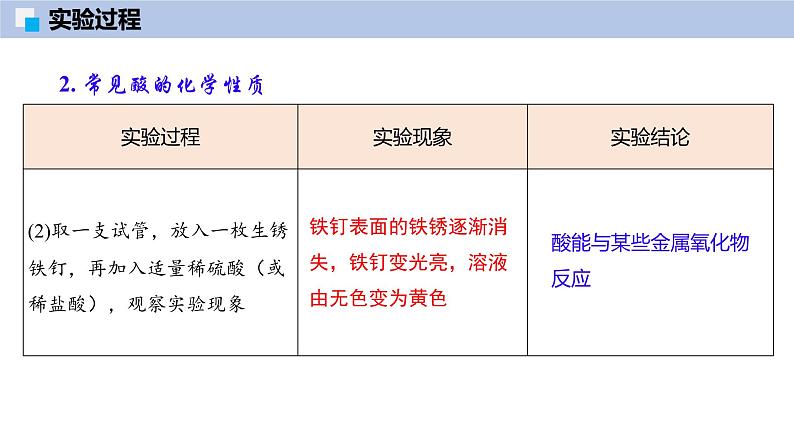
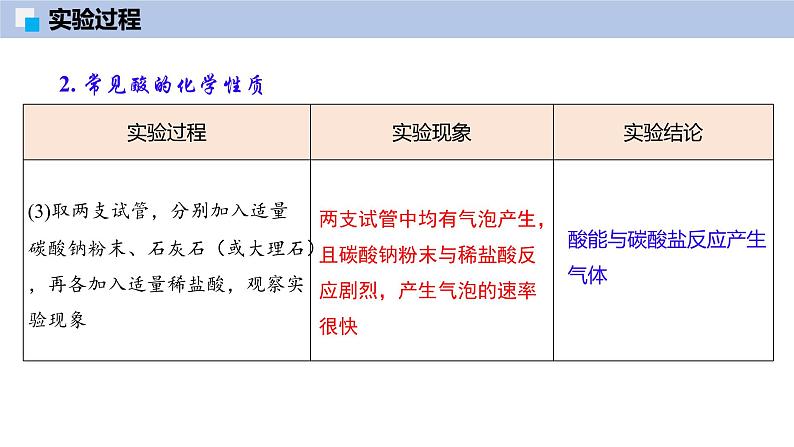
2. 常见酸的化学性质
铁钉表面的铁锈逐渐消失,铁钉变光亮,溶液由无色变为黄色
酸能与某些金属氧化物反应
两支试管中均有气泡产生,且碳酸钠粉末与稀盐酸反应剧烈,产生气泡的速率很快
酸能与碳酸盐反应产生气体
碱能与某些盐溶液发生反应
2. 常见碱的化学性质
碱溶液能使酚酞溶液变红
溶液由红色变为无色,溶液温度上升
酸碱恰好完全反应,中和反应是放热反应
氢氧化钠过量,此时溶液显碱性
1. 用稀酸除去铁制品表面的铁锈,是否能将铁制品长期浸泡在酸溶液中?为什么?写出相关的化学方程式?
不能。若将铁制品长期浸泡在酸溶液中,铁锈与酸反应后,铁会继续与酸反应,损坏铁制品。
Fe2O3 + 6HCl == 2FeCl3 + 3H2O
Fe + 2HCl == FeCl2 + H2↑
2. 根据实验现象说明,在实验室中常用稀盐酸和大理石反应来制取CO2气体的原因。
大理石价格低廉,稀盐酸和大理石反应能持续地产生CO2气体,且速率适中便于收集;而碳酸钠与酸溶液反应速率过快,不便于气体的收集。
3. 酸碱中和反应实验中,步骤(3)的目的是什么?
目的是验证酸、碱是否恰好完全反应。
1. 下列物质中能使石蕊试液变红的是( )A.石灰水B.食盐水 C.白醋 D.酒精
2. 室温下,维生素C的水溶液能使紫色石蕊试液变红。其水溶液的酸碱性是( )A.酸性 B.中性 C.碱性 D.无法判断
3. 炎炎夏日,各色饮料能够帮助人们降温解暑。常温下,下列饮料呈碱性的是( )A.纯净水(pH≈7) B.苏打水 (pH≈9)C.柠檬水 (pH≈3) D.椰子水 (pH≈5)
4. 盐酸常用于除铁锈,但铁制品不宜在盐酸中长时间浸泡,这是因为盐酸会与铁反应生成氯化亚铁(FeCl2)和氢气,该反应的化学方程式为: 。
Fe+2HCl=== FeCl2+H2↑
5. 小海用如图所示的思维导图总结了稀盐酸的五条化学性质。分析下图并回答问题:(1)该同学向稀盐酸中滴入紫色石蕊试液,发现紫色石蕊试液由紫色变成 色;(2)铁锈的主要成分是,试写出盐酸除铁锈的化学方程式: ;
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
5. 小海用如图所示的思维导图总结了稀盐酸的五条化学性质。分析下图并回答问题:(3)为验证性质③,该同学可选择的物质是______(填字母序号);A.Mg B.CO2 C.Na2CO3 D.Mg(OH)2(4)小海把稀盐酸和氢氧化钠溶液混合后,发现无明显现象,再向溶液中滴入无色酚酞试液,观察到无色溶液变成红色,则此时混合溶液的溶质是 (填化学式,不考虑酚酞)。
6. 如图所示,在白色点滴板上进行酸、碱性质的实验。完成以下实验报告:
Zn+2HCl=== ZnCl2+H2↑
2NaOH+H2SO4=== Na2SO4+2H2O
相关课件
这是一份人教版(2024)九年级下册(2024)实验活动8 常见酸、碱的化学性质精品教学课件ppt,文件包含核心素养《实验活动8常见酸碱的化学性质》课件PPTpptx、核心素养《实验活动8常见酸碱的化学性质》教学设计docx、核心素养《实验活动8常见酸碱的化学性质》同步分层练习docx等3份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
这是一份化学基础实验8 酸与碱的化学性质习题课件ppt,共24页。PPT课件主要包含了化学性质,不变色,石蕊溶液变蓝,无色酚酞变红,NaOH溶液,稀盐酸,无色酚酞等内容,欢迎下载使用。
这是一份初中沪教版基础实验8 酸与碱的化学性质图片ppt课件









