
苏教版 (2019)必修 第二册第一单元 化石燃料与有机化合物练习
展开
这是一份苏教版 (2019)必修 第二册第一单元 化石燃料与有机化合物练习,共12页。试卷主要包含了下列有关乙烯的说法不正确的是,下列关于乙烯的说法不正确的是,下列反应中属于加成反应的是,下列反应中,属于加成反应的是,下列关于实验的说法正确的是等内容,欢迎下载使用。
A.能与NaOH溶液反应
B.能使酸性溶液褪色
C.一定条件下可以聚合成聚乙烯
D.通入溴的四氯化碳溶液中,能与发生加成反应
2.下列关于乙烯的说法不正确的是( )
A.属于烃B.官能团为碳碳双键
C.不能使酸性高锰酸钾溶液褪色D.能在空气中燃烧
3.足量的下列物质不能使溴水褪色的是( )
A.二氧化硫B.甲烷C.乙烯D.氢氧化钠溶液
4.下列反应中属于加成反应的是( )
A.乙烯使溴水褪色
B.乙烯使酸性高锰酸钾溶液褪色
C.将苯滴入溴水中,振荡后水层接近无色
D.甲烷与氯气混合,黄绿色消失
5.下列反应中,属于加成反应的是( )
A.甲烷与氯气在光照下反应B.乙烯与水反应制取乙醇
C.甲烷燃烧生成二氧化碳和水D.乙醇与酸性高锰酸钾溶液反应
6.某实验小组为了探究乙烯的性质,设计了如图所示的实验装置:
下列叙述错误的是( )
A.温度需要控制在170 ℃
B.点燃具支试管Ⅱ试管处排出的尾气可以观察到明亮蓝色的火焰
C.该实验可以观察到4和5处颜色逐渐褪去
D.3的作用是防止二氧化硫干扰实验
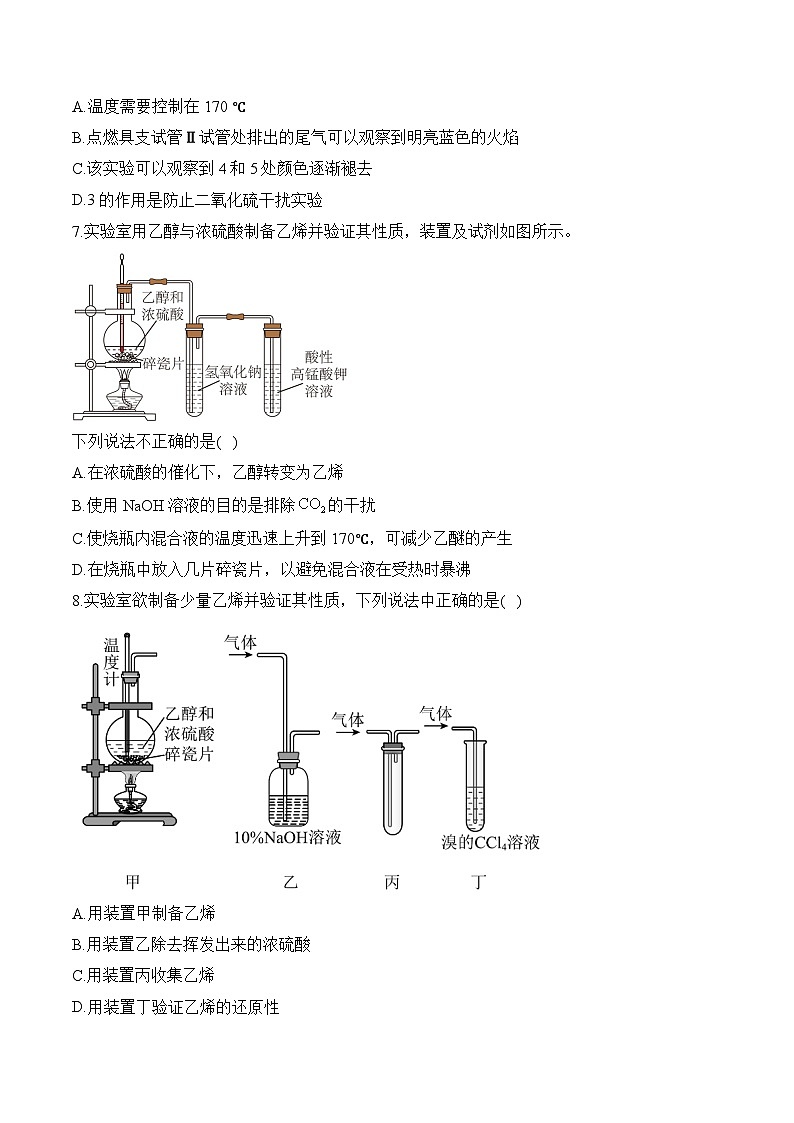
7.实验室用乙醇与浓硫酸制备乙烯并验证其性质,装置及试剂如图所示。
下列说法不正确的是( )
A.在浓硫酸的催化下,乙醇转变为乙烯
B.使用NaOH溶液的目的是排除的干扰
C.使烧瓶内混合液的温度迅速上升到170℃,可减少乙醚的产生
D.在烧瓶中放入几片碎瓷片,以避免混合液在受热时暴沸
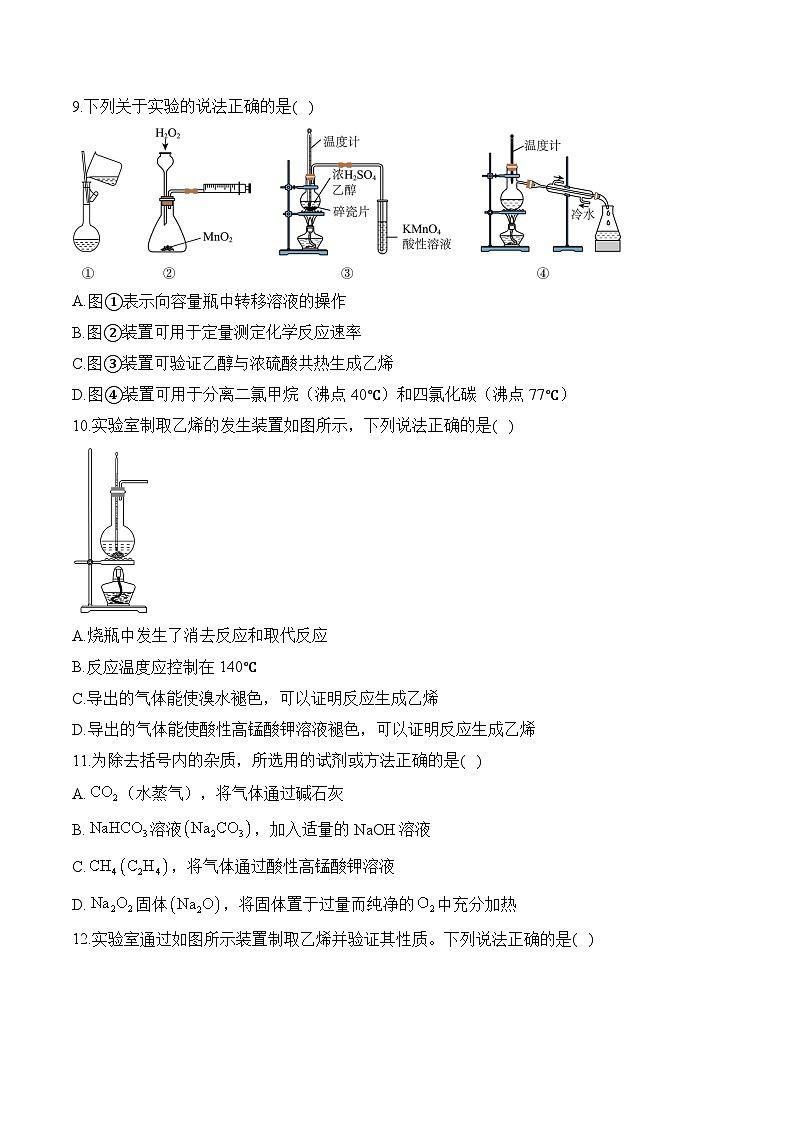
8.实验室欲制备少量乙烯并验证其性质,下列说法中正确的是( )
A.用装置甲制备乙烯
B.用装置乙除去挥发出来的浓硫酸
C.用装置丙收集乙烯
D.用装置丁验证乙烯的还原性
9.下列关于实验的说法正确的是( )
A.图①表示向容量瓶中转移溶液的操作
B.图②装置可用于定量测定化学反应速率
C.图③装置可验证乙醇与浓硫酸共热生成乙烯
D.图④装置可用于分离二氯甲烷(沸点40℃)和四氯化碳(沸点77℃)
10.实验室制取乙烯的发生装置如图所示,下列说法正确的是( )
A.烧瓶中发生了消去反应和取代反应
B.反应温度应控制在140℃
C.导出的气体能使溴水褪色,可以证明反应生成乙烯
D.导出的气体能使酸性高锰酸钾溶液褪色,可以证明反应生成乙烯
11.为除去括号内的杂质,所选用的试剂或方法正确的是( )
A.(水蒸气),将气体通过碱石灰
B.溶液,加入适量的NaOH溶液
C.,将气体通过酸性高锰酸钾溶液
D.固体,将固体置于过量而纯净的中充分加热
12.实验室通过如图所示装置制取乙烯并验证其性质。下列说法正确的是( )
A.装置甲加热时应缓慢升高温度到170℃
B.装置甲中浓硫酸的作用是作催化剂和吸水剂
C.为除去乙烯中混有的少量,装置乙中可加入NaOH溶液
D.装置丙中溶液褪色时有生成
13.有机物A的产量是衡量一个国家石油化工发展水平的标志,可发生以下系列转化,B、D是生活中常见的两种有机物,下列说法不正确的是( )
A.A的电子式为:
B.75%的B溶液(体积分数)可作医用消毒剂
C.B、D、E三种物质可以用饱和溶液鉴别
D.由B、D制备E时浓只作脱水剂
14.实验室制得气体中常含有杂质,会影响其性质检验。下图A为除杂装置,B为性质检验装置,完成下列表格。
15.实验室为探究铜与浓硫酸的反应,并验证的性质,设计如图所示装置进行实验。
请回答下列问题:
(1)装置A中的反应,浓硫酸体现了__________性和__________性。
(2)装置B中酸性溶液逐渐褪色,证明具有__________性;装置C中发生反应的化学方程式__________。
(3)装置D的作用是__________;实验结束时需从导管a通入大量空气,其目的是__________。
(4)装置E中NaOH溶液足量,写出E中反应的离子方程式__________。
(5)溶于水生成,已知酸性,为了证明酸性,将通入到下列试剂,下列试剂排序正确的是_______(填选项)。
①小苏打溶液;②品红溶液;③酸性溶液;④漂白粉溶液
A.②①③④B.③②①④C.①③②④D.④③②①
(6)实验室制取的乙烯中常混有少量,用下面装置证明混合气体中含有乙烯。其中Ⅱ中为品红溶液,Ⅲ中为溴的四氯化碳溶液。
①Ⅰ中的试剂可以为__________(填字母)。
a.酸性溶液b.NaOH溶液c.溶液
②证明含有乙烯的现象是__________。
答案以及解析
1.答案:A
解析:乙烯结构简式是,能够发生燃烧反应、加成反应、加聚反应,能够被酸性溶液氧化,据此分析解答。
A.乙烯是中性气体,与NaOH溶液不能发生反应,A错误;
B.乙烯分子中含有不饱和的碳碳双键,能被酸性溶液氧化而使酸性溶液褪色,B正确;
C.乙烯分子中含有不饱和的碳碳双键,在一定条件下能够发生加聚反应产生高分子化合物聚乙烯,C正确;
D.乙烯分子中含有不饱和的碳碳双键,能够与发生加成反应产生1,2-二溴乙烷,D正确;
故合理选项是A。
2.答案:C
解析:A.乙烯只含有碳和氢两种元素,属于烃,A正确;
B.乙烯为烯烃,官能团为碳碳双键,B正确;
C.乙烯的官能团为碳碳双键,可以被酸性高锰酸钾氧化,高锰酸钾溶液褪色,C错误;
D.乙烯是可以燃烧的有机物,D正确;故选C。
3.答案:B
解析:,A项不符合题意;
甲烷不能使溴水褪色,B项符合题意;
,C项不符合题意;
溴水类似氯水可以与NaOH反应,方程式为,D项不符合题意。
4.答案:A
解析:A.乙烯和溴水发生加成反应,故符合题意;B.乙烯使酸性高锰酸钾溶液褪色是发生氧化反应,故不符合题意;C.苯和澳水是萃取过程,不是化学反应,故不符合题意;D.甲烷和氨气发生取代反应,故不符合题意。故答案为:A。
5.答案:B
解析:有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应;
A.甲烷与氯气在光照下反应发生的是取代反应,故A错误;
B.乙烯与水反应制取乙醇的反应为加成反应,故B正确;
C.甲烷燃烧生成二氧化碳和水的反应为氧化反应,故C错误;
D.乙醇与酸性高锰酸钾溶液反应属于氧化反应,故D错误;
故选:B。
6.答案:B
解析:温度过低会生成副产物乙醚,A叙述正确;尾气为未反应的乙烯,乙烯在空气中燃烧,火焰明亮且伴有黑烟,B叙述错误;乙烯可以与溴水发生加成反应、与酸性高锰酸钾溶液发生氧化反应而使二者颜色逐渐褪去,C叙述正确;酒精易与浓硫酸发生氧化还原反应,从而产生二氧化硫干扰乙烯性质的检验,3中的氢氧化钠溶液可以吸收乙烯中混有的二氧化硫气体,D叙述正确。
7.答案:B
解析:A.在浓硫酸的催化下,乙醇发生消去反应,生成乙烯,A正确;
B.浓硫酸具有脱水性和强氧化性,反应过程中会生成、,、乙醇都能使酸性高锰酸钾溶液褪色,不能使酸性高锰酸钾溶液褪色,则、乙醇扰乙烯的检验,不干扰乙烯的检验,所以使用氢氧化钠溶液的目的是排除、乙醇的干扰,B错误;
C.乙醇在浓硫酸作催化剂、加热170°C下发生消去反应生成乙烯,在浓硫酸作催化剂、加热140℃下发生取代反应生成乙醚,所以使烧瓶内混合液的温度迅速上升到170°C,可减少乙醚的产生,C正确;
D.碎瓷片能防暴沸,所以在烧瓶中放入几片碎瓷片,以避免混合液在受热时暴沸,D正确;
故选B。
8.答案:A
解析:A.无水乙醇和浓硫酸的混合液迅速加热到时制取乙烯,温度计伸入液体中,碎瓷片可防倒吸,可用装置甲制备乙烯,故选A;
B.浓硫酸不挥发,装置乙为洗气瓶,用装置乙除杂,除乙烯中的二氧化硫、二氧化碳等,故不选B;
C.乙烯的密度和空气的密度相近,不能用排空气法收集乙烯,故不选C;
D.乙烯和溴发生加成反应,若用装置丁验证乙烯的还原性,应选用酸性高锰酸钾溶液,故不选D;
选A。
9.答案:D
解析:A.向容量瓶中转移溶液时,玻璃棒应该在刻度线以下,A错误;
B.定量测定化学反应速率,应该把长颈漏斗改为分液漏斗,B错误;
C.乙醇与浓硫酸共热生成乙烯,反应温度170℃,温度计在溶液中,但是挥发的乙醇和乙烯都能够与酸性高锰酸钾反应,不能得出生成乙烯,C错误;
D.二氯甲烷(沸点40℃)和四氯化碳(沸点77℃)互溶,可以通过蒸馏分离,D正确;
故选D。
10.答案:A
解析:A.在170℃发生消去反应生成乙烯,在140℃发生取代反应生成乙醚,故A正确;
B.乙醇和浓硫酸混合加热制乙烯,反应温度控制在170℃,故B错误;
C.浓硫酸与乙醇混合制乙烯时会发生氧化还原反应生成, 也能使溴水褪色,则无法证明反应生成乙烯,故C错误;
D.乙醇具有挥发性,浓硫酸与乙醇混合制乙烯时会挥发乙醇,乙醇也能使酸性高锰酸钾褪色,则无法证明反应生成乙烯,故D错误;
故选A。
11.答案:D
解析:A.二氧化碳可与碱石灰反应,将原物质除去,不能除杂,故A错误;B.碳酸氢钠溶液与NaOH溶液反应,将原物质除去不能除杂,故B错误;C.通入氨气,二者均反应生成沉淀,沉淀均溶于盐酸,不能除杂,故C错误;D.氧化钠与氧气反应生成过氧化钠,则将固体置于过量而纯净的中充分加热可除杂,故D正确;故选:D。
12.答案:C
解析:A.在浓硫酸的作用下,乙醇制备乙烯的反应温度为170℃,关键是迅速升温至,防止温度较低发生副反应,A错误;
B.装置甲中浓硫酸的作用是作催化剂和脱水剂,B错误;
C.二氧化硫与氢氧化钠溶液可以反应,而乙烯与氢氧化钠溶液不反应,C正确;
D.装置丙中溶液褪色时有生成,无,D错误;
13.答案:D
解析:根据题意可知A是乙烯,B是乙醇,C是乙醛D是乙酸,E是乙酸乙酯。A是乙烯,其电子式为,A项正确;体积分数为75%的酒精可作医用消毒剂,B项正确;乙醇能够溶于水,不分层,乙酸与饱和溶液反应放出气体,有气泡产生,而乙酸乙酯与饱和溶液互不相溶,混合后分层,故可以用饱和溶液鉴别B、D、E三种物质,C项正确;由B、D制备E时浓作催化剂、吸水剂,D项错误。
14.答案:;水;;NaOH溶液;;溶液
解析:根据装置可知A装置用来进行气体除杂,B装置进行气体性质检验,据此分析解题。
(1)溴乙烷和NaOH的醇溶液加热发生消去反应,反应的化学方程式是:,乙醇易挥发,且易溶于水,乙烯混有乙醇,可用水除杂;
(2)无水乙醇在浓硫酸的作用下加热至170℃发生消去反应生成乙烯和水,反应的化学方程式是;若温度过高或加热时间过长,制得的乙烯往往混有,故选用NaOH溶液进行除杂;
(3)电石与饱和食盐水反应生成的乙炔气体中含有杂质,反应方程式为:;溶液和反应生成CuS沉淀和硫酸,用溶液可除去乙炔中的,所以A中试剂是溶液。
15.答案:(1)酸;氧化
(2)还原;
(3)验证的漂白性和生成物的不稳定性;使装置中残留的完全被装置E吸收,防止污染空气
(4)
(5)C
(6)bc;Ⅱ中品红溶液不褪色,Ⅲ中溴的四氯化碳溶液褪色
解析:装置A中,铁丝与浓硫酸反应生成二氧化硫,二氧化硫在装置B被酸性溶液氧化,表现还原性,在装置C被还原表现氧化性,二氧化硫通入到品红溶液中褪色表现漂白性,最后,使用装置对剩余二氧化硫进行尾气处理,以此作答。
(1)在装置A中,铁与浓硫酸反应生成的硫酸铁、二氧化硫和水,浓硫酸表现了氧化性和酸性,故答案为:酸;氧化;
(2)装置B酸性溶液将氧化为硫酸根离子,证明具有还原性;在装置C中和反应生成S和,其化学方程式为,故答案为:还原;;
(3)通入品红溶液中使品红溶液褪色表现漂性,加热后又恢复至原来的颜色说明生成物的不稳定性;实验结束时,装置中存在气体,为防止污染空气,可从导管a处通入大量空气,装置中排入装置E中被装置E吸收,故答案为:验证的漂白性和生成物的不稳定性;使装置中残留的完全被装置E吸收,防止污染空气;
(4)通入NaOH溶液后被吸收,生成和水,其离子方程式为:,故答案为:;
(5)因为具有强还原性,有强氧化性,能将氧化,故不能直接将直接通入漂白粉溶液,需先将通入小苏打溶液中制备,证明酸性,然后通入到酸性溶液除去气体,再通入品红溶液证明已经除净,最后将纯净的通入到漂白粉溶液中制备HClO,证明酸性,从而证明,故答案为:C。
(6)①I中试剂的作用是吸收二氧化硫但不与乙烯反应,可选用氢氧化钠溶液和亚硫酸钠溶液,酸性高锰酸钾能将乙烯氧化为二氧化碳,故答案为:bc;
②Ⅱ中为品红溶液,Ⅲ中为溴的四氯化碳溶液,证明含有乙烯的现象是:Ⅱ中品红溶液不褪色,Ⅲ中溴的四氯化碳溶液褪色。
序号
检验气体
反应原理
A中试剂
(1)
乙烯
溴乙烷和NaOH的醇溶液加热,反应的化学方程式是_____________。
_____________
(2)
乙烯
无水乙醇在浓硫酸的作用下加热至170℃,反应的化学方程式是_____________。
_____________
(3)
乙炔
电石与饱和食盐水反应,反应的化学方程式是_____________。
_____________
相关试卷
这是一份高中化学苏教版 (2019)必修 第二册第二单元 化学反应中的热同步达标检测题,共11页。试卷主要包含了下列燃烧热相同的是,下列热化学方程式书写正确的是,各相关物质的燃烧热数据如下表,已知等内容,欢迎下载使用。
这是一份苏教版 (2019)必修 第二册第一单元 氮的固定课后作业题,共10页。试卷主要包含了下列关于的叙述错误的是,下列过程属于人工固氮的是,下列过程不属于氮的固定的是,下列过程属于氮的固定的是,自然界的氮循环包括以下过程等内容,欢迎下载使用。
这是一份必修 第二册专题8 有机化合物的获得与应用第一单元 化石燃料与有机化合物一课一练,共10页。试卷主要包含了下列物质中,属于不饱和烃是,下列化学用语表述正确的是,下列有关烃的说法错误的是,以下说法错误的是,下列关于苯的叙述正确的是等内容,欢迎下载使用。









