




所属成套资源:2023-2024学年高一下学期化学人教版(2019)必修第二册
高中第七章 有机化合物第一节 认识有机化合物集体备课ppt课件
展开
这是一份高中第七章 有机化合物第一节 认识有机化合物集体备课ppt课件,共38页。PPT课件主要包含了青霉素,CH4,都含有C元素,有机化合物,无机化合物,碳“四价”理论,思考与交流,碳原子的成键特点,资料卡片,甲烷的分子结构等内容,欢迎下载使用。
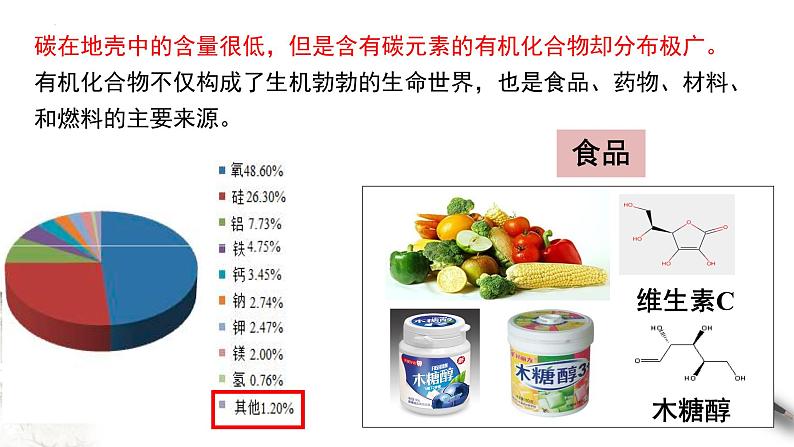
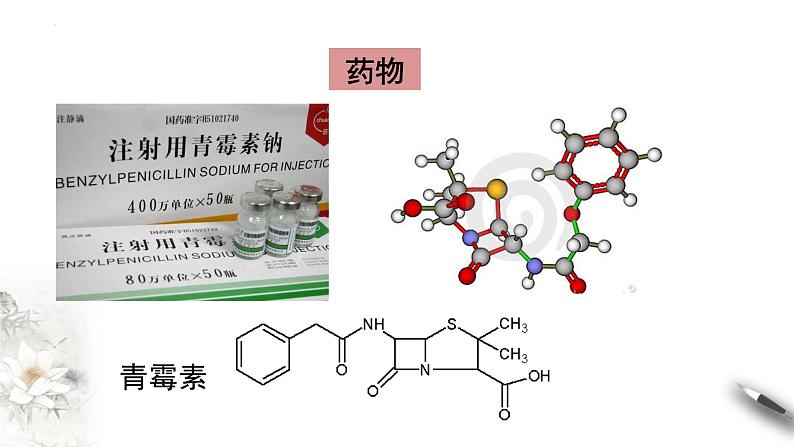
碳在地壳中的含量很低,但是含有碳元素的有机化合物却分布极广。有机化合物不仅构成了生机勃勃的生命世界,也是食品、药物、材料、和燃料的主要来源。
目前,人们在自然界发现和人工合成的物质已超过1亿种,其中绝大多数都是有机化合物,而且新的有机化合物仍在源源不断地被发现或合成出来。有机化合物为什么如此繁多?它们的结构和性质具有哪些一般特点?
让我们一起走进奇妙的有机世界
第七章 有机化合物第一节 认识有机化合物第一课时 有机化合物中碳原子的成键特点
有机化合物在日常生活中随处可见,你能举出哪些例子?
1.食品:糖类,油脂,蛋白质等
4.燃料:煤炭,石油,天然气等
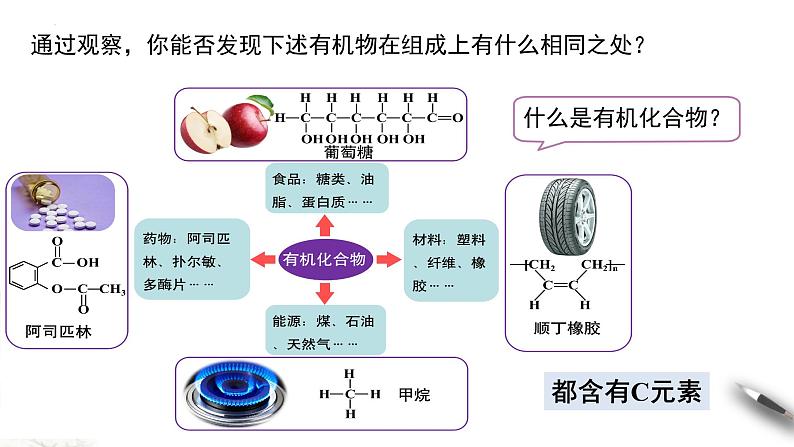
通过观察,你能否发现下述有机物在组成上有什么相同之处?
绝大多数含碳元素的化合物
碳的单质(例金刚石,石墨,C60 等)、
(1)有机化合物一定含有碳元素,但不一定含有氢元素
(2)含有碳元素的物质不一定是有机化合物
硫氰酸(HSCN)、硫氰化物(例KSCN)等物质。
CS2、碳化硅 SiC(金刚砂) , CaC2 碳化钙(电石)、
碳酸(H2CO3)、碳酸盐(例Na2CO3) 、碳酸氢盐(例NaHCO3)
氢氰酸(HCN)、氰化物(例NaCN)、
例CCl4 是有机物
如:CH4、C6H12O6、C2H5OH等
氰化氢的水溶液为氢氰酸 ,有剧毒,是一种极弱的酸,酸性比碳酸弱,比碳酸氢根强。
氰化氢,是一种无机化合物,化学式为HCN,沸点26℃,
碳、氢、氧、硫、氮、磷、卤素等
有机物种类繁多,我们如何去学习它们的性质呢?
标准状态下为液态,无色,有苦杏仁味。
从化学键的形成角度来看,甲烷属于什么化合物?这反映了碳原子成键时的什么特点?
碳原子通常与相邻原子以共价键的成键方式形成共价化合物。
仔细观察下列有机化合物的结构,归纳碳原子间可有哪些结合方式(碳骨架)
碳原子周围形成了4个共价键(4对共用电子对)
每个碳原子形成几条键?碳原子间结合形成哪些键?
通常与 H、O、S、N 等非金属原子以共价键的成键方式形成共价化合物。
二、有机化合物中碳原子的成键特点
每个碳原子都与其他原子形成 4 个共价键。
(1)成键的类型:碳原子与碳原子之间可以形成单键、双键或三键。
(碳原子最外层有 4 个电子,在化学反应中不易失去或得到电子)
请结合下图显示的4个碳原子相互结合的几种方式,分析以碳为骨架的有机物种类繁多的原因。
碳原子间可以以单键、双键或三键相结合,也可以形成碳链或碳环等碳骨架。
有机物中碳原子成键特点和碳原子间的连接特点决定了有机物种类繁多。
含有相同碳原子数的有机物分子,可能因为碳原子间的成键方式或碳骨架的不同而具有多种结构。
(2)碳骨架形式:碳原子之间可构成链状结构,也可构成环状结构。
【变1】2019年8月15日,牛津大学化学系与IBM苏黎世研究实验室合作的一项成果发表在《Sicence》,他们合成了世界上第一个完全由碳原子构成的环状分子——C18,如图所示,其中的18个碳原子通过交替的碳碳单键和碳碳三键相连接。下列关于C18的说法错误的是( )A.属于环状有机物 B.与石墨、金刚石互为同素异形体C.属于无机物 D.碳原子间的结合方式有多种
【例2】有机物分子中的碳原子与其他原子的结合方式是( )A.通过两个共价键 B.通过非极性键C.形成四对共用电子对D.通过离子键和共价键
【变2-1】碳原子的不同结合方式使得有机物种类繁多,下列碳原子的结合方式中错误的是( )
【变2-2】下列化学式及结构式中,从成键情况看不合理的是( )
3.下图是表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。
(1)碳原子间所成的化学键全是碳碳单键的有_____________(填字母,下同),含有碳碳双键的有________,含有碳碳三键的有______。
(2)碳骨架为链状的有 _______________________ ,为环状的有_______,含有支链的有 ________ 。
A、B、C、D、E、F、G
使用模型研究物质结构 将微观的分子结构通过模型呈现出来,便于我们了解分子中原子的结合方式与空间位置关系,获取更多的结构信息。随着现代信息技术的发展,除了实物模型,还可以通过计算机对物质的结构进行模拟和计算。这是人们探索物质结构的重要方法,也是学习化学的直观工具。
今天我们也效仿科学家,采用实物模型来研究有机物中碳原子的成键特点。
CH4 的空间结构——正四面体
甲烷分子中5个原子不在同一平面上,而是形成了正四面体的空间结构,
碳原子位于正四面体的中点,4个氢原子分别位于4个顶点。分子中的4个C—H键的长度和强度相同,夹角也相同。
最简单的有机化合物----甲烷分子结构
经过科学实验证明甲烷分子的结构是正四面体结构,键能为413.4KJ/ml,键长为109pm,键角为109°28′。
三、有机化合物组成和结构的表示方法
结构式是表达原子之间共用电子对情况的平面模型,并不能把物质的空间结构真实表达出来。实际上甲烷中的5个原子并不是处于同一平面。
(1)甲烷分子中的4个C—H 极性键完全相同,5个原子不在同一平面上,其中最多有3个原子在同一平面上。
(2)甲烷分子的电子式和结构式均表示分子中原子的成键方式,但不能表示分子真实的空间结构;
球棍模型和空间填充模型则能表示分子中原子间的连接方式、原子的相对大小及空间分布等。
表示物质组成的各元素原子最简整数比的式子。
(2)最简式(实验式):
如 C4H10 的最简式为
用元素符号表示物质分子组成的式子,可反映一个分子中原子的种类和数目
如 C2H6 的最简式为
如 C3H8的最简式为
省略C−H键,把同一碳原子上的H合并,省略横线上C−C键
【注意】省略单键,但双键、三键不能省略
用短线来表示原子间的共用电子对
用小黑点等符号代替电子,表示原子最外层电子成键情况的式子
练习1. 根据下列有机分子的结构式,写出下列有机物的结构简式:
CH3CH2CH3
CH3CH2CH2CH3
或 CH3CH(CH3 )CH3
省略碳、氢元素符号,只写碳碳键;通常相邻碳碳键之间的夹角画成120°,每个端点和转折点都表示碳原子,除C、H以外原子都保留下来。
如:CH3CH2CH3 键线式可表示为__________________
键线式可表示为__________________
CH3CH=CHCH3 键线式可表示为__________________
用不同体积的小球表示不同大小的原子,空间填充模型可以表示分子的空间结构。
能够表示分子的空间结构和分子内原子之间的成键类型。
“棍”表示共价键(单键、双键或三键) 。
练习2. 根据下列有机分子的球棍模型,写出下列有机物的结构简式
CH3-CH2-CH2-CH2-CH3
练习3. 根据下列有机分子的碳骨架,写出各有机物对应的结构简式。
CH3—C≡C—CH2—CH3
练习4. 写出下列分子模型对应的结构简式
或:CH3(CH2)2CH(CH3)CH3
1.如图所示均能表示甲烷的分子结构,下列说法错误的是( )A.Ⅰ将各原子看成了质点,为立体结构示意图B.Ⅱ为电子式,表示甲烷分子中有8个电子C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键D.Ⅳ为空间填充模型,能表示出甲烷的空间构型及各原子的相对大小
2.下图为正丁烷的球棍模型。下列说法正确的是 ( )A.正丁烷的分子式为C4H8B.分子中4个碳原子在同一条直线上C.分子中含有4个碳碳单键D.分子中共含有13个共价键
相关课件
这是一份高中化学人教版 (2019)必修 第二册第一节 认识有机化合物课文内容课件ppt,共18页。
这是一份高中化学人教版 (2019)必修 第二册第一节 认识有机化合物备课课件ppt,共19页。PPT课件主要包含了想一想,思考与交流,碳原子的成键特点,形成4个共价键,球棍模型,比例模型,结构式,电子式,原子结构示意图,烷烃的结构特点等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第二册第一节 认识有机化合物教课内容课件ppt,共60页。PPT课件主要包含了碳+氢,tànqīng,tīng,最简单的烃甲烷,碳碳单键,碳碳双键,碳碳三键,典型例题,甲烷的空间构型等内容,欢迎下载使用。









