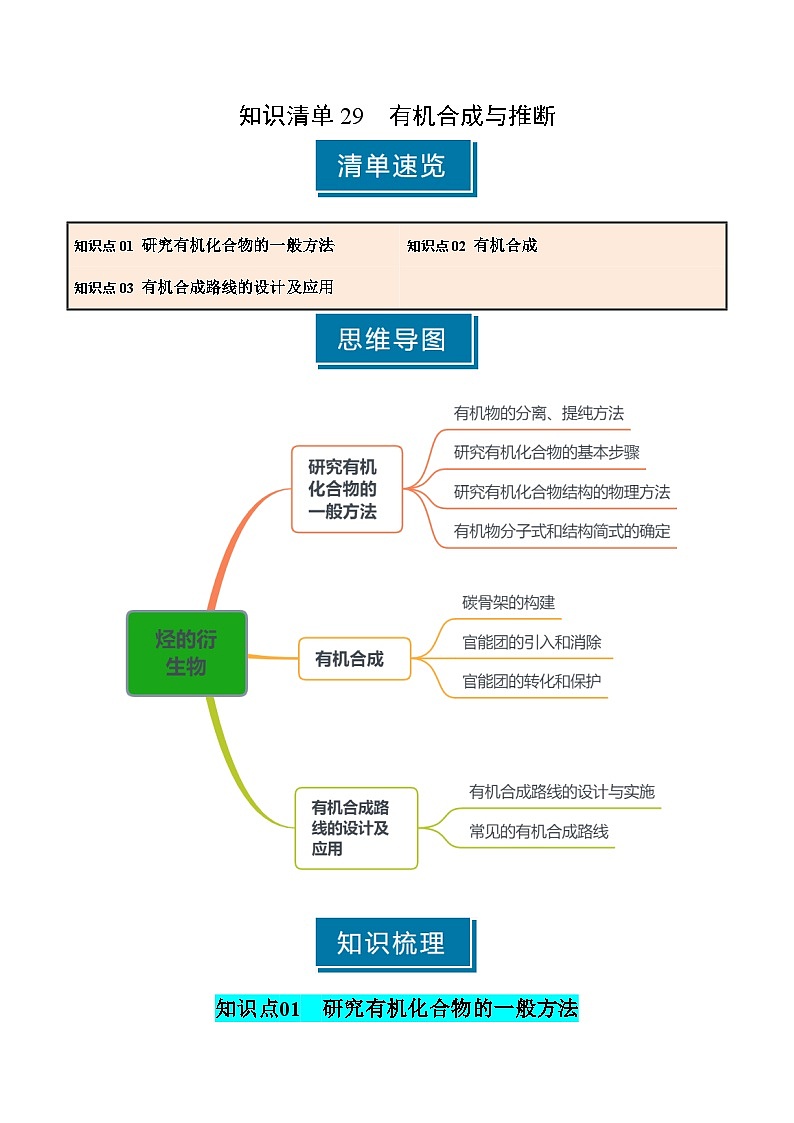

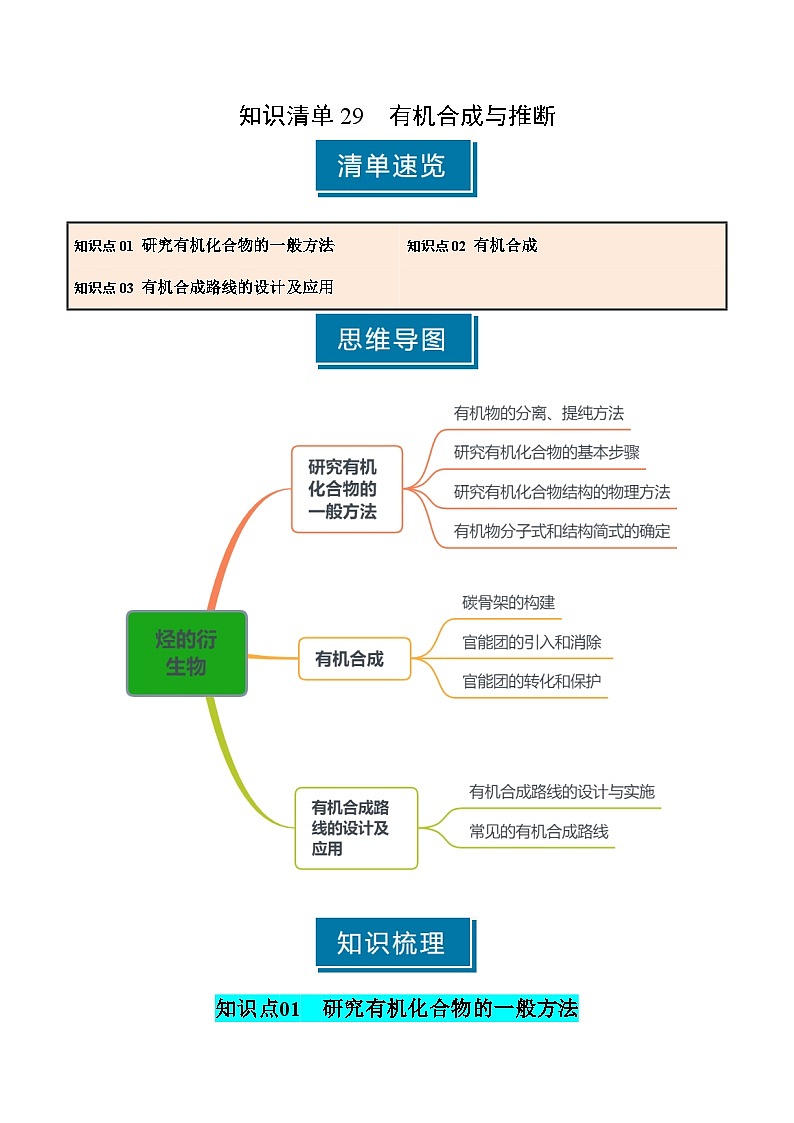

知识清单29 有机合成与推断(含答案) 2025年高考化学一轮复习知识清单
展开知识点01 研究有机化合物的一般方法
一、有机物的分离、提纯方法
1.蒸馏
(1)适用范围:分离、提纯的有机物热稳定性较高,其沸点与杂质的沸点相差较大。
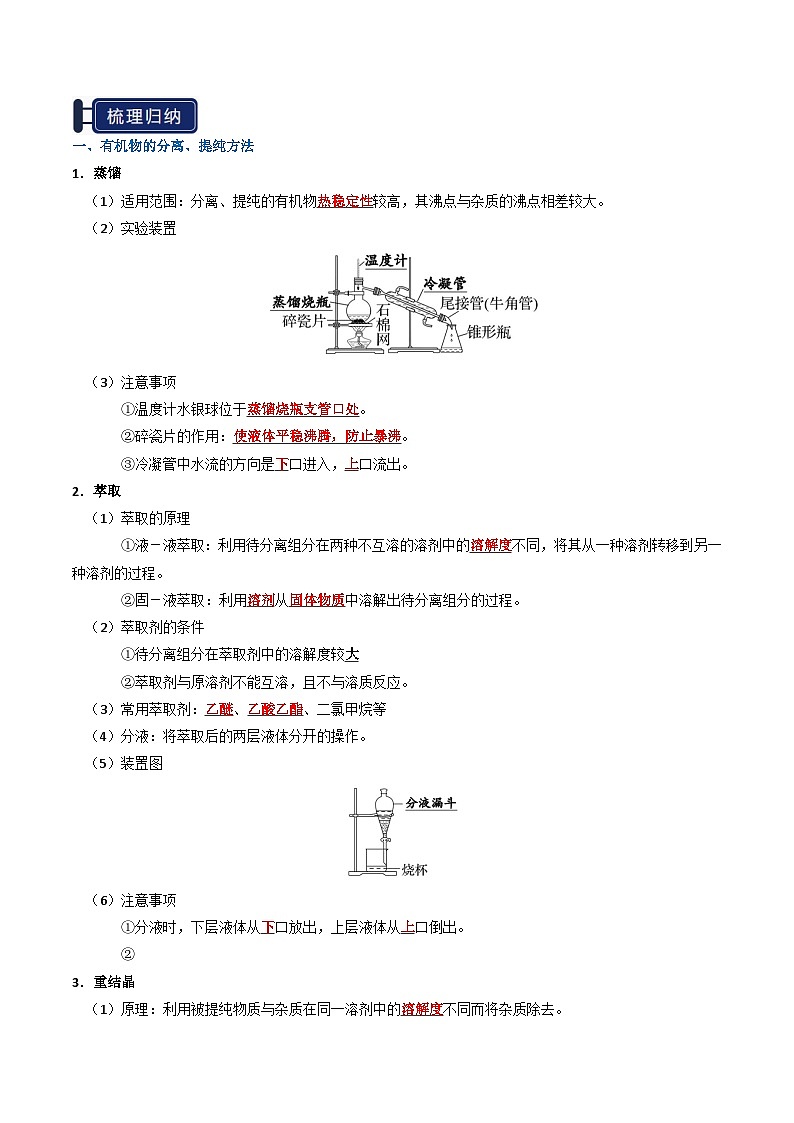
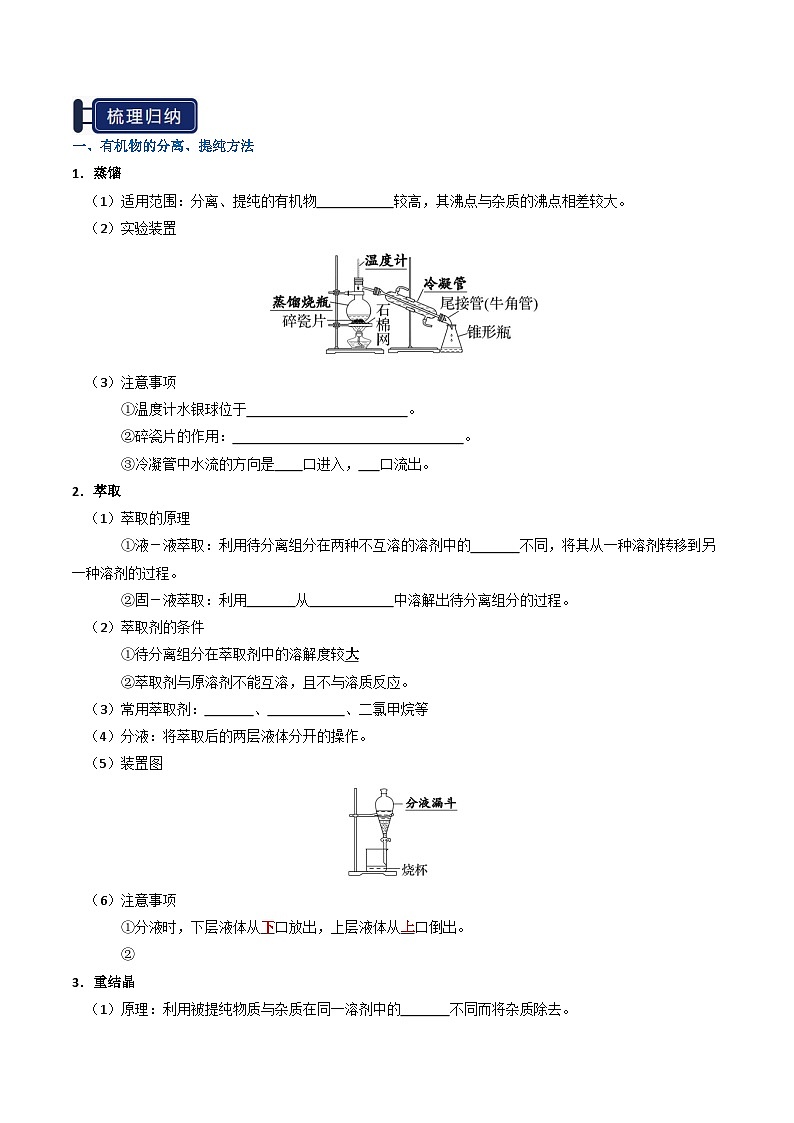
(2)实验装置
(3)注意事项
①温度计水银球位于蒸馏烧瓶支管口处。
②碎瓷片的作用:使液体平稳沸腾,防止暴沸。
③冷凝管中水流的方向是下口进入,上口流出。
2.萃取
(1)萃取的原理
①液-液萃取:利用待分离组分在两种不互溶的溶剂中的溶解度不同,将其从一种溶剂转移到另一种溶剂的过程。
②固-液萃取:利用溶剂从固体物质中溶解出待分离组分的过程。
(2)萃取剂的条件
①待分离组分在萃取剂中的溶解度较大
②萃取剂与原溶剂不能互溶,且不与溶质反应。
(3)常用萃取剂:乙醚、乙酸乙酯、二氯甲烷等
(4)分液:将萃取后的两层液体分开的操作。
(5)装置图
(6)注意事项
①分液时,下层液体从下口放出,上层液体从上口倒出。
②
3.重结晶
(1)原理:利用被提纯物质与杂质在同一溶剂中的溶解度不同而将杂质除去。
(2)溶剂的选择
①杂质在所选溶剂中的溶解度很大或溶解度很小,易于除去。
②被提纯的有机化合物在所选溶剂中的溶解度受温度的影响较大,能够进行冷却结晶。
(3)装置图及操作步骤
4.常见有机物的分离提纯方法(括号内为杂质)
二、研究有机化合物的基本步骤
三、研究有机化合物结构的物理方法
1.质谱法
(1)作用:测定有机物的相对分子质量
(2)读图:质谱图中最右侧的分子离子峰或质荷比最大值表示样品中分子的相对分子质量
(3)示例:该有机物的相对分子质量为46。
2.红外光谱
(1)作用:初步判断某有机物分子中所含有的化学键或官能团。
(2)不同的化学键或官能团的吸收频率不同,在红外光谱图上将处于不同的位置。
(3)示例:有机物C2H6O的红外光谱上有O-H、C-H和C-O的吸收峰,可推知其结构为C2H5OH。
3.核磁共振氢谱
(1)作用:测定有机物分子中氢原子的类型和它们的相对数目。
(2)读图:吸收峰数目=氢原子种类,吸收峰面积比=氢原子数之比。
(3)示例:有机物C2H6O的核磁共振氢谱如图,图中三个峰的面积之比是1∶2∶3,则有3种处于不同化学环境的氢原子,个数比为1∶2∶3,其结构简式为CH3CH2OH。
4.X射线衍射
(1)作用:可以获得键长、键角等分子结构信息。
(2)应用:将X射线衍射技术用于有机物(特别是复杂的生物大分子)晶体结构的测定,可以获得更为直接而详尽的结构信息。
四、有机物分子式和结构简式的确定
1.有机物分子式的确定
(1)常规确定方法
(2)化学方程式法:利用有机反应中反应物、生成物之间“量”的关系求分子式的方法。
①CxHy+(x+)O2xCO2+H2O(g)
②CxHyOz+(x+-)O2xCO2+H2O(g)
③CxHyOzNp+(x+ QUOTE - QUOTE )O2xCO2+ QUOTE H2O+ QUOTE N2
(3)“商余法”推断烃的分子式(设烃的相对分子质量为M)
QUOTE M12 的余数为0或碳原子数大于或等于氢原子数时,将碳原子数依次减少一个,每减少一个碳原子即增加12个氢原子,直到饱和为止。
2.有机物的不饱和度的确定
(1)计算公式:
①不含氮原子:Ω=
②含有氮原子:Ω=
(2)说明
①N(C)表示碳原子数,N(H)表示氢原子数,N(N)表示氮原子数。
②若有机化合物分子中含有卤素原子,则将其视为氢原子。
(3)常见官能团或原子团的不饱和度
3.有机物分子结构的鉴定
(1)分子结构确定步骤
(2)有机物的不饱和度与分子结构的关系
①Ω=0,说明分子是饱和链状结构;
②Ω=1,说明分子中有一个双键或一个环;
③Ω=2,说明分子中有两个双键或一个三键,或一个双键和一个环,或两个环;
④Ω≥4,说明分子中很有可能有苯环。
(3)实验方法确定有机化合物的官能团
1.判断正误,正确的打“√”,错误的打“×”。
(1)己烷中混有己烯,可使用溴水进行除杂,用分液的方法分离。( )
(2)红外光谱与核磁共振氢谱可以用于确定有机物的官能团和相对分子质量。( )
(3)李比希元素分析仪不仅可以分析试样中常见元素的含量,还可以测定试样分子的空间结构。( )
(4)1-丁醇与乙醚互为同分异构体,则质谱图相同。( )
(5)有机物核磁共振氢谱有两个峰,且峰面积之比为3:1。( )
(6)已知某有机物燃烧生成的CO2和H2O的量,即可判断该有机物的最简式。( )
(7)有机物完全燃烧后仅生成CO2和H2O,则该有机物中一定含有C、H、O三种元素。( )
(8)燃烧是测定有机物分子结构的有效方法。( )
(9) 的核磁共振氢谱中有6组峰。( )
(10)蒸馏分离液态有机物时,在蒸馏烧瓶中应加少量碎瓷片。( )
(11)乙醇是良好的有机溶剂,根据相似相溶原理用乙醇从水溶液中萃取有机物。( )
(12)用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3。( )
(13)CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不用H-NMR来鉴别。( )
(14)根据物质的沸点利用蒸馏法提纯液态有机物时,沸点相差大于30 ℃为宜。( )
(15)有机物核磁共振氢谱中会出现三组峰,且峰面积之比为3:4:1。( )
(16)混合物经萃取、分液后可获得纯净物。( )
(17)质谱法可以测定有机物的摩尔质量,而红外光谱和核磁共振氢谱图可以确定有机物的官能团类型。( )
【答案】(1) ( × )(2) ( × )(3) ( × )(4) ( × )(5) ( √ )(6) ( × )(7) ( × )(8) ( × )
(9) (×)(10) (√)(11) (×)(12) ( × )(13) ( × )(14) ( √ )(15) ( × )(16) ( × )(17) ( × )
1.下列实验中,所采取的分离或提纯方法与对应原理都正确的是( )
【答案】B
【解析】 乙醇与水互溶,不能用作萃取剂分离溶于水中的碘,A错误;乙酸与CaO反应,转化为难挥发的乙酸钙,再通过蒸馏即可提纯乙醇,B正确;乙烯会被酸性KMnO4溶液氧化为CO2,使甲烷中混有新的杂质,C错误;汽油和四氯化碳互溶,无法用分液法分离二者,D错误。
2.有机物M的核磁共振氢谱图如图,则M的结构简式可能是( )
A.CH3OCH3 B.CH3CH2OH
C.CH3CH2CH3 D.CH3COOCH2CH2CH3
【答案】B
【解析】 有机物含有1种H,则核磁共振氢谱有1个峰,故A错误;含有3种H,核磁共振氢谱有3个峰,故B正确;含有2种H,核磁共振氢谱有2个峰,故C错误;含有4种H,核磁共振氢谱有4个峰,故D错误。
知识点02 有机合成
一、碳骨架的构建
1.碳链的增长
(1)卤代烃的取代反应
①溴乙烷与氰化钠在酸性条件下的反应:
CH3CH2Br+NaCN→CH3CH2CN+NaBr,CH3CH2CNCH3CH2COOH。
②溴乙烷与丙炔钠的反应
CH3CH2Br+NaC≡CCH3→CH3CH2C≡CCH3+NaBr
(2)醛酮的加成反应
①丙酮与HCN的反应
②乙醛与HCN的反应
CH3CHO+HCNCH3CH(OH)CN
③羟醛缩合(以乙醛为例)
CH3CHO+CH3CHOCH3CH(OH)CH2CHO
④醛、酮与RMgX加成:
+RMgX。
2.碳链的缩短
(1)与酸性KMnO4溶液的氧化反应
①烯烃、炔烃的氧化反应
CH3-CHCH3CH3COOH+ CH3--CH3
②苯的同系物的氧化反应
CH2CH3COOH
(2)脱羧反应
①无水醋酸钠与氢氧化钠的反应:CH3COONa+NaOHCH4↑+Na2CO3
②2-甲基丙酸钠与氢氧化钠的反应:CH3-COONa+NaOHCH3CH2CH3↑+Na2CO3
(3)某些有机物的水解反应
①蛋白质的水解反应
②糖类的水解反应
③酯的水解反应
(4)水解的裂化或裂解
①异丁烷裂化:CH3-CH3CH4+CH3CH=CH2
②十八烷裂化:C18H38C8H18(辛烷)+ C8H16(辛烯)
二、官能团的引入和消除
1.官能团的引入
(1)碳碳双键的引入
①醇的消去:CH3CH2OHCH2=CH2↑+H2O
②卤代烃的消去:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
③邻二卤代烃的消去:+ZnCH2=CH2↑+ZnCl2
④炔烃与H2的加成:CH≡CH+H2CH2=CH2
(2)卤素原子的引入
①与HX的加成:CH2=CH2+HBrCH3CH2Br、CH≡CH+HBrCH2=CHBr
②与X2的加成:CH2=CH2+X2、CH≡CH+X2
③烷烃、芳香烃的取代反应:CH4+Cl2CH3Cl+HCl、+Br2Br +HBr
④烯烃、羧酸的α-H取代
CH3-CH=CH2+Cl22-CH=CH2+HCl
RCH2COOH+Cl2R--COOH +HCl
⑤醇与卤代烃的取代:CH3CH2OH+HBrCH3CH2Br+H2O
(3)羟基的引入方式
①烯烃与水加成:CH2=CH2+H2OCH3CH2OH
②醛、酮与H2加成:CH3CHO+H2CH3CH2OH
③醛、酮与HCN加成:CH3--H +HCNCH3--CN
④羟醛缩合:CH3--H +H-CH2CHOCH3--CH2-CHO
⑤卤代烃的水解:CH3--CH3+NaOHCH3--CH3+NaBr
⑥酯的水解:CH3--O-C2H5+H2OCH3COOH+C2H5OH
⑦酚钠与酸反应:ONa+H2O+CO2OH +NaHCO3
(4)羧基的引入方式
①烯的氧化:RCH2CH=CH2RCH2COOH+CO2↑
②腈的水解:CH3CH2CNCH3CH2COOH
③醛的氧化:2RCHO+O22RCOOH
(5)羰基的引入方式
①烯的氧化:CH2CH3CO2↑+CH3--CH3
②叔醇的催化氧化:2R--R′+O22R--R′+2H2O
2.官能团的消除
(1)通过加成反应消除或-C≡C-
①CH2=CH2+H2CH3CH3
②CH3-C≡C-CH3+2H2CH3CH2CH2CH3
(2)通过消去反应或氧化反应或酯化反应消除-OH
①CH3CH2OHCH2=CH2↑+H2O
②2CH3CH2OH+O22CH3CHO+2H2O
③CH3CH2OH+CH3COOHCH3COOC2H5+H2O。
(3)通过氧化反应或加成反应可消除-CHO
①2CH3CHO+O22CH3COOH
②CH3CHO+H2CH3CH2OH
(4)通过消去反应或水解反应可消除卤素原子
①CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
②CH3CH2Br+NaOHCH3CH2OH+NaBr
(5)通过水解反应消除酯基
①CH3COOC2H5+H2OCH3COOH+C2H5OH
②CH3COOCH2CH3+NaOHCH3CH2OH+CH3COONa
3.成环与开环的反应
(1)成环
①羟基酸分子内酯化
(内酯)+H2O
②二元酸和二元醇分子间酯化成环
+(环酯)+2H2O
③双烯合成反应
+
(2)开环
①环酯的水解反应
+2H2O+
②某些环状烯烃的氧化反应
HOOC(CH2)4COOH
CH3--(CH2)4COOH
三、官能团的转化和保护
1.典型的官能团的转化关系
2.官能团的保护
有机合成时,往往在有机物分子中引入多个官能团,但有时在引入某一个官能团时容易对其他官能团造成破坏,导致不能实现目标化合物的合成。因此,在制备过程中要把分子中的某些官能团通过恰当的方法保护起来,在适当的时候再将其转变回来,从而达到有机合成的目的。
(1)醇羟基的保护
R-OHR-O-R′R″-O-R′R″-OH
(2)酚羟基的保护
因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH反应,把-OH变为-ONa将其保护起来,待氧化后再酸化将其转变为-OH。
(3)碳碳双键的保护
碳碳双键也容易被氧化,在氧化其他基团前可以利用其与卤素单质、卤化氢等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。
例如,已知烯烃中在某些强氧化剂的作用下易发生断裂,因而在有机合成中有时需要对其进行保护,过程可简单表示如下:
①+Br2 +Zn+ZnBr2
②CH2=CHRCH2Cl-CH2RCH2Cl-CH2R′CH2=CHR′
(4)氨基(-NH2)的保护
例如,在对硝基甲苯合成对氨基苯甲酸的过程中应先把-CH3氧化成-COOH,再把-NO2还原为-NH2。防止当KMnO4氧化-CH3时,-NH2(具有还原性)也被氧化。
(5)醛基的保护
①醛基可被弱氧化剂氧化,为避免在反应过程中受到影响,对其保护和恢复过程为:
Ⅰ.Ⅱ.R-CHO
再如检验碳碳双键时,当有机物中含有醛基、碳碳双键等多种官能团时,可以先用弱氧化剂,如银氨溶液、新制Cu(OH)2悬浊液等氧化醛基,再用溴水、酸性KMnO4溶液等对碳碳双键进行检验。
②醛与醇反应生成缩醛:
+H2O
生成的缩醛比较稳定,与稀碱和氧化剂均难反应,但在稀酸中微热,缩醛会水解为原来的醛。
1.判断正误,正确的打“√”,错误的打“×”。
(1)有机合成应尽量选择步骤最少的合成路线,符合低价、绿色、环保等要求。( )
(2)只有通过取代反应才能引入—OH。( )
(3)通过加成反应可以同时引入两个卤素原子。( )
(4)某酯C6H12O2经水解后得到相同碳原子数的羧酸和醇,再把醇氧化得到丙酮(),则酯是C2H5COOCH(CH3)2。( )
(5)通过加成反应不能引入碳碳双键官能团。( )
(6)酯基官能团只能通过酯化反应得到。( )
(7)由CH3CH3→CH3CH2Cl→CH2===CH2→CH3CH2OH的转化过程中,经过的反应类型是取代反应→消去反应→加成反应。( )
(8)用盐析的方法分离提纯蛋白质。( )
(9)加聚反应可以使有机物碳链增长,取代反应不能。( )
(10)CH2===CHCHO能使酸性高锰酸钾溶液褪色,说明分子中含有碳碳双键。( )
(11)引入羟基只能通过取代反应实现。( )
(12)某有机物具有酸性,只可能含有羧基。( )
(13)某有机物可发生银镜反应,说明该有机物属于醛类。( )
【答案】(1) ( √ )(2) ( × )(3) ( √ )(4) ( √ )(5) ( × )(6) ( × )(7) ( √ )(8) ( √ )
(9) ( × )(10) ( × )(11) ( × )(12) ( × )(13) ( × )
1.由石油裂解产物乙烯制取HOCH2COOH,需要经历的反应类型有( )
A.氧化——氧化——取代——水解
B.加成——水解——氧化——氧化
C.氧化——取代——氧化——水解
D.水解——氧化——氧化——取代
【答案】A
【解析】 由乙烯CH2===CH2合成HOCH2COOH的步骤:CH2===CH2→CH3CHO→CH3COOH→Cl—CH2COOH→HOCH2COOH。故反应类型:氧化——氧化——取代——水解。
2.有机分析中,常用臭氧氧化分解来确定有机物中碳碳双键的位置与数目。如:
(CH3)2C===CH—CH3eq \(――――→,\s\up7(①O3),\s\d5(②Zn、H2O))(CH3)2C===O+CH3CHO
已知某有机物A经臭氧氧化分解后发生以下一系列的变化:
从B合成E通常经过多步反应,其中最佳次序是( )
A.水解、酸化、氧化 B.氧化、水解、酸化
C.水解、酸化、还原 D.氧化、水解、酯化
【答案】B
【解析】 本题考查有机合成最佳路线的分析和选择能力,体现科学探究与创新意识的学科核心素养。
知识点03 有机合成路线的设计及应用
一、有机合成路线的设计与实施
1.有机合成路线确定的要素
(1)基础:在掌握碳骨架构建和官能团转化基本方法的基础上。
(2)设计与操作:进行合理的设计与选择,确定合成路线,以较低的成本和较高的产率,通过简便而对环境友好的操作得到目标产物。
2.有机合成的过程
3.有机合成路线设计应遵循的四个原则
(1)符合绿色化学思想。
①有机合成中的原子经济性;
②原料的绿色化;
③试剂与催化剂的无公害性。
(2)原料价廉,原理正确。
(3)路线简捷,便于操作,条件适宜,安全可靠。
(4)易于分离,产率高。
4.有机合成的发展
(1)有机合成的技术和效率不断提高的影响因素
①新的有机反应;
②新试剂的不断发现;
③有机合成理论的发展
(2)发展过程
(3)有机合成发展的作用
①使人们能通过人工手段合成原本只能从生物体内分离、提取的天然产物。
②使人们可以根据实际需要设计合成具有特定结构和性能的新物质。
③为化学、生物、医学、材料等领域的研究和相关工业生产提供了坚定的物质基础。
④有力地促进了人类健康水平提高和社会发展进步。
二、有机合成的分析方法
1.正合成法
此法是采用正向思维方法,从已知原料入手,找出合成所需要的直接或间接的中间产物,逐步推向待合成有机物,其思维程序是原料中间产物产品。
2.逆合成法
此法是采用逆向思维方法,从产品的组成、结构、性质入手,找出合成所需要的直接或间接的中间产物,逐步推向已知原料,其思维程序是产品中间产物原料。
3.综合比较法
此法是采用综合思维的方法,将正向或逆向推导出的几种合成途径进行比较,从而得到最佳的合成路线。其思维程序是原料中间产物目标产物。
二、常见的有机合成路线
1.烃、卤代烃、烃的含氧衍生物之间的转化关系
烃R-H卤代烃R-X醇类R-OH醛类R-CHO羧酸R-COOH酯类RCOOR′
2.一元合成路线
R-CH=CH2卤代烃一元醇一元醛一元羧酸酯
3.二元合成路线
CH2=CH2CH2X-CH2X二元醇二元醛二元羧酸链酯、环酯、聚酯
4.芳香族化合物合成路线
(1)
(2)
1.判断正误,正确的打“√”,错误的打“×”。
(1)有机合成应尽量选择步骤最少的合成路线,符合低价、绿色、环保等要求。( )
(2)有机物间存在下列转化关系:
其中a是烃类,其余是烃的衍生物,若a的相对分子质量是42,则d是乙醛。( )
(3)有机合成的思路就是通过有机反应构建目标化合物的分子碳架,并引入或转化成所需的官能团。( )
(4)逆合成分析法可以简单表示为目标化合物→中间体Ⅱ→中间体Ⅰ→基础原料。( )
(5)为减少污染,有机合成不能使用辅助原料,不能有副产物。( × )
【答案】(1) ( √ )(2) ( × )(3) ( √ )(4) ( √ )(5) ( × )
1.根据某有机合成的片段:
写出以C2H5OH为原料合成乳酸()的路线(其他试剂任选)。
________________________________________________________________________
________________________________________________________________________
【答案】 CH3CH2OHeq \(――→,\s\up7(Cu/O2),\s\d5(△))CH3CHOeq \(――→,\s\up7(HCN))
2.维生素E是一种人体必需的脂溶性维生素,现已广泛应用于医药、营养品、化妆品等。天然的维生素E由多种生育酚组成,其中α-生育酚(化合物E)含量最高,生理活性也最高。下面是化合物E的一种合成路线,其中部分反应略去。
已知以下信息:
回答下列问题:
(1)A的化学名称为 。
(2)B的结构简式为 。
(3)反应物C含有三个甲基,其结构简式为 。
(4)反应⑤的反应类型为 。
(5)反应⑥的化学方程式为 。
(6)化合物C的同分异构体中能同时满足以下三个条件的有 个(不考虑立体异构体,填标号)。
ⅰ.含有两个甲基;
ⅱ.含有酮羰基(但不含C===C===O);
ⅲ.不含有环状结构。
a.4 b.6
c.8 d.10
【答案】(1) 3-甲基苯酚(或间甲基苯酚)。
(2) 。
(3) 。
(4) 加成反应 。
(5)
。
(6) c 。
【解析】 本题考查有机化学基础知识,考查的核心素养是证据推理与模型认知。
(1)由A的结构简式知,A为3-甲基苯酚(或间甲基苯酚)。
(2)间甲基苯酚和CH3OH发生类似题给已知信息a的反应生成B,结合B的分子式可知B的结构简式为。
(3)由题给已知信息b知与C发生反应生成,C中含有三个甲基,结合C的分子式可知C的结构简式为。
(4)由题给已知信息c知与HC≡CH发生加成反应生成D,则反应⑤的反应类型为加成反应。
(5)D()与H2发生加成反应生成,则反应⑥的化学方程式为+H2eq \(――→,\s\up7(Pd-Ag),\s\d5(△))。
(6)C的分子为C6H10O,满足题给条件的C的同分异构体有:①
共8个,其中含有手性碳的化合物的结构简式为
知识点01 研究有机化合物的一般方法
知识点02 有机合成
知识点03 有机合成路线的设计及应用
混合物
试剂
分离提纯的方法
苯(苯甲酸)
NaOH溶液
分液
乙酸乙酯(乙酸)
饱和Na2CO3溶液
溴苯(溴)
NaOH溶液
苯(乙苯)
KMnO4酸性溶液、NaOH溶液
乙醇(水)
CaO
蒸馏
乙醛(乙酸)
NaOH溶液
苯甲酸(苯甲酸钠)
水
重结晶
官能团或原子团
不饱和度
官能团或原子团
不饱和度
一个碳碳双键
1
一个碳碳三键
2
一个羰基
1
一个苯环
4
一个脂环
1
一个氰基
2
一个硝基
1
官能团种类
试剂
判断依据
碳碳双键或碳碳三键
溴的四氯化碳溶液
橙红色溶液褪色
酸性KMnO4溶液
紫色溶液褪色
卤素原子
NaOH溶液(加热)、稀硝酸、AgNO3溶液
有沉淀产生,根据沉淀的颜色判断卤素的种类
醇羟基
钠
缓慢反应,有氢气放出
酚羟基
FeCl3溶液
显色
浓溴水
有白色沉淀产生
醛基
银氨溶液(水浴加热)
有银镜生成
新制氢氧化铜悬浊液(加热煮沸)
有砖红色沉淀产生
羧基
NaHCO3溶液
有二氧化碳气体放出
选项
实验目的
分离或提纯方法
原理
A
分离溶于水中的碘
乙醇萃取
碘在乙醇中的溶解度较大
B
除去乙醇中的乙酸
加入CaO固体后蒸馏
乙酸转化为难挥发的乙酸钙
C
除去甲烷中的乙烯
通过酸性KMnO4溶液洗气
乙烯与酸性KMnO4溶液反应
D
分离汽油和四氯化碳
分液
四氯化碳和汽油的密度不同
时间
发展过程
20世纪初
维尔施泰特通过十余步反应合成颠茄酮,总产率仅有0.75%
十几年后,罗宾逊改进了合成思路,仅用3步反应便完成合成,总产率达90%
20世纪中后期
伍德沃德与多位化学家合作,成功合成了一系列结构复杂的天然产物,促进了有机合成技术和有机反应理论的发展
科里提出了系统化的逆合成概念,开始利用计算机来辅助设计合成路线,让合成路线的设计逐步成为有严密思维逻辑的科学过程,使有机合成进入了新的发展阶段。
知识清单23 盐类的水解(含答案) 2025年高考化学一轮复习知识清单: 这是一份知识清单23 盐类的水解(含答案) 2025年高考化学一轮复习知识清单,文件包含知识清单23盐类的水解教师版2025年高考化学一轮复习知识清单docx、知识清单23盐类的水解学生版2025年高考化学一轮复习知识清单docx等2份学案配套教学资源,其中学案共28页, 欢迎下载使用。
知识清单21 电离平衡(含答案) 2025年高考化学一轮复习知识清单: 这是一份知识清单21 电离平衡(含答案) 2025年高考化学一轮复习知识清单,文件包含知识清单21电离平衡教师版2025年高考化学一轮复习知识清单docx、知识清单21电离平衡学生版2025年高考化学一轮复习知识清单docx等2份学案配套教学资源,其中学案共17页, 欢迎下载使用。
知识清单04 物质的量(含答案) 2025年高考化学一轮复习知识清单: 这是一份知识清单04 物质的量(含答案) 2025年高考化学一轮复习知识清单,文件包含知识清单04物质的量教师版2025年高考化学一轮复习知识清单docx、知识清单04物质的量学生版2025年高考化学一轮复习知识清单docx等2份学案配套教学资源,其中学案共30页, 欢迎下载使用。












