




初中化学人教版(2024)九年级下册课题2 溶解度教学演示课件ppt
展开1.了解固体物质溶解度和气体溶解度的含义;知道影响溶解度的一些因素2.根据溶解度表提供的数据绘制溶解度曲线,通过分析讨论溶解度表和溶解度曲线的含义,初步学会数据处理方法3.通过溶解度的学习,会利用有关溶解度的知识解释身边的一些现象;感受化学对改善生活和促进社会发展的积极作用
冬天捞碱
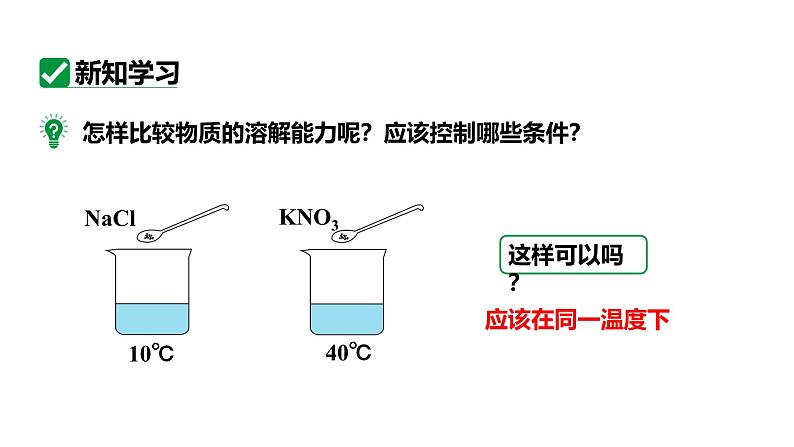
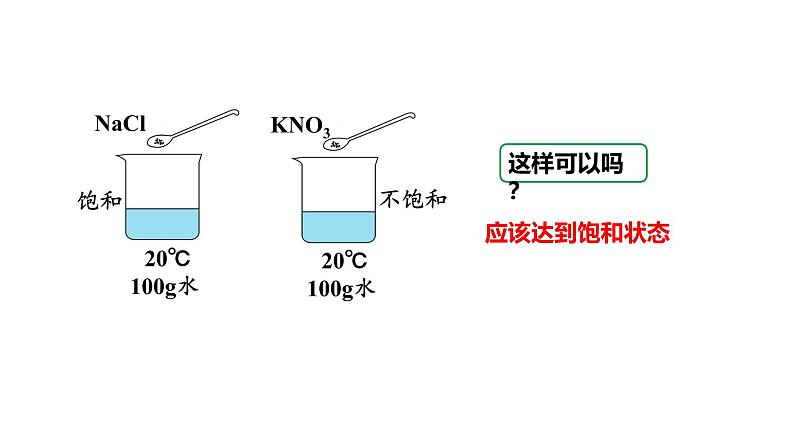
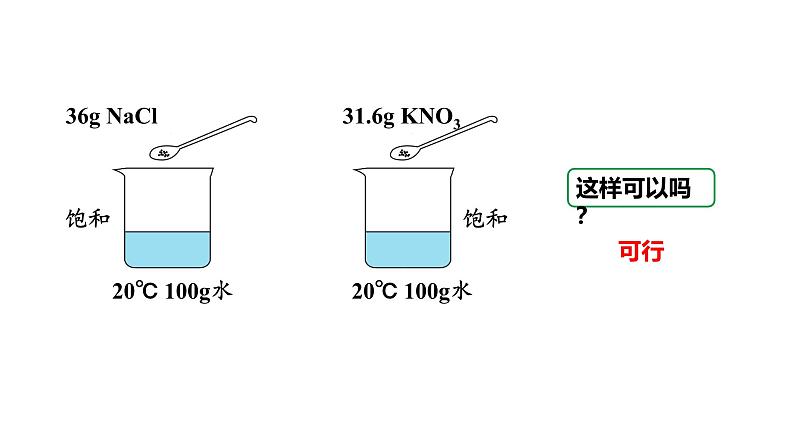
比较固体物质在溶剂中溶解的最大量
溶解度(s):在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
1.内因:溶质、溶剂本身的性质(或溶质和溶剂的种类)。2.外因:温度。固体物质溶解度与溶剂量的多少没有关系,因为概念中溶剂的量已经规定为100g,所以在外部因素中固体物质溶解度只与温度有关。
影响固体物质溶解度的因素
1.“20℃时,氯化钠固体的溶解度为36.0g”,其含义是什么?
在20℃时,100g水中溶解36.0g氯化钠固体,溶液达到饱和。
在20℃时,100g水中最多可溶解36.0g氯化钠固体。
2. “20℃时硝酸钾的溶解度是31.6g”,这句话的含义是什么?将其关系代入下表:
1. 把20克某物质溶解在100克水里恰好制成饱和溶液,这种物质的 溶解度就是20克。2. 20℃时10克氯化钠溶解在水里制成饱和溶液,故20℃时氯化钠 的溶解度是10克。
判断下列说法是否正确。若不正确,则指明错误原因。
3. 20℃时10克氯化钠可溶解在100克水里,故20℃时氯化钠的溶解度是10克。4. 20℃时36克食盐溶解在100克水中恰好饱和,故20℃时食盐的溶解度是36。
未指明溶液的状态是饱和
溶解性只是定性地说明某种物质在某种溶剂里溶解能力的大小,而溶解度是定量衡量某种物质在某种溶剂里溶解性大小的尺度。
固体物质溶解度与溶解性的关系
1. 20℃时,食盐的溶解度是36g,它的含义是( )A. 20 ℃时,136g饱和食盐水中含有36g食盐B. 在100 g水中最多溶解36g食盐C. 20 ℃时,饱和食盐水中含有36g食盐D. 20 ℃时,100g饱和食盐水中含有36g食盐
同一固体物质在不同温度下的溶解度不同,该用什么方法表示该物质的溶解度呢?
用横坐标表示温度,纵坐标表示溶解度绘制出溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
从绘制的溶解度曲线上,查出上述几种物质在25℃和85℃时的溶解度。
根据下图,说明固体物质的溶解度随温度的变化有什么规律。从溶解度曲线中还能获得哪些信息?
陡升型:大多数固体物质的溶解度随温度的升高而增大,表现为曲线坡度陡增,如KNO3、NH4NO3等。
缓升型:少数固体物质的溶解度受温度变化的影响较小,表现为曲线坡度比较平缓,如NaCl。
下降型:极少数固体物质的溶解度随温度的升高而减小,表现为曲线坡度下降,如Ca(OH)2。
由溶解度曲线获得的信息
曲线a:物质甲的溶解度随温度的升高而增大,受温度变化影响较大。
曲线b:物质乙的溶解度随温度的升高而缓慢增大,受温度变化影响较小。
M点:在t2℃时物质甲和物质乙的溶解度相等,都为S2g。
N点:物质甲在t1℃时的溶解度为S1g。
P点:物质乙在t3℃时的溶解度为S3g。
当甲中含有少量乙(如KNO3中含有少量的NaCl)时,可采用冷却热饱和溶液(降温结晶)法分离(或提纯)出物质甲。
当乙中含有少量甲(如NaCl中含有少量的KNO3)时,可采用蒸发结晶法分离(或提纯)出物质乙。
从表中可以看出,食盐的溶解度随温度变化很小,而纯碱的溶解度随温度的变化很大。
当季节从夏天变到冬天时,随着盐碱湖水温度的下降,湖中食盐的溶解度变化很小,而纯碱的溶解度却从38.0g 降至7.0 g,这样就会有纯碱晶体从湖水中析出,并浮在湖面上。于是人们在冬天就可以在湖边直接捞出碱来。
到了夏天,湖水温度升高后,虽然食盐和纯碱的溶解度十分接近,但由于冬天纯碱从湖水中析出并被捞上,导致湖水中纯碱浓度降低,而食盐的浓度几乎没变,即食盐的浓度远远大于纯碱的浓度。所以,水份蒸发后,食盐会从湖水中以晶体的形态析出,而纯碱却不会从湖水中析出。
1. 如图是甲、乙两种物质的溶解度曲线,下列叙述正确的是( )A.20℃时,甲的溶解度大于乙的溶解度B.40℃时,甲、乙两种物质的溶解度相等C.采用降温的方法可以将乙的不饱和溶液转化为饱和溶液D.60℃时,在100g水中加入100g甲,充分溶解后溶液质量为200g
气体的溶解度是指该气体的压强为101kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积。
四要素:1. 条件:在压强为101kPa、一定温度时。2. 标准:1体积水。3. 状态:达到饱和状态。4. 单位:体积。
在压强不变的条件下,温度越高,气体的溶解度越小
在温度不变的条件下,压强越大,气体的溶解度越大
气体溶解度和固体溶解度的比较
1. 生活中的下列现象,不能说明气体的溶解度随温度的升高而减小的是( )A.烧开水时,水沸腾前有气泡冒出B.喝下冰镇汽水后,感觉到有气体冲到鼻腔C.打开啤酒瓶盖时,有大量的泡沫溢出D.夏季午后池塘里的鱼常跃出水面
温度:溶解度曲线随温度变化的规律
1.影响固体物质溶解度大小的因素有( )①溶质的性质 ②温度 ③压强 ④溶质的质量 ⑤溶剂的性质 ⑥溶解时是否搅拌或振荡 ⑦固体物质的颗粒大小A. ①②⑤ B. ①②③ C. ①④⑥ D. ②⑥⑦
2. (2022枣庄节选)硝酸钾的溶解度曲线如图所示,回答下列问题:(1)图中P点所表示的 KNO3溶液________(填“饱和”或“不饱和”)。(2)将 KNO3的饱和溶液变为不饱和溶液,可采用的方法有_____________(写一种即可)。(3)20 ℃时,将 20 g KNO3固体加入到50 g水中,充分溶解,所得溶液的质量为______g。
3. 固体甲、乙、丙在不同温度下的溶解度如下表所示,甲、乙、丙从溶液中析出的晶体不含结晶水。下列说法正确的是( ) A. 固体甲的溶解度随温度的升高而增大B. 20 ℃时,丙溶液中溶质和溶剂质量比为31.6∶100C. 分别将等质量的乙、丙饱和溶液由60 ℃降温到20 ℃,溶质质量大小:丙>乙D. 分别将等质量的甲、丙饱和溶液由60 ℃降温到20 ℃,溶剂质量大小:甲>丙
在干净的玻璃杯中加入约20mL开水,然后加入白糖,用筷子搅拌,直到有少量白糖不再溶解为止。将一根细线的一端浸入白糖溶液中,另一端留在玻璃杯外,用硬纸片盖住玻璃杯(防止灰尘进入溶液),静置。过4~5天或更长时间,拿掉硬纸片,观察溶液表面、玻璃杯壁和细线上白糖晶体的生成。
初中化学人教版九年级下册课题2 溶解度作业ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度作业ppt课件,共7页。PPT课件主要包含了图K9-2-5等内容,欢迎下载使用。
人教版九年级下册第九单元 溶液课题2 溶解度教学ppt课件: 这是一份人教版九年级下册第九单元 溶液课题2 溶解度教学ppt课件,共17页。PPT课件主要包含了课程要求,知识点精讲,课堂检测,溶解度曲线,溶解度,不饱和,硝酸钾,氯化钠,蒸发溶剂,氢氧化钙等内容,欢迎下载使用。
人教版课题2 溶解度教学课件ppt: 这是一份人教版课题2 溶解度教学课件ppt,共19页。PPT课件主要包含了课程要求,知识点精讲,课堂检测,课前预习,在20℃,一定温度,态物质,饱和状态,错未指明,错未指明是饱等内容,欢迎下载使用。













