

高考化学二轮复习核心考点逐项突破专题一0三水的电离与溶液的pH(专讲)(原卷版+解析)
展开核心考点1、水的电离溶液的酸碱性
1.水的电离
(1)任何条件下,水电离出的c(H+)=c(OH-);常温下,离子积常数KW=1.0×10-14。
(2)酸、碱抑制水的电离, pH相等的盐酸、醋酸对水的电离的抑制程度相同;浓度相等的盐酸和醋酸,盐酸对水的电离的抑制程度更大。
(3)能水解的正盐则促进水的电离。
(4)溶液中的c(H+)与水电离出的c(H+)的区别
①室温下水电离出的c(H+)=c(OH-)=1.0×10-7 ml/L,若某溶液中水电离出的c(H+)<1.0×10-7 ml/L,则可判断该溶液呈酸性或碱性,电解质电离产生的H+或OH-抑制了水的电离;若某溶液中水电离出的c(H+)>1.0×10-7 ml/L,则可判断该溶液中存在能水解的盐,从而促进了水的电离。
②室温下,溶液中c(H+)>1.0×10-7 ml/L,说明溶液是酸性溶液或水解呈酸性的盐溶液;溶液中c(H+)<1.0×10-7 ml/L,说明溶液是碱性溶液或水解呈碱性的盐溶液。
2.溶液的酸碱性及pH
(1)溶液酸碱性与pH:在任何温度下的中性溶液中c(H+)=c(OH-)=eq \r(KW),常温下中性溶液pH=7,温度升高时,中性溶液的pH<7。
(2)溶液pH的计算方法
①强酸溶液pH=-lg c(H+) ,若两强酸溶液(pH相差2以上)等体积混合,混合后溶液的pH等于混合前溶液pH小的加0.3。
②强碱溶液pH=-lg c(H+)=14-lg c(OH-),若两强碱溶液(pH相差2以上)等体积混合,混合后溶液的pH等于混合前溶液pH大的减0.3。
③强酸与强碱混合:若恰好中和,pH=7;若剩余酸,先求中和后剩余的c(H+),再求pH;若剩余碱,先求中和后剩余的c(OH-),再通过KW求出c(H+),最后求pH。
【归纳提升】1.一个基本不变
相同温度下,不论是纯水还是稀溶液,水的离子积常数不变。应用这一原则时需要注意两个条件:水溶液必须是稀溶液;温度必须相同。
2.两个判断标准
(1)任何温度
c(H+)>c(OH-),酸性;c(H+)=c(OH-),中性;c(H+)
pH>7,碱性;pH=7,中性;pH<7,酸性。
1.【2022年1月浙江卷】已知25℃时二元酸H2A的Ka1=1.3×10-7,Ka2=7.1×10-15。下列说法正确的是
A.在等浓度的Na2A.NaHA溶液中,水的电离程度前者小于后者
B.向0.1ml·L-1的H2A溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则H2A的电离度为0.013%
C.向H2A溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
D.取pH=a的H2A溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2.(2021.1·浙江真题)25℃时,下列说法正确的是
A.NaHA溶液呈酸性,可以推测H2A为强酸
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 ml·L-1、0.10ml·L-1的醋酸溶液的电离度分别为α1、α2,则α1<α2
D.100 mL pH=10.00的Na2CO3溶液中水电离出H+的物质的量为1.0×10-5ml
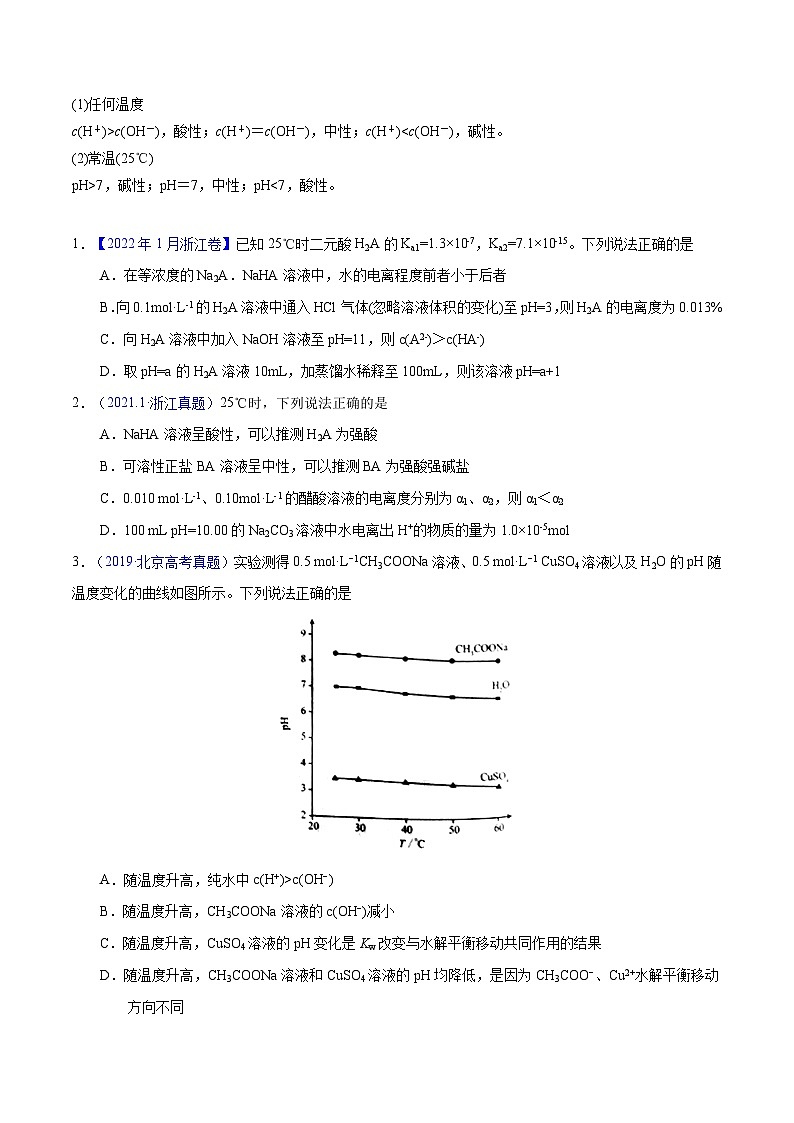
3.(2019·北京高考真题)实验测得0.5 ml·L−1CH3COONa溶液、0.5 ml·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
A.随温度升高,纯水中c(H+)>c(OH−)
B.随温度升高,CH3COONa溶液的c(OH−)减小
C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同
4.(2019·上海高考真题)25℃时,0.005ml/LBa(OH)2中H+浓度是( )
A.1×ml/LB.1×ml/L
C.5×ml/LD.5×ml/L
5.(2017·上海高考真题)下列物质的水溶液呈酸性,并且使水的电离平衡向正方向移动的是:
A.Na2CO3 B.NH4Cl C.H2SO4 D.NaHCO3
6.(2017·浙江高考真题)下列说法不正确的是
A.pH<7的溶液不一定呈酸性
B.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
C.在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl-)=c(CH3COO-)
D.氨水和盐酸反应后的溶液,若c(Cl―)=c(NH4+),则溶液呈中性
1.(2021·湖北·统考二模)常温下,向1 L浓度为0.4 ml·L-1的乙醇酸[CH2(OH)COOH]溶液中加入8 g NaOH固体得到X溶液,将X溶液平均分成两等份,一份通入HCl气体,得到溶液Y,另一份加入NaOH固体得到溶液Z,溶液Y、Z的pH随所加物质的物质的量的变化情况如图所示(体积变化忽略不计)。下列说法正确的是
A.b点对应曲线代表的是加入HCl的曲线
B.溶液中水的电离程度:c>b
C.a点:c(Na+)>c[CH2(OH)COO-]>c(H+)>c(OH- )
D.稀释Y溶液后,溶液中不变
2.(2020·天津·模拟预测)用pH试纸测定溶液的pH,下列叙述正确的是
A.测得某浓度的NaClO溶液的pH为10
B.常温下测得NH4Cl溶液pH约为4.1
C.用湿润的pH试纸测pH相同的盐酸和醋酸溶液的pH,误差较大的是盐酸
D.在试管内放入少量溶液并煮沸,把pH试纸放在管口观察其颜色并与标准比色卡比较
3.(2022·北京·模拟预测)常温下,将pH相同、体积均为V0的盐酸和醋酸分别加水稀释至V,pH随的变化如图所示。下列说法不正确的是
A.曲线②表示CH3COOH溶液
B.c点溶液的导电性比b点溶液的导电性强
C.盐酸和醋酸分别稀释到pH=4时,c(Cl-)>c(CH3COO-)
D.c点酸的总浓度大于a点酸的总浓度
4.(2022·山东·模拟预测)室温下,分别向体积均为20mL、 浓度均为0.1ml·L-1的HX、HY溶液中,滴加相同浓度的Ba(OH)2溶液(Ba2+与X-、Y-均不反应)。随着Ba(OH)2溶液的加入,由水电离产生的c(H+)的变化趋势如图所示。下列说法错误的是
A.相同条件下,Ka(HX)>Ka(HY)
B.M点溶液显中性,溶液中c(Y-)
D.T点溶液中阴离子浓度之和大于M点
5.(2022·湖南邵阳·邵阳市第二中学校考模拟预测)H3PO2是一种一元弱酸,25℃时,在20.0 mL0.1 ml/LH3PO2溶液中滴加0.1 ml/L氢氧化钠溶液V mL,混合溶液的pH与的关系如图所示。下列说法正确的是
A.a=5.77
B.m点时,加入的氢氧化钠溶液的体积大于20 mL
C.25℃时,H3PO2的电离常数Ka的数量级为10-2
D.当V=20.0时,溶液中存在关系:
核心考点2溶液酸碱性
1.pH及其测量
(1)计算公式:pH=-lg c(H+)。
适用范围:c(H+)和c(OH-)小于1 ml·L-1的稀溶液。pH越小,表示酸性越强。
(2)pH测量的三种方法
①pH试纸法
用镊子夹取一小块pH试纸放在玻璃片或表面皿上,用洁净的玻璃棒蘸取待测液点在试纸的中央,变色后与标准比色卡对照,即可确定溶液的pH。
注意:a.pH试纸使用前不能用蒸馏水润湿,否则待测液因被稀释可能会产生误差。b.pH试纸不能测定氯水的pH。c.用广泛pH试纸读出的pH只能是整数。
②pH计测量法。 仪器pH计可精确测定试液的pH(读至小数点后2位)。
③酸碱指示剂
酸碱指示剂能粗略测定溶液的pH范围。常见酸碱指示剂的变色范围如下表所示:
2.溶液酸碱性的判断
(1)溶液酸碱性,取决于溶液中c(H+)和c(OH-)的相对大小。常温下,如下表所示:
【注意】用pH判断溶液酸碱性时,要注意温度。如温度升高到100℃时,pH=6,但仍为中性,pH<6显酸性,pH>6显碱性;若溶液未注明温度,一般认为是常温,以pH=7为中性。
(2)[H+]、pH与溶液酸碱性的关系
pH是酸碱性的量度,常温下三者关系如下图所示:
(3)使用范围
pH的取值范围为0~14,即只适用于c(H+)≤1 ml·L-1或c(OH-)≤1 ml·L-1的电解质溶液,当c(H+)或c(OH-)≥1 ml·L-1时,直接用c(H+)或c(OH-)表示溶液的酸碱性。
3.溶液pH计算的思维模板
强酸、强碱等体积溶液混合(常温下)
(1)若ΔpH(pH的差值)≥2的两种强酸溶液等体积混合,酸溶液的pH≈pH小+0.3;如pH=3和pH=5的两种HCl等体积混合,pH≈3+0.3=3.3;
(2)若ΔpH(pH的差值)≥2的两种强碱溶液等体积混合,碱溶液的pH≈pH大-0.3;如pH=9和pH=12的两种NaOH等体积混合,pH≈12-0.3=11.7。
(3)强酸与强碱的等体积混合:
①pH酸+pH碱=14时,pH混=7;
②pH酸+pH碱<14时,pH混≈pH酸+0.3;
③pH酸+pH碱>14时,pH混≈pH碱﹣0.3;
4.四条判断规律
(1)正盐溶液
强酸强碱盐显中性,强酸弱碱盐(如NH4Cl)显酸性,强碱弱酸盐(如CH3COONa)显碱性。
(2)酸式盐溶液
NaHSO4显酸性(NaHSO4 AUTOTEXT == \* MERGEFORMAT =Na++H++SO eq \\al(2-,4))、NaHSO3、NaHC2O4、NaH2PO4水溶液显酸性(酸式根电离程度大于水解程度);NaHCO3、NaHS、Na2HPO4水溶液显碱性(酸式根水解程度大于电离程度)。
注意 因为浓度相同的CH3COO-与NH+4的水解程度相同,所以CH3COONH4溶液显中性,而NH4HCO3溶液略显碱性。
(3)弱酸(或弱碱)及其盐1∶1混合溶液
①1∶1的CH3COOH和CH3COONa混合液呈酸性。
②1∶1的NH3·H2O和NH4Cl混合溶液呈碱性。
(对于等浓度的CH3COOH与CH3COO-,CH3COOH的电离程度大于CH3COO-的水解程度)。
(4)酸碱pH之和等于14等体积混合溶液
pH和等于14的意义:酸溶液中的氢离子浓度等于碱溶液中的氢氧根离子的浓度。
①已知酸、碱溶液的pH之和为14,则等体积混合时:
eq \x(强酸、强碱)eq \(――→,\s\up7(恰好中和))pH=7
eq \x(强酸、弱碱)eq \(――→,\s\up7(碱过量))pH>7
eq \x(弱酸、强碱)eq \(――→,\s\up7(酸过量))pH<7
②已知酸、碱溶液的pH之和为14,若混合后溶液的pH为7,溶液呈中性,则
eq \x(强酸、强碱)―→V酸∶V碱=1∶1
eq \x(强酸、弱碱)―→V酸∶V碱>1∶1
eq \x(弱酸、强碱)―→V酸∶V碱<1∶1
③强酸、强碱等体积混合后溶液酸、碱性的判断
5. 图像法理解一强一弱的稀释规律
(1)相同体积、相同浓度的盐酸、醋酸
①加水稀释相同的倍数,醋酸的pH大。
②加水稀释到相同的pH,盐酸加入的水多。
(2)相同体积、相同pH的盐酸、醋酸
①加水稀释相同的倍数,盐酸的pH大。
②加水稀释到相同的pH,醋酸加入的水多。
【解题策略】 看“三角度”,突破酸HA强弱的判断方法
(1)从水解的角度分析,取其钠盐(NaA)溶于水,测其pH,若pH>7,则说明HA是弱酸,若pH=7,则说明HA是强酸。
(2)从是否完全电离的角度分析,配制一定物质的量浓度的HA溶液(如0. 1 ml·L-1),测其pH,若pH>1,则说明HA是弱酸,若pH=1,则说明HA是强酸。
(3)从电离平衡移动的角度分析,如①向HA溶液中加水稀释100倍后,溶液pH增大值小于2的是弱酸,pH增大2的是强酸;②向HA溶液中加入NaA晶体,溶液pH增大的是弱酸,pH不变的是强酸。
1.【2022年1月浙江卷】已知25℃时二元酸H2A的Ka1=1.3×10-7,Ka2=7.1×10-15。下列说法正确的是
A.在等浓度的Na2A.NaHA溶液中,水的电离程度前者小于后者
B.向0.1ml·L-1的H2A溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则H2A的电离度为0.013%
C.向H2A溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
D.取pH=a的H2A溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2.(2021.1·浙江真题)25℃时,下列说法正确的是
A.NaHA溶液呈酸性,可以推测H2A为强酸
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010ml·L-1、0.10ml·L-1的醋酸溶液的电离度分别为α1、α2,则α1<α2
D.100mLpH=10.00的Na2CO3溶液中水电离出H+的物质的量为1.0×10-5ml
3.(2019·北京高考真题)实验测得0.5 ml·L−1CH3COONa溶液、0.5 ml·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
A.随温度升高,纯水中c(H+)>c(OH−)
B.随温度升高,CH3COONa溶液的c(OH−)减小
C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同
4.(2017·浙江高考真题)下列说法不正确的是
A.pH<7的溶液不一定呈酸性
B.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
C.在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl-)=c(CH3COO-)
D.氨水和盐酸反应后的溶液,若c(Cl―)=c(NH4+),则溶液呈中性
5.(2017·浙江高考真题)下列物质的水溶液不能使酚酞变红的是
A.NaOHB.Na2CO3C.NaClD.NH3
【答案】C
【解析】A.NaOH是强碱,溶液显碱性,能使酚酞变红,不选;B.Na2CO3属于强碱弱酸盐,水解后溶液显碱性,能使酚酞变红,不选;C.NaCl是强酸强碱盐,溶液显中性,不能使酚酞变红,选;D.NH3的水溶液显碱性,能使酚酞变红,不选;故选C。
6.(2008·全国高考真题)实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4,石蕊:50~8.0,酚酞:8.2~10.0,用0.1000ml·L-1NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述正确的是( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
1.有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是 (填“正确的”或“错误的”),其理由是
。
(2)如不正确,请分析是否一定有误差:
。
(3)若用此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是
。
2. T ℃时,水的离子积为KW,该温度下,将a ml·L-1一元酸HA与b ml·L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是( )
A.混合液pH=7
B.混合液中,c(H+)=eq \r(KW)
C.a=b
D.混合液中,c(B+)=c(A-)+c(OH-)
3. 溶液的酸碱性可用酸度(AG)表示[AG=lgc(H+)c(OH−)],室温下,向浓度均为0.1ml/L体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,AG随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )
A.HX、HY均为弱酸
B.a点由水电离出的c(H+)=1.0×l0﹣13ml•L﹣l
C.c点溶液中:c(Y﹣)<c(Na+)<c(HY)
D.b点时,溶液的pH=7,酸碱恰好完全中和
核心考点3 中和滴定
1.定义:利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法称为酸碱中和滴定。
注意:(1)酸碱恰好中和是指酸与碱按化学方程式中化学计量数关系恰好完全反应生成正盐。
(2)酸碱恰好中和时溶液不一定呈中性,最终溶液的酸碱性取决于生成盐的性质,强酸强碱盐的溶液呈中性,强碱弱酸盐的溶液呈碱性,强酸弱碱盐的溶液呈酸性。
2.实质:酸电离出的 H+与碱电离出的OH- 以等物质的量的关系结合成H2O 的反应,即H++OH-=H2O。
3.中和滴定原理:
对于反应:H+ + OH- = H2O
1 ml 1 ml
c(H+)V(H+) c(OH-)V(OH-)
即可得c(H+)V(H+)=c(OH-)V(OH-)
在中和反应中使用一种已知浓度的酸(或碱)溶液与未知浓度的碱(或酸)溶液完全中和,测出二者所用的体积,根据化学方程式中酸、碱化学计量数关系求出未知浓度溶液的浓度。
计算公式:(以一元酸与一元碱的滴定为例)。
4.实验用品
(1)仪器
酸式滴定管(如图A)、碱式滴定管(如图B)、锥形瓶、滴定管夹、铁架台等。
注意:①酸式、碱式滴定管的异同
②滴定管的优点是易于控制所滴加液体,读数比较精确,可精确到小数点后两位,估读到0.01ml,如24.00ml、23.36 ml,最后一位是估读值。滴定管的“0”刻度在上,往下刻度值越来越大,且容积大于其最大刻度值,因为下面有一段没有刻度。滴定时,所以溶液不得超过最低刻度。
③关闭活塞,加水观察活塞周围有无水渗出;旋转活塞180°再检验有无水渗出。
(2)试剂
标准液、待测液、指示剂、蒸馏水。
5.常用酸碱指示剂及变色范围
6.滴定终点的判断
7.酸碱中和滴定实验操作(以酚酞作指示剂,标准盐酸滴定待测氢氧化钠溶液为例)
(1)滴定前的准备
①查漏:检查滴定管的活塞是否灵活、滴定管是否漏水。
②洗涤:滴定管、锥形瓶均需用蒸馏水洗涤干净。
③润洗:用待盛溶液将滴定管润洗2~3次,以保证装入溶液时不改变溶液的浓度。注意:锥形瓶水洗后不能进行润洗。
④装液:将酸、碱溶液分别装入相应的滴定管中,并使液面位于“0”刻度或“0”刻度上方 2~3cm处。
⑤排气:调节滴定管活塞(或挤压玻璃球),赶走气泡使滴定管尖嘴部分充满溶液。
⑥调液面:使液面处于“0”刻度或“0”刻度以下某一刻度处。
⑦记录:读数时视线应与溶液凹液面最低处相平,记录初始液面刻度刻度。
(2)滴定
①用碱式滴定管(或移液管)取一定体积的待测液于锥形瓶中,并滴入2~3滴酚酞试剂,把锥形瓶放在酸式滴定管下面。
②用左手控制活塞将溶液逐滴滴至锥形瓶内,右手不断摇动锥形瓶,滴至溶液变至无色且半分钟内不再恢复红色,记下刻度。
(3)终点判断
等到滴入最后一滴标准液,溶液由红色变为无色,且在30s内不恢复原来的颜色,视为滴定终点并记录标准液的体积。
注意:当滴入最后一滴××标准溶液后,溶液变成××色,且半分钟内不恢复原来的颜色,即可认为已经达到滴定终点。
①最后一滴:必须说明是滴入“最后一滴”溶液。
②颜色变化:必须说明滴入“最后一滴”溶液后溶液的颜色变化。
③30s:必须说明溶液颜色变化后“30s内不恢复原来的颜色”。
(4)数据处理
按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据原理计算。
8.误差分析的方法(以一元酸滴定一元碱为例)
(1)原理:依据原理c(标准)·V(标准)=c(待测)·V(待测),所以,因为c(标准)与V(待测)已确定,所以只要分析出不正确操作引起V(标准)的变化,即分析出结果。若用标准液滴定待测液,消耗标准液变多,则c(待测)偏高;消耗标准液变少,则c(待测)偏低。
(2)常见的因操作不正确而引起的误差
以标准酸溶液滴定未知浓度的碱溶液(酚酞作指示剂)为例,常见的因操作不正确而引起的误差有
【衔接扩展】在酸碱中和滴定过程中,开始时由于被滴定的酸(或碱)浓度较大,滴入少量的碱(或酸)对其pH的影响不大。当滴定接近终点(pH=7)时,很少量(一滴,约0.04 mL)的碱(或酸)就会引起溶液pH突变(如图所示)。
【易错辨析】
(1)滴定管在使用前要查漏、润洗,酸式滴定管可以盛放酸性、中性、氧化性的物质;碱式滴定管盛放碱性物质。
(2)在进行实验时,为了减少实验偶然性带来的误差,要进行多次实验,一般进行三次,若其中一次误差太大,要舍弃,取其平均值,根据c(碱)· V (碱)=c(酸)·V(酸)计算待测溶液的浓度。
(3)通常会引起实验误差的步骤有洗涤、取液、滴定、读数等,要具体问题具体分析,然后判断其造成的影响。
1.【2022年6月浙江卷】时,向浓度均为的盐酸和醋酸的混合溶液中逐滴加入的溶液(醋酸的;用的溶液滴定等浓度的盐酸,滴定终点的突跃范围4.3~9.7)。下列说法不正确的是
A.恰好中和时,溶液呈碱性
B.滴加溶液至的过程中,发生反应的离子方程式为:
C.滴定过程中,
D.时,
2.【2022年1月浙江卷】某同学在两个相同的特制容器中分别加入20mL0.4ml·L-1Na2CO3溶液和40mL0.2ml·L-1NaHCO3溶液,再分别用0.4ml·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
下列说法正确的的是
A.图中甲、丁线表示向NaHCO3溶液中滴加盐酸,乙、丙线表示向Na2CO3溶液中滴加盐酸
B.当滴加盐酸的体积为V1mL时(a点、b点),所发生的反应用离子方程式表示为:HCO+H+=CO2↑+H2O
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.Na2CO3和NaHCO3溶液中均满足:c(H2CO3)-c(CO)=c(OH-)-c(H+)
3.(2021·湖南真题)常温下,用的盐酸分别滴定20.00mL浓度均为三种一元弱酸的钠盐溶液,滴定曲线如图所示。下列判断错误的是
A.该溶液中:
B.三种一元弱酸的电离常数:
C.当时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
4.(2020·全国高考真题)以酚酞为指示剂,用0.1000 ml·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数:δ(A2-)=c(A2-)c(H2A)+c(HA-)+c(A2-)]
下列叙述正确的是
A.曲线①代表δ(H2A),曲线②代表δ(HA-)
B.H2A溶液的浓度为0.2000 ml·L−1
C.HA−的电离常数Ka=1.0×10−2
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
5.(2020·浙江高考真题)室温下,向盐酸中滴加溶液,溶液的pH随溶液体积的变化如图。已知。下列说法不正确的是( )
A.与盐酸恰好完全反应时,
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.时,
1. 室温下向10 mL 0.1 ml·L-1NaOH溶液中加入0.1 ml·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
2. 如图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是( )
A.盐酸的物质的量浓度为 1 ml·L-1
B.P点时反应恰好完全,溶液呈中性
C.曲线a是盐酸滴定氢氧化钠的滴定曲线
D.酚酞不能用作本实验的指示剂
3. 室温时,将0.10 ml·L-1 NaOH溶液滴入20.00 mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积的变化曲线如图所示。当V(NaOH)=20.00 mL,二者恰好完全反应。则下列有关说法不正确的是( )
A.该一元酸溶液浓度为0.10 ml·L-1
B.a、b、c点的水溶液导电性依次增强
C.室温时,HA的电离常数Ka≈1×10-5
D.a点和c点所示溶液中H2O的电离程度相同指示剂
变色范围的pH
石蕊
<5红色
5~8紫色
>8蓝色
甲基橙
<3.1红色
3.1~4.4橙色
>4.4黄色
酚酞
<8.2无色
8.2~10浅红色
>10红色
相对大小
c(H+)大小
pH
溶液的酸碱性
c(H+)>c(OH-)
c(H+)>1×10-7 ml·L-1
<7
酸性溶液
c(H+)=c(OH-)
c(H+)=1×10-7ml·L-1
=7
中性溶液
c(H+)<c(OH-)
c(H+)<1×10-7ml·L-1
>7
碱性溶液
指示剂
变色范围的pH
石蕊
<5.0红色
5.0~8.0紫色
>8.0蓝色
甲基橙
<3.1红色
3.1~4.4橙色
>4.4黄色
酚酞
<8.2无色
8.2~10.0浅红色
>10.0红色
步骤
操作
V(标准)
c(待测)
洗涤
酸式滴定管未用标准酸溶液润洗
变大
偏高
碱式滴定管未用待测溶液润洗
变小
偏低
锥形瓶用待测溶液润洗
变大
偏高
锥形瓶洗净后还留有蒸馏水
不变
无影响
取液
取碱液的滴定管开始有气泡,读数时气泡消失
变小
偏低
滴定
酸式滴定管滴定前有气泡,滴定终点时气泡消失
变大
偏高
振荡锥形瓶时部分液体溅出
变小
偏低
部分酸液滴在锥形瓶外
变大
偏高
读数
酸式滴定管滴定前读数正确,滴定后俯视读数(或前仰后俯)
变小
偏低
酸式滴定管滴定前读数正确,滴定后仰视读数(或前俯后仰)
变大
偏高
专题十三 水的电离和溶液的pH
核心考点1、水的电离溶液的酸碱性
1.水的电离
(1)任何条件下,水电离出的c(H+)=c(OH-);常温下,离子积常数KW=1.0×10-14。
(2)酸、碱抑制水的电离, pH相等的盐酸、醋酸对水的电离的抑制程度相同;浓度相等的盐酸和醋酸,盐酸对水的电离的抑制程度更大。
(3)能水解的正盐则促进水的电离。
(4)溶液中的c(H+)与水电离出的c(H+)的区别
①室温下水电离出的c(H+)=c(OH-)=1.0×10-7 ml/L,若某溶液中水电离出的c(H+)<1.0×10-7 ml/L,则可判断该溶液呈酸性或碱性,电解质电离产生的H+或OH-抑制了水的电离;若某溶液中水电离出的c(H+)>1.0×10-7 ml/L,则可判断该溶液中存在能水解的盐,从而促进了水的电离。
②室温下,溶液中c(H+)>1.0×10-7 ml/L,说明溶液是酸性溶液或水解呈酸性的盐溶液;溶液中c(H+)<1.0×10-7 ml/L,说明溶液是碱性溶液或水解呈碱性的盐溶液。
2.溶液的酸碱性及pH
(1)溶液酸碱性与pH:在任何温度下的中性溶液中c(H+)=c(OH-)=eq \r(KW),常温下中性溶液pH=7,温度升高时,中性溶液的pH<7。
(2)溶液pH的计算方法
①强酸溶液pH=-lg c(H+) ,若两强酸溶液(pH相差2以上)等体积混合,混合后溶液的pH等于混合前溶液pH小的加0.3。
②强碱溶液pH=-lg c(H+)=14-lg c(OH-),若两强碱溶液(pH相差2以上)等体积混合,混合后溶液的pH等于混合前溶液pH大的减0.3。
③强酸与强碱混合:若恰好中和,pH=7;若剩余酸,先求中和后剩余的c(H+),再求pH;若剩余碱,先求中和后剩余的c(OH-),再通过KW求出c(H+),最后求pH。
【归纳提升】1.一个基本不变
相同温度下,不论是纯水还是稀溶液,水的离子积常数不变。应用这一原则时需要注意两个条件:水溶液必须是稀溶液;温度必须相同。
2.两个判断标准
(1)任何温度
c(H+)>c(OH-),酸性;c(H+)=c(OH-),中性;c(H+)
pH>7,碱性;pH=7,中性;pH<7,酸性。
1.【2022年1月浙江卷】已知25℃时二元酸H2A的Ka1=1.3×10-7,Ka2=7.1×10-15。下列说法正确的是
A.在等浓度的Na2A.NaHA溶液中,水的电离程度前者小于后者
B.向0.1ml·L-1的H2A溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则H2A的电离度为0.013%
C.向H2A溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
D.取pH=a的H2A溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
【答案】B
【解析】A.在等浓度的Na2A.NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故A错误;B.溶液中c(H+)=10-3ml/L,H2A电离程度较小,溶液中c(H2A)≈0.1ml/L,Ka1=,c(HA-)=1.3×10-5ml/L,c(HA-)≈c(H2A) 电离,则H2A的电离度 0.013%,故B正确;C.向H2A溶液中加入NaOH溶液至pH=11,,则c(A2-)
A.NaHA溶液呈酸性,可以推测H2A为强酸
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 ml·L-1、0.10ml·L-1的醋酸溶液的电离度分别为α1、α2,则α1<α2
D.100 mL pH=10.00的Na2CO3溶液中水电离出H+的物质的量为1.0×10-5ml
【答案】D
【解析】A.NaHA溶液呈酸性,可能是HA-的电离程度大于其水解程度,不能据此得出H2A为强酸的结论,A错误;B.可溶性正盐BA溶液呈中性,不能推测BA为强酸强碱盐,因为也可能是B+和A-的水解程度相同,即也可能是弱酸弱碱盐,B错误;C.弱酸的浓度越小,其电离程度越大,因此0.010 ml·L-1、0.10 ml·L-1的醋酸溶液的电离度分别为α1、α2,则α1>α2,C错误;D.100 mL pH=10.00的Na2CO3溶液中氢氧根离子的浓度是1×10-4ml/L,碳酸根水解促进水的电离,则水电离出H+的浓度是1×10-4ml/L,其物质的量为0.1L×1×10-4ml/L=1×10-5ml,D正确;答案选D。
3.(2019·北京高考真题)实验测得0.5 ml·L−1CH3COONa溶液、0.5 ml·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
A.随温度升高,纯水中c(H+)>c(OH−)
B.随温度升高,CH3COONa溶液的c(OH−)减小
C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同
【答案】C
【解析】水的电离为吸热过程,升高温度,促进水的电离;盐类水解为吸热过程,升高温度促进盐类水解,据此解题;A.水的电离为吸热过程,升高温度,平衡向着电离方向移动,水中c(H+).c(OH-)=Kw增大,故pH减小,但c(H+)=c(OH-),不符合题意;B.水的电离为吸热过程,升高温度,促进水的电离,所以c(OH-)增大,醋酸根水解为吸热过程,CH3COOH-+H2O CH3COOH+OH-,升高温度促进盐类水解,所以c(OH-)增大,不符合题意;C.升高温度,促进水的电离,(H+)增大;升高温度,促进铜离子水解Cu2++2H2OCu(OH)2 +2H+,(H+)增大,两者共同作用使pH发生变化,符合题意;D.盐类水解为吸热过程,升高温度促进盐类水解,不符合题意;综上所述,本题应选C。
4.(2019·上海高考真题)25℃时,0.005ml/LBa(OH)2中H+浓度是( )
A.1×ml/LB.1×ml/L
C.5×ml/LD.5×ml/L
【答案】A
【解析】溶液中的氢氧根离子浓度为0.01ml/L,根据水的离子积常数计算,氢离子浓度为 ml/L。故选A 。
5.(2017·上海高考真题)下列物质的水溶液呈酸性,并且使水的电离平衡向正方向移动的是:
A.Na2CO3 B.NH4Cl C.H2SO4 D.NaHCO3
【答案】B
【解析】A.Na2CO3是强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,促进水电离,错误;B.氯化铵是强酸弱碱盐,铵根离子水解,溶液显酸性,促进水的电离,正确;C.硫酸完全电离生成氢离子而导致溶液中c(H+)增大,溶液显酸性,抑制水的电离,错误;D.碳酸氢钠是强碱弱酸酸式盐,碳酸氢根离子水解程度大于电离程度,溶液显碱性,促进水的电离,错误;故选B。
6.(2017·浙江高考真题)下列说法不正确的是
A.pH<7的溶液不一定呈酸性
B.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
C.在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl-)=c(CH3COO-)
D.氨水和盐酸反应后的溶液,若c(Cl―)=c(NH4+),则溶液呈中性
【答案】B
【解析】A.pH<7的溶液不一定呈酸性,只有当溶液中c(OH-)<c(H+)时溶液显酸性,A正确;B.氢氧化钠是强碱,完全电离,一水合氨是弱碱,部分电离,在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)不相等,前者小于后者,B错误;C.盐酸、CH3COOH溶液中存在电荷守恒:c(H+)=c(OH-)+c(Cl-)、c(H+)=c(OH-)+c(CH3COO-),因此在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl-)=c(CH3COO-),C正确;D.氨水和盐酸反应后的溶液中存在电荷守恒:c(NH4+)+c(H+)=c(OH-)+c(Cl-),若c(Cl―)=c(NH4+),则c(H+)=c(OH-),溶液呈中性,D正确。答案选B。
1.(2021·湖北·统考二模)常温下,向1 L浓度为0.4 ml·L-1的乙醇酸[CH2(OH)COOH]溶液中加入8 g NaOH固体得到X溶液,将X溶液平均分成两等份,一份通入HCl气体,得到溶液Y,另一份加入NaOH固体得到溶液Z,溶液Y、Z的pH随所加物质的物质的量的变化情况如图所示(体积变化忽略不计)。下列说法正确的是
A.b点对应曲线代表的是加入HCl的曲线
B.溶液中水的电离程度:c>b
C.a点:c(Na+)>c[CH2(OH)COO-]>c(H+)>c(OH- )
D.稀释Y溶液后,溶液中不变
【答案】D
【分析】由题可知,n[CH2(OH)COOH]=0.4ml,第一次加入0.2mlNaOH固体,即溶液X为等浓度的CH2(OH)COOH和[CH2(OH)COO]Na的混合溶液,由a点可知,CH2(OH)COOH的电离程度大于CH2(OH)COO-水解程度,导致溶液呈酸性,以此解答。
【详解】A.加入HCl会使溶液pH减小,c点对应曲线代表的是加入HCl的曲线,故A错误;
B.b点时溶液中含0.06mlCH2(OH)COOH和0.14mlCH2(OH)COONa,c点时溶液中含0.14mlCH2(OH)COOH和0.06mlCH2(OH)COONa,b点水的电离程度大于c点水的电离程度,故B错误;
C.a点为等浓度的CH2(OH)COOH和CH2(OH)COONa的混合溶液,且CH2(OH)COO-的电离程度大于水解程度,根据电荷守恒可判断a点离子浓度大小关系为:c[CH2(OH)COO-]>c(Na+)>c(H+)>c(OH-),故C错误;
D.该比例关系为CH2(OH)COO-水解常数的倒数,只与温度有关,稀释过程中,该数值不发生改变,故D正确;
故选D。
2.(2020·天津·模拟预测)用pH试纸测定溶液的pH,下列叙述正确的是
A.测得某浓度的NaClO溶液的pH为10
B.常温下测得NH4Cl溶液pH约为4.1
C.用湿润的pH试纸测pH相同的盐酸和醋酸溶液的pH,误差较大的是盐酸
D.在试管内放入少量溶液并煮沸,把pH试纸放在管口观察其颜色并与标准比色卡比较
【答案】C
【详解】A.NaClO溶液具有漂白性,会将pH试纸漂白,故不能用pH试纸测定其pH,故A错误;
B.广泛的pH试纸测定的溶液的pH的数值为整数,故B错误;
C.稀释时,醋酸还会继续电离出氢离子,故稀释pH相同的盐酸和醋酸溶液时,醋酸的氢离子浓度变化小,pH变化小,故用湿润的pH试纸测pH相同的盐酸和醋酸溶液的pH,误差较大的是盐酸,故C正确;
D.在试管内放入少量溶液并煮沸,把pH试纸放在管口,无法测定溶液的pH,故D错误;
故选C。
3.(2022·北京·模拟预测)常温下,将pH相同、体积均为V0的盐酸和醋酸分别加水稀释至V,pH随的变化如图所示。下列说法不正确的是
A.曲线②表示CH3COOH溶液
B.c点溶液的导电性比b点溶液的导电性强
C.盐酸和醋酸分别稀释到pH=4时,c(Cl-)>c(CH3COO-)
D.c点酸的总浓度大于a点酸的总浓度
【答案】C
【分析】HCl是一元强酸,完全电离,CH3COOH是一元弱酸,部分电离,存在电离平衡,当溶液pH相等时,酸的浓度:c(CH3COOH)>c(HCl),稀释相同倍数时,CH3COOH溶液pH变化小,酸的浓度仍然是c(CH3COOH)>c(HCl)。
【详解】A.开始时溶液pH=3,当=1,即溶液都稀释10倍,曲线①pH=4,pH增大了1个单位,而曲线②pH=3.5<4,pH变化小于1个单位,说明曲线①表示盐酸,曲线②表示CH3COOH溶液,A正确;
B.同一酸溶液,溶液稀释倍数越小,溶液的pH越小,离子浓度越大,该溶液的导电能力就越强。根据图示可知溶液的pH:c<b,则离子浓度:c>b,所以c点溶液的导电性比b点溶液的导电性强,B正确;
C.在HCl溶液中存在电荷守恒:c(H+)=c(OH-)+c(Cl-),在CH3COOH溶液中也存在电荷守恒:c(H+)=c(OH-)+c(CH3COO-),当盐酸和醋酸分别稀释到pH=4时,两种溶液中c(H+)相等,c(OH-)也相等,因此c(Cl-)=c(CH3COO-),C错误;
D.pH相等的两种酸溶液,c(CH3COOH)>c(HCl),当二者稀释相同倍数时,HCl只有稀释作用使离子浓度减小,而弱酸CH3COOH在溶液中存在电离平衡,又电离产生离子,使离子浓度有所增加,此时溶液中酸的浓度仍然是c(CH3COOH)>c(HCl),即c点酸的总浓度大于a点酸的总浓度,D正确;
故合理选项是C。
4.(2022·山东·模拟预测)室温下,分别向体积均为20mL、 浓度均为0.1ml·L-1的HX、HY溶液中,滴加相同浓度的Ba(OH)2溶液(Ba2+与X-、Y-均不反应)。随着Ba(OH)2溶液的加入,由水电离产生的c(H+)的变化趋势如图所示。下列说法错误的是
A.相同条件下,Ka(HX)>Ka(HY)
B.M点溶液显中性,溶液中c(Y-)
D.T点溶液中阴离子浓度之和大于M点
【答案】B
【详解】A.由图示可知,水解对水的电离促进程度较大,则HY的酸性较弱,所以相同条件下Ka(HX)>Ka(HY),故A不选;
B.本题为向酸中滴加Ba(OH)2溶液,因此随着Ba(OH)2溶液的加入溶液先进行酸碱中和反应,所以当HY与Ba(OH)2溶液中水电离出的第一次达到时为中性点,当继续滴加Ba(OH)2溶液会抑制水的电离(N点之后),即第二次水电离该点为碱性点,所以M点呈中性,根据电荷守恒,所以c(Y-)>(Ba2+),故B;
C.N点完全反应点,0.1ml/LBa(OH)2溶液中,故消耗完20mL0.1ml/L的HY需要10mL0.1ml/LBa(OH)2溶液,故C不选;
D.根据电荷守恒可得T点;M点;T、M点相同,T点大于M点,所以,故D不选。
答案选B
5.(2022·湖南邵阳·邵阳市第二中学校考模拟预测)H3PO2是一种一元弱酸,25℃时,在20.0 mL0.1 ml/LH3PO2溶液中滴加0.1 ml/L氢氧化钠溶液V mL,混合溶液的pH与的关系如图所示。下列说法正确的是
A.a=5.77
B.m点时,加入的氢氧化钠溶液的体积大于20 mL
C.25℃时,H3PO2的电离常数Ka的数量级为10-2
D.当V=20.0时,溶液中存在关系:
【答案】AC
【详解】A.,计算得Ka=1.0×10-1.23,则a=7.00-1.23=5.77,A正确;
B.由图可知,m点时pH=7.00,当加入氢氧化钠溶液的体积等于20 mL时,此时溶质为NaH2PO2,NaH2PO2为强碱弱酸盐,溶液显碱性,故m点时加入的氢氧化钠溶液的体积小于20 mL,B错误;
C.根据上述计算结果Ka=1.0×10-1.23,可知H3PO2的电离常数Ka的数量级为10-2,C正确;
D.H3PO2为一元弱酸,不能电离出、,D错误;
故合理选项是AC。
核心考点2溶液酸碱性
1.pH及其测量
(1)计算公式:pH=-lg c(H+)。
适用范围:c(H+)和c(OH-)小于1 ml·L-1的稀溶液。pH越小,表示酸性越强。
(2)pH测量的三种方法
①pH试纸法
用镊子夹取一小块pH试纸放在玻璃片或表面皿上,用洁净的玻璃棒蘸取待测液点在试纸的中央,变色后与标准比色卡对照,即可确定溶液的pH。
注意:a.pH试纸使用前不能用蒸馏水润湿,否则待测液因被稀释可能会产生误差。b.pH试纸不能测定氯水的pH。c.用广泛pH试纸读出的pH只能是整数。
②pH计测量法。 仪器pH计可精确测定试液的pH(读至小数点后2位)。
③酸碱指示剂
酸碱指示剂能粗略测定溶液的pH范围。常见酸碱指示剂的变色范围如下表所示:
2.溶液酸碱性的判断
(1)溶液酸碱性,取决于溶液中c(H+)和c(OH-)的相对大小。常温下,如下表所示:
【注意】用pH判断溶液酸碱性时,要注意温度。如温度升高到100℃时,pH=6,但仍为中性,pH<6显酸性,pH>6显碱性;若溶液未注明温度,一般认为是常温,以pH=7为中性。
(2)[H+]、pH与溶液酸碱性的关系
pH是酸碱性的量度,常温下三者关系如下图所示:
(3)使用范围
pH的取值范围为0~14,即只适用于c(H+)≤1 ml·L-1或c(OH-)≤1 ml·L-1的电解质溶液,当c(H+)或c(OH-)≥1 ml·L-1时,直接用c(H+)或c(OH-)表示溶液的酸碱性。
3.溶液pH计算的思维模板
强酸、强碱等体积溶液混合(常温下)
(1)若ΔpH(pH的差值)≥2的两种强酸溶液等体积混合,酸溶液的pH≈pH小+0.3;如pH=3和pH=5的两种HCl等体积混合,pH≈3+0.3=3.3;
(2)若ΔpH(pH的差值)≥2的两种强碱溶液等体积混合,碱溶液的pH≈pH大-0.3;如pH=9和pH=12的两种NaOH等体积混合,pH≈12-0.3=11.7。
(3)强酸与强碱的等体积混合:
①pH酸+pH碱=14时,pH混=7;
②pH酸+pH碱<14时,pH混≈pH酸+0.3;
③pH酸+pH碱>14时,pH混≈pH碱﹣0.3;
4.四条判断规律
(1)正盐溶液
强酸强碱盐显中性,强酸弱碱盐(如NH4Cl)显酸性,强碱弱酸盐(如CH3COONa)显碱性。
(2)酸式盐溶液
NaHSO4显酸性(NaHSO4 AUTOTEXT == \* MERGEFORMAT =Na++H++SO eq \\al(2-,4))、NaHSO3、NaHC2O4、NaH2PO4水溶液显酸性(酸式根电离程度大于水解程度);NaHCO3、NaHS、Na2HPO4水溶液显碱性(酸式根水解程度大于电离程度)。
注意 因为浓度相同的CH3COO-与NH+4的水解程度相同,所以CH3COONH4溶液显中性,而NH4HCO3溶液略显碱性。
(3)弱酸(或弱碱)及其盐1∶1混合溶液
①1∶1的CH3COOH和CH3COONa混合液呈酸性。
②1∶1的NH3·H2O和NH4Cl混合溶液呈碱性。
(对于等浓度的CH3COOH与CH3COO-,CH3COOH的电离程度大于CH3COO-的水解程度)。
(4)酸碱pH之和等于14等体积混合溶液
pH和等于14的意义:酸溶液中的氢离子浓度等于碱溶液中的氢氧根离子的浓度。
①已知酸、碱溶液的pH之和为14,则等体积混合时:
eq \x(强酸、强碱)eq \(――→,\s\up7(恰好中和))pH=7
eq \x(强酸、弱碱)eq \(――→,\s\up7(碱过量))pH>7
eq \x(弱酸、强碱)eq \(――→,\s\up7(酸过量))pH<7
②已知酸、碱溶液的pH之和为14,若混合后溶液的pH为7,溶液呈中性,则
eq \x(强酸、强碱)―→V酸∶V碱=1∶1
eq \x(强酸、弱碱)―→V酸∶V碱>1∶1
eq \x(弱酸、强碱)―→V酸∶V碱<1∶1
③强酸、强碱等体积混合后溶液酸、碱性的判断
5. 图像法理解一强一弱的稀释规律
(1)相同体积、相同浓度的盐酸、醋酸
①加水稀释相同的倍数,醋酸的pH大。
②加水稀释到相同的pH,盐酸加入的水多。
(2)相同体积、相同pH的盐酸、醋酸
①加水稀释相同的倍数,盐酸的pH大。
②加水稀释到相同的pH,醋酸加入的水多。
【解题策略】 看“三角度”,突破酸HA强弱的判断方法
(1)从水解的角度分析,取其钠盐(NaA)溶于水,测其pH,若pH>7,则说明HA是弱酸,若pH=7,则说明HA是强酸。
(2)从是否完全电离的角度分析,配制一定物质的量浓度的HA溶液(如0. 1 ml·L-1),测其pH,若pH>1,则说明HA是弱酸,若pH=1,则说明HA是强酸。
(3)从电离平衡移动的角度分析,如①向HA溶液中加水稀释100倍后,溶液pH增大值小于2的是弱酸,pH增大2的是强酸;②向HA溶液中加入NaA晶体,溶液pH增大的是弱酸,pH不变的是强酸。
1.【2022年1月浙江卷】已知25℃时二元酸H2A的Ka1=1.3×10-7,Ka2=7.1×10-15。下列说法正确的是
A.在等浓度的Na2A.NaHA溶液中,水的电离程度前者小于后者
B.向0.1ml·L-1的H2A溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则H2A的电离度为0.013%
C.向H2A溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
D.取pH=a的H2A溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
【答案】B
【解析】A.在等浓度的Na2A.NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故A错误;B.溶液中c(H+)=10-3ml/L,H2A电离程度较小,溶液中c(H2A)≈0.1ml/L,Ka1=,c(HA-)=1.3×10-5ml/L,c(HA-)≈c(H2A) 电离,则H2A的电离度 0.013%,故B正确;C.向H2A溶液中加入NaOH溶液至pH=11,,则c(A2-)
A.NaHA溶液呈酸性,可以推测H2A为强酸
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010ml·L-1、0.10ml·L-1的醋酸溶液的电离度分别为α1、α2,则α1<α2
D.100mLpH=10.00的Na2CO3溶液中水电离出H+的物质的量为1.0×10-5ml
【答案】D
【解析】A.NaHA溶液呈酸性,可能是HA-的电离程度大于其水解程度,不能据此得出H2A为强酸的结论,A错误;B.可溶性正盐BA溶液呈中性,不能推测BA为强酸强碱盐,因为也可能是B+和A-的水解程度相同,即也可能是弱酸弱碱盐,B错误;C.弱酸的浓度越小,其电离程度越大,因此0.010ml·L-1、0.10ml·L-1的醋酸溶液的电离度分别为α1、α2,则α1>α2,C错误;D.100mLpH=10.00的Na2CO3溶液中氢氧根离子的浓度是1×10-4ml/L,碳酸根水解促进水的电离,则水电离出H+的浓度是1×10-4ml/L,其物质的量为0.1L×1×10-4ml/L=1×10-5ml,D正确;答案选D。
3.(2019·北京高考真题)实验测得0.5 ml·L−1CH3COONa溶液、0.5 ml·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
A.随温度升高,纯水中c(H+)>c(OH−)
B.随温度升高,CH3COONa溶液的c(OH−)减小
C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同
【答案】C
【解析】水的电离为吸热过程,升高温度,促进水的电离;盐类水解为吸热过程,升高温度促进盐类水解,据此解题;A.水的电离为吸热过程,升高温度,平衡向着电离方向移动,水中c(H+).c(OH-)=Kw增大,故pH减小,但c(H+)=c(OH-),不符合题意;B.水的电离为吸热过程,升高温度,促进水的电离,所以c(OH-)增大,醋酸根水解为吸热过程,CH3COOH-+H2O CH3COOH+OH-,升高温度促进盐类水解,所以c(OH-)增大,不符合题意;C.升高温度,促进水的电离,(H+)增大;升高温度,促进铜离子水解Cu2++2H2OCu(OH)2 +2H+,(H+)增大,两者共同作用使pH发生变化,符合题意;D.盐类水解为吸热过程,升高温度促进盐类水解,不符合题意;综上所述,本题应选C。
4.(2017·浙江高考真题)下列说法不正确的是
A.pH<7的溶液不一定呈酸性
B.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
C.在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl-)=c(CH3COO-)
D.氨水和盐酸反应后的溶液,若c(Cl―)=c(NH4+),则溶液呈中性
【答案】B
【解析】A.pH<7的溶液不一定呈酸性,只有当溶液中c(OH-)<c(H+)时溶液显酸性,A正确;B.氢氧化钠是强碱,完全电离,一水合氨是弱碱,部分电离,在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)不相等,前者小于后者,B错误;C.盐酸、CH3COOH溶液中存在电荷守恒:c(H+)=c(OH-)+c(Cl-)、c(H+)=c(OH-)+c(CH3COO-),因此在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl-)=c(CH3COO-),C正确;D.氨水和盐酸反应后的溶液中存在电荷守恒:c(NH4+)+c(H+)=c(OH-)+c(Cl-),若c(Cl―)=c(NH4+),则c(H+)=c(OH-),溶液呈中性,D正确。答案选B。
5.(2017·浙江高考真题)下列物质的水溶液不能使酚酞变红的是
A.NaOHB.Na2CO3C.NaClD.NH3
【答案】C
【解析】A.NaOH是强碱,溶液显碱性,能使酚酞变红,不选;B.Na2CO3属于强碱弱酸盐,水解后溶液显碱性,能使酚酞变红,不选;C.NaCl是强酸强碱盐,溶液显中性,不能使酚酞变红,选;D.NH3的水溶液显碱性,能使酚酞变红,不选;故选C。
6.(2008·全国高考真题)实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4,石蕊:50~8.0,酚酞:8.2~10.0,用0.1000ml·L-1NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述正确的是( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
【答案】D
【解析】NaOH与CH3COOH恰好完全反应生成CH3COONa,CH3COONa为强碱弱酸盐,水解后溶液呈碱性,为了减少滴定误差,应选择指示剂的pH范围与CH3COONa溶液的pH接近,所以指示剂选择酚酞,故答案为D。
ml/L=7.6×10-12ml/L,所以该点溶液pH<12,正确;故选D。
1.有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是 (填“正确的”或“错误的”),其理由是
。
(2)如不正确,请分析是否一定有误差:
。
(3)若用此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是
。
【解析】用蒸馏水润湿pH试纸的操作是错误的,会使测定时溶液被稀释,对于酸性、碱性或中性溶液将会产生不同的影响。
【答案】(1)错误的 用湿润的pH试纸来测定溶液的pH,相当于将溶液稀释了,测出的溶液pH可能会产生误差。
(2)不一定有误差,当溶液为中性时则不产生误差
(3)盐酸的pH 因为在稀释过程中醋酸继续电离产生H+,使得醋酸溶液中c(H+)受到的影响比盐酸溶液中的小,故误差较小
2. T ℃时,水的离子积为KW,该温度下,将a ml·L-1一元酸HA与b ml·L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是( )
A.混合液pH=7
B.混合液中,c(H+)=eq \r(KW)
C.a=b
D.混合液中,c(B+)=c(A-)+c(OH-)
【解析】由于题中温度未知,A错; 由于KW=c(H+)·c(OH-),当溶液呈中性时,c(H+)=c(OH-),c(H+)=eq \r(KW),B正确;酸、碱强弱未知,当a=b时,混合液pH不能确定,C错;由于反应后溶液呈中性说明c(H+)=c(OH-),D错误。
【答案】B
3. 溶液的酸碱性可用酸度(AG)表示[AG=lgc(H+)c(OH−)],室温下,向浓度均为0.1ml/L体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,AG随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )
A.HX、HY均为弱酸
B.a点由水电离出的c(H+)=1.0×l0﹣13ml•L﹣l
C.c点溶液中:c(Y﹣)<c(Na+)<c(HY)
D.b点时,溶液的pH=7,酸碱恰好完全中和
解析:A.lgc(H+)c(OH−)越大,溶液中氢离子浓度越大,未加NaOH时,HX溶液中lgc(H+)c(OH−)的值大,所以HX的酸性大于HY,加入氢氧化钠物质的量10×10﹣3ml,lgc(H+)c(OH−)=1,c(H+)=c(OH﹣)酸和氢氧化钠溶液恰好反溶液呈中性,HX为强酸,故A错误;B.a点lgc(H+)c(OH−)=12,则溶液中c(H+)=0.1ml/L,溶液中水电离的c(H+)=10−140.1=10﹣13ml•L﹣1,故B正确;C.c点lgc(H+)c(OH−)=6,则溶液中c(H+)=10﹣4ml/L,此时消耗的NaOH为0.005ml,则溶液中的溶质为NaY和HY,由于溶液显酸性,所以HY的电离程度大于NaY的水解程度,所以c(Y﹣)>c(HY),故C错误;D.浓度均为0.1ml•L﹣1、体积均100mL的HY与NaOH恰好中和消耗NaOH为0.01ml,而b点时消耗的NaOH为0.008ml,所以酸过量,故D错误。
答案:B
核心考点3 中和滴定
1.定义:利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法称为酸碱中和滴定。
注意:(1)酸碱恰好中和是指酸与碱按化学方程式中化学计量数关系恰好完全反应生成正盐。
(2)酸碱恰好中和时溶液不一定呈中性,最终溶液的酸碱性取决于生成盐的性质,强酸强碱盐的溶液呈中性,强碱弱酸盐的溶液呈碱性,强酸弱碱盐的溶液呈酸性。
2.实质:酸电离出的 H+与碱电离出的OH- 以等物质的量的关系结合成H2O 的反应,即H++OH-=H2O。
3.中和滴定原理:
对于反应:H+ + OH- = H2O
1 ml 1 ml
c(H+)V(H+) c(OH-)V(OH-)
即可得c(H+)V(H+)=c(OH-)V(OH-)
在中和反应中使用一种已知浓度的酸(或碱)溶液与未知浓度的碱(或酸)溶液完全中和,测出二者所用的体积,根据化学方程式中酸、碱化学计量数关系求出未知浓度溶液的浓度。
计算公式:(以一元酸与一元碱的滴定为例)。
4.实验用品
(1)仪器
酸式滴定管(如图A)、碱式滴定管(如图B)、锥形瓶、滴定管夹、铁架台等。
注意:①酸式、碱式滴定管的异同
②滴定管的优点是易于控制所滴加液体,读数比较精确,可精确到小数点后两位,估读到0.01ml,如24.00ml、23.36 ml,最后一位是估读值。滴定管的“0”刻度在上,往下刻度值越来越大,且容积大于其最大刻度值,因为下面有一段没有刻度。滴定时,所以溶液不得超过最低刻度。
③关闭活塞,加水观察活塞周围有无水渗出;旋转活塞180°再检验有无水渗出。
(2)试剂
标准液、待测液、指示剂、蒸馏水。
5.常用酸碱指示剂及变色范围
6.滴定终点的判断
7.酸碱中和滴定实验操作(以酚酞作指示剂,标准盐酸滴定待测氢氧化钠溶液为例)
(1)滴定前的准备
①查漏:检查滴定管的活塞是否灵活、滴定管是否漏水。
②洗涤:滴定管、锥形瓶均需用蒸馏水洗涤干净。
③润洗:用待盛溶液将滴定管润洗2~3次,以保证装入溶液时不改变溶液的浓度。注意:锥形瓶水洗后不能进行润洗。
④装液:将酸、碱溶液分别装入相应的滴定管中,并使液面位于“0”刻度或“0”刻度上方 2~3cm处。
⑤排气:调节滴定管活塞(或挤压玻璃球),赶走气泡使滴定管尖嘴部分充满溶液。
⑥调液面:使液面处于“0”刻度或“0”刻度以下某一刻度处。
⑦记录:读数时视线应与溶液凹液面最低处相平,记录初始液面刻度刻度。
(2)滴定
①用碱式滴定管(或移液管)取一定体积的待测液于锥形瓶中,并滴入2~3滴酚酞试剂,把锥形瓶放在酸式滴定管下面。
②用左手控制活塞将溶液逐滴滴至锥形瓶内,右手不断摇动锥形瓶,滴至溶液变至无色且半分钟内不再恢复红色,记下刻度。
(3)终点判断
等到滴入最后一滴标准液,溶液由红色变为无色,且在30s内不恢复原来的颜色,视为滴定终点并记录标准液的体积。
注意:当滴入最后一滴××标准溶液后,溶液变成××色,且半分钟内不恢复原来的颜色,即可认为已经达到滴定终点。
①最后一滴:必须说明是滴入“最后一滴”溶液。
②颜色变化:必须说明滴入“最后一滴”溶液后溶液的颜色变化。
③30s:必须说明溶液颜色变化后“30s内不恢复原来的颜色”。
(4)数据处理
按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据原理计算。
8.误差分析的方法(以一元酸滴定一元碱为例)
(1)原理:依据原理c(标准)·V(标准)=c(待测)·V(待测),所以,因为c(标准)与V(待测)已确定,所以只要分析出不正确操作引起V(标准)的变化,即分析出结果。若用标准液滴定待测液,消耗标准液变多,则c(待测)偏高;消耗标准液变少,则c(待测)偏低。
(2)常见的因操作不正确而引起的误差
以标准酸溶液滴定未知浓度的碱溶液(酚酞作指示剂)为例,常见的因操作不正确而引起的误差有
【衔接扩展】在酸碱中和滴定过程中,开始时由于被滴定的酸(或碱)浓度较大,滴入少量的碱(或酸)对其pH的影响不大。当滴定接近终点(pH=7)时,很少量(一滴,约0.04 mL)的碱(或酸)就会引起溶液pH突变(如图所示)。
【易错辨析】
(1)滴定管在使用前要查漏、润洗,酸式滴定管可以盛放酸性、中性、氧化性的物质;碱式滴定管盛放碱性物质。
(2)在进行实验时,为了减少实验偶然性带来的误差,要进行多次实验,一般进行三次,若其中一次误差太大,要舍弃,取其平均值,根据c(碱)· V (碱)=c(酸)·V(酸)计算待测溶液的浓度。
(3)通常会引起实验误差的步骤有洗涤、取液、滴定、读数等,要具体问题具体分析,然后判断其造成的影响。
1.【2022年6月浙江卷】时,向浓度均为的盐酸和醋酸的混合溶液中逐滴加入的溶液(醋酸的;用的溶液滴定等浓度的盐酸,滴定终点的突跃范围4.3~9.7)。下列说法不正确的是
A.恰好中和时,溶液呈碱性
B.滴加溶液至的过程中,发生反应的离子方程式为:
C.滴定过程中,
D.时,
【答案】B
【解析】A.恰好中和时,生成氯化钠溶液和醋酸钠溶液,其中醋酸根离子会水解,溶液显碱性,A正确;B.滴加溶液至的过程中,若只发生反应的离子方程式:,则滴加NaOH溶液的体积为20mL,则根据电离常数,的醋酸中,c(H+)≈c(CH3COO-)= ==>1.0×10-4.3,故用氢氧化钠滴定的过程中,醋酸也参加了反应,则离子方程式为:H++OH-=H2O和CH3COOH+OH-=CH3COO-+H2O,B错误;C.滴定前盐酸和醋酸的浓度相同,故滴定过程中,根据物料守恒可知:,C正确;D.向浓度均为的盐酸和醋酸的混合溶液中逐滴加入的溶液,当盐酸的体积为20ml时,溶液为氯化钠和醋酸的混合溶液,显酸性,需要再滴加适量的氢氧化钠,当加入的NaOH溶液的体积为30mL时,溶液为NaCl和等浓度的CH3COONA.CH3COOH,根据Ka=1.8×10-5>Kh=可知,此时溶液仍然呈酸性,需继续滴加NaOH溶液,故有,D正确;故答案为:B。
2.【2022年1月浙江卷】某同学在两个相同的特制容器中分别加入20mL0.4ml·L-1Na2CO3溶液和40mL0.2ml·L-1NaHCO3溶液,再分别用0.4ml·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
下列说法正确的的是
A.图中甲、丁线表示向NaHCO3溶液中滴加盐酸,乙、丙线表示向Na2CO3溶液中滴加盐酸
B.当滴加盐酸的体积为V1mL时(a点、b点),所发生的反应用离子方程式表示为:HCO+H+=CO2↑+H2O
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.Na2CO3和NaHCO3溶液中均满足:c(H2CO3)-c(CO)=c(OH-)-c(H+)
【答案】C
【解析】A.碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,则碳酸钠溶液的起始pH较大,甲曲线表示碳酸钠溶液中滴加盐酸,碳酸钠与盐酸反应先生成碳酸氢钠,碳酸氢根离子再与氢离子反应产生碳酸,进而产生二氧化碳,则图中丁线表示向Na2CO3溶液中滴加盐酸,乙、丙线表示向NaHCO3溶液中滴加盐酸,A项错误;B.由图示可知,当滴加盐酸的体积为20mL时,碳酸根离子恰好完全转化为碳酸氢根子,而V1> 20mL,V1mL时(a点、b点),没有二氧化碳产生,则所发生的反应为碳酸氢根离子与氢离子结合生成碳酸,离子方程式表示为:HCO+H+=H2CO3,B项错误;C.根据pH-V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指示范围,可用酚酞作指示剂;d点的pH在4左右,符合甲基橙的指示范围,可用甲基橙作指示剂指示滴定终点,C项正确;D.根据电荷守恒和物料守恒,则Na2CO3中存在c(OH-)-c(H+)=2c(H2CO3)+c(HCO), NaHCO3溶液中满足c(H2CO3)-c(CO)=c(OH-)-c(H+),D项错误;答案选C。
3.(2021·湖南真题)常温下,用的盐酸分别滴定20.00mL浓度均为三种一元弱酸的钠盐溶液,滴定曲线如图所示。下列判断错误的是
A.该溶液中:
B.三种一元弱酸的电离常数:
C.当时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
【答案】C
【解析】由图可知,没有加入盐酸时,NaX、NaY、NaZ溶液的pH依次增大,则HX、HY、HZ三种一元弱酸的酸性依次减弱。A.NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为c(Na+)>c(X-)>c(OH-)>c(H+),故A正确;B.弱酸的酸性越弱,电离常数越小,由分析可知,HX、HY、HZ三种一元弱酸的酸性依次减弱,则三种一元弱酸的电离常数的大小顺序为Ka(HX)>Ka (HY)>Ka(HZ),故B正确;C.当溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,则三种盐溶液中酸根的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;D.向三种盐溶液中分别滴加20.00mL盐酸,三种盐都完全反应,溶液中钠离子浓度等于氯离子浓度,将三种溶液混合后溶液中存在电荷守恒关系c(Na+)+ c(H+)= c(X-)+c(Y-)+c(Z-)+ c(Cl-)+ c(OH-),由c(Na+)= c(Cl-)可得:c(X-)+c(Y-)+c(Z-)= c(H+)—c(OH-),故D正确;故选C。
4.(2020·全国高考真题)以酚酞为指示剂,用0.1000 ml·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数:δ(A2-)=c(A2-)c(H2A)+c(HA-)+c(A2-)]
下列叙述正确的是
A.曲线①代表δ(H2A),曲线②代表δ(HA-)
B.H2A溶液的浓度为0.2000 ml·L−1
C.HA−的电离常数Ka=1.0×10−2
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
【答案】C
【解析】根据图像,曲线①代表的粒子的分布系数随着NaOH的滴入逐渐减小,曲线②代表的粒子的分布系数随着NaOH的滴入逐渐增大,粒子的分布系数只有1个交点;当加入40mLNaOH溶液时,溶液的pH在中性发生突变,且曲线②代表的粒子达到最大值接近1;没有加入NaOH时,pH约为1,说明H2A第一步完全电离,第二步部分电离,曲线①代表δ(HA-),曲线②代表δ(A2-),根据反应2NaOH+H2A=Na2A+2H2O,c(H2A)=0.1000ml/L×40mL2×20.00mL=0.1000ml/L,据此分析作答。A.根据分析,曲线①代表δ(HA-),曲线②代表δ(A2-),A错误;B.当加入40.00mLNaOH溶液时,溶液的pH发生突变,说明恰好完全反应,结合分析,根据反应2NaOH+H2A=Na2A+2H2O,c(H2A)= 0.1000ml/L×40mL2×20.00mL=0.1000ml/L,B错误;C.根据曲线当δ(HA-)=δ(A2-)时溶液的pH=2,则HA-的电离平衡常数Ka=c(A2-)⋅c(H+)c(HA-)=c(H+)=1×10-2,C正确;D.用酚酞作指示剂,酚酞变色的pH范围为8.2~10,终点时溶液呈碱性,c(OH-)>c(H+),溶液中的电荷守恒为c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),则c(Na+)>2c(A2-)+c(HA-),D错误;答案选C。
5.(2020·浙江高考真题)室温下,向盐酸中滴加溶液,溶液的pH随溶液体积的变化如图。已知。下列说法不正确的是( )
A.与盐酸恰好完全反应时,
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.时,
【答案】C
【解析】A.与盐酸恰好完全反应时溶液中的溶质为NaCl,呈中性,室温下,正确;B.选择变色范围在pH突变范围内的指示剂,可减小实验误差,B正确;C.甲基橙的变色范围在pH突变范围外,误差更大,错误;D.时,溶液中的溶质为氯化钠和氢氧化钠,且c(NaOH)==0.02ml/L,即溶液中c(OH-)=0.02ml,则c(H+)=5×10-13 ml/L,pH=-lgc(H+)=12.3,正确;故答案为C。
1. (2015·山东理综,13)室温下向10 mL 0.1 ml·L-1NaOH溶液中加入0.1 ml·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
解析:A.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,NaA溶液水解呈碱性,c(HA)>c(H+),故A正确;B.a点A﹣水解,促进水的电离,b点时HA过量,溶液呈酸性,HA电离出H+,抑制水的电离,故B正确;C.pH=7时,c(H+)=c(OH﹣),由电荷守恒可知c(Na+)+c(H+)=c(A﹣)+c(OH﹣),则c(Na+)=c(A﹣),故C错误;D.b点HA过量一倍,溶液存在NaA和HA,溶液呈酸性,说明HA电离程度大于A﹣水解程度,则存在c(A﹣)>c(HA),故D正确。
答案:C
2. 如图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是( )
A.盐酸的物质的量浓度为 1 ml·L-1
B.P点时反应恰好完全,溶液呈中性
C.曲线a是盐酸滴定氢氧化钠的滴定曲线
D.酚酞不能用作本实验的指示剂
解析:根据曲线a知,滴定前盐酸的pH=1,c(HCl)=0.1 ml·L-1,A错误;P点表示盐酸与氢氧化钠恰好完全中和,溶液呈中性,B正确;曲线a是氢氧化钠溶液滴定盐酸的曲线,曲线b是盐酸滴定氢氧化钠溶液的曲线,C错误;强酸与强碱相互滴定,可以用酚酞作指示剂,D错误。
答案:B
3. 室温时,将0.10 ml·L-1 NaOH溶液滴入20.00 mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积的变化曲线如图所示。当V(NaOH)=20.00 mL,二者恰好完全反应。则下列有关说法不正确的是( )
A.该一元酸溶液浓度为0.10 ml·L-1
B.a、b、c点的水溶液导电性依次增强
C.室温时,HA的电离常数Ka≈1×10-5
D.a点和c点所示溶液中H2O的电离程度相同
解析 根据信息,当V(NaOH)=20 mL时,二者恰好完全反应,NaOH+HA===NaA+H2O,因此c(HA)=0.1 ml·L-1,故A项正确;导电性与溶液中离子浓度以及所带电荷数有关,离子浓度越大,所带电荷数越多,导电能力越强,根据起点HA的pH=2,说明HA为弱酸,a点溶质为NaA和HA,HA物质的量较多,b点时溶质为NaA和HA,NaA较多,c点时溶质为NaA和NaOH,都是强电解质,因此导电能力c>b>a,故B项正确;HAH++A-,电离产生的c(H+)=c(A-)=10-2 ml·L-1,弱电解质电离程度微弱,即c(HA)约为0.1 ml·L-1,根据电离平衡常数的表达式K=eq \f(cH+×cA-,cHA)≈eq \f(10-2×10-2,0.1)=10-3,故C项错误;a点对应的pH=3,即溶液中c(H+)=10-3 ml·L-1,c点时pH=11,溶液中c(OH-)=10-3 ml·L-1,两点对水的电离抑制能力相同,故D项正确。
答案 C
指示剂
变色范围的pH
石蕊
<5红色
5~8紫色
>8蓝色
甲基橙
<3.1红色
3.1~4.4橙色
>4.4黄色
酚酞
<8.2无色
8.2~10浅红色
>10红色
相对大小
c(H+)大小
pH
溶液的酸碱性
c(H+)>c(OH-)
c(H+)>1×10-7 ml·L-1
<7
酸性溶液
c(H+)=c(OH-)
c(H+)=1×10-7ml·L-1
=7
中性溶液
c(H+)<c(OH-)
c(H+)<1×10-7ml·L-1
>7
碱性溶液
【易错辨析】
①pH试纸使用前不能用蒸馏水润湿,如用湿润pH试纸测碱性溶液,则结果偏小;如用湿润pH试纸测酸性溶液,则结果偏大;但测中性溶液结果不变,其实质是待测溶液被稀释。
②若某溶液具有漂白性或强氧化性时,则不能用pH试纸测量其pH,比如:不能测定氯水、次氯酸钠溶液的pH。
③用广泛pH试纸测量溶液pH时,读出的数值只能是整数。
④pH试纸不能伸入待测液中。
【特别提醒】本题考查酸碱混合溶液酸碱性判断及溶液中离子浓度大小比较,涉及盐类的水解和弱酸的电离等,题目难度中等,侧重于考查学生的分析能力和计算能力.
指示剂
变色范围的pH
石蕊
<5.0红色
5.0~8.0紫色
>8.0蓝色
甲基橙
<3.1红色
3.1~4.4橙色
>4.4黄色
酚酞
<8.2无色
8.2~10.0浅红色
>10.0红色
步骤
操作
V(标准)
c(待测)
洗涤
酸式滴定管未用标准酸溶液润洗
变大
偏高
碱式滴定管未用待测溶液润洗
变小
偏低
锥形瓶用待测溶液润洗
变大
偏高
锥形瓶洗净后还留有蒸馏水
不变
无影响
取液
取碱液的滴定管开始有气泡,读数时气泡消失
变小
偏低
滴定
酸式滴定管滴定前有气泡,滴定终点时气泡消失
变大
偏高
振荡锥形瓶时部分液体溅出
变小
偏低
部分酸液滴在锥形瓶外
变大
偏高
读数
酸式滴定管滴定前读数正确,滴定后俯视读数(或前仰后俯)
变小
偏低
酸式滴定管滴定前读数正确,滴定后仰视读数(或前俯后仰)
变大
偏高
高考化学二轮复习核心考点逐项突破专题一0五盐类的水解(专讲)(原卷版+解析): 这是一份高考化学二轮复习核心考点逐项突破专题一0五盐类的水解(专讲)(原卷版+解析),共30页。试卷主要包含了盐类的水解及其规律,盐类水解的影响因素及应用,把握三种守恒,明确等量关系等内容,欢迎下载使用。
高考化学二轮复习核心考点逐项突破专题一0五盐类的水解(专练)(原卷版+解析): 这是一份高考化学二轮复习核心考点逐项突破专题一0五盐类的水解(专练)(原卷版+解析),共31页。试卷主要包含了所有题目必须在答题卡上作答,考试结束后,只交试卷答题页,5~8,90,8-2等内容,欢迎下载使用。
高考化学二轮复习核心考点逐项突破专题一0二化学反应速率与化学平衡(专讲)(原卷版+解析): 这是一份高考化学二轮复习核心考点逐项突破专题一0二化学反应速率与化学平衡(专讲)(原卷版+解析),共49页。试卷主要包含了化学反应速率的计算,化学反应速率快慢的比较方法,稀有气体对反应速率的影响等内容,欢迎下载使用。












