


湖南省张家界市2023-2024学年高一下学期期末考试化学试题(含答案)
展开满分100分,考试时间75分钟
注意事项:
1.答卷前,考生务必将自己的姓名、考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,交卷时只交答题卡。
可能用到的相对原子质量:H:1 C:12 O:16 Na:23 S:32 Cl:35.5 Ca: 40 Zn:65
一、单选题:共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求。
1.化学与生活、科技密切相关,下列说法错误的是
A.某地废旧塑料品的处理途径为焚烧回收热能、深挖填埋
B.据调查,武陵源景区已连续多年未出现酸雨,酸雨是指pH<5.6的降雨
C.杭州亚运会吉祥物“江南忆”机器人所采用的芯片主要成分为单晶硅D.食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用
2.“学以致用”让化学生活化。下列物质的应用与氧化还原反应无关的是
A.用NaClO溶液杀菌消毒 B.用于漂白草编制品
C.用浸有KMnO4的硅藻土吸收水果散发的乙烯 D.节日期间燃放烟花爆竹
3.下列实验操作规范且能达到实验目的的是
4.下列关于Na2O和Na2O2的叙述不正确的是
A.过氧化钠的电子式B.都可以作供氧剂
C.都可由单质通过化合反应得到D.与水反应后的溶液均呈碱性
5.下列反应中,属于加成反应的是
A.CH3CH3+Cl2CH3CH2Cl+HCl
B.2CH3CH2OH+2Na2CH3CH2ONa+H2↑
C.CH2=CH2+Br2BrCH2CH2Br
D.CH3COOH +NaOHCH3COONa +H2O
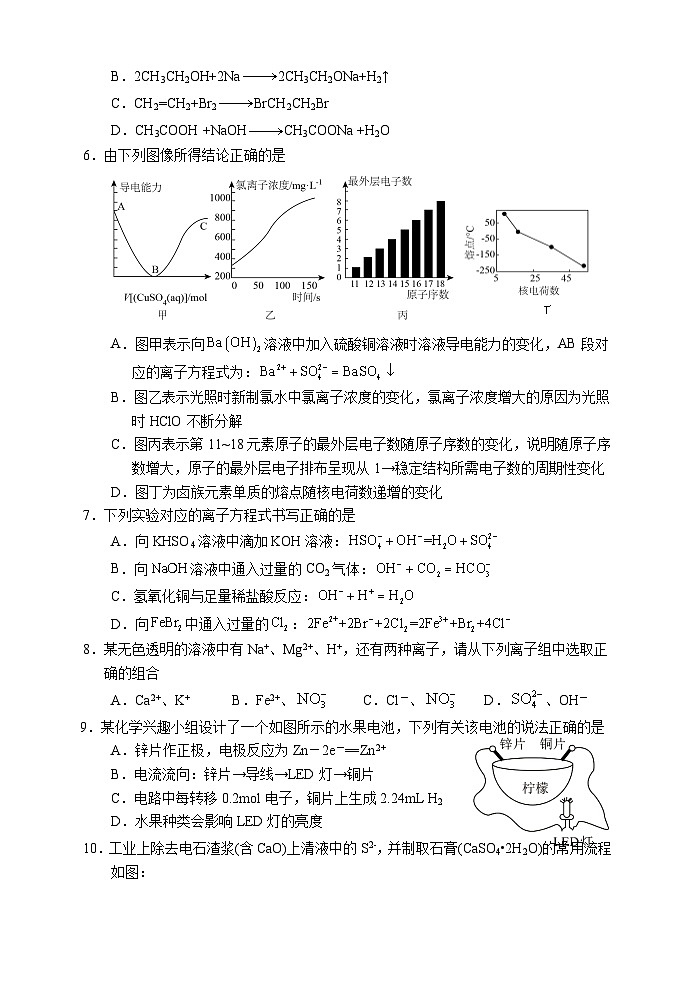
6.由下列图像所得结论正确的是
丁
A.图甲表示向溶液中加入硫酸铜溶液时溶液导电能力的变化,AB段对应的离子方程式为:
B.图乙表示光照时新制氯水中氯离子浓度的变化,氯离子浓度增大的原因为光照时HClO不断分解
C.图丙表示第11~18元素原子的最外层电子数随原子序数的变化,说明随原子序数增大,原子的最外层电子排布呈现从1→稳定结构所需电子数的周期性变化
D.图丁为卤族元素单质的熔点随核电荷数递增的变化
7.下列实验对应的离子方程式书写正确的是
A.向KHSO4溶液中滴加KOH溶液:
B.向溶液中通入过量的CO2气体: QUOTE OH-+CO2=HCO3-
C.氢氧化铜与足量稀盐酸反应:
D.向中通入过量的:
8.某无色透明的溶液中有Na+、Mg2+、H+,还有两种离子,请从下列离子组中选取正确的组合
A.Ca2+、K+ B.Fe2+、C.Cl-、 D.、OH-
9.某化学兴趣小组设计了一个如图所示的水果电池,下列有关该电池的说法正确的是
A.锌片作正极,电极反应为Zn-2e-== Zn2+
B.电流流向:锌片→导线→LED灯→铜片
C.电路中每转移0.2ml电子,铜片上生成2.24mL H2
D.水果种类会影响LED灯的亮度
10.工业上除去电石渣浆(含CaO)上清液中的S2-,并制取石膏(CaSO4•2H2O)的常用流程如图:
常温下,饱和石灰水的物质的量浓度为0.002ml•L-1,下列说法不正确的是
A.S2O在过程Ⅱ中是氧化产物,Mn(OH)2在过程Ⅰ中作还原剂
B.将1L上清液中的S2-直接被O2氧化为SO(S2-浓度为480mg•L-1),理论上共需要0.03ml的O2
C.由上述流程图可知,O2的氧化性强于MnO
D.常温下,56gCaO溶于水配成1L溶液,溶液中Ca2+的数目为NA个
11.设NA表示阿伏加德罗常数的值,下列说法正确的是
A.39 g Na2S和Na2O2组成的混合物中,含有阴离子的数目为0.5 NA
B.0.1 ml H2和0.1 ml I2于密闭容器中充分反应后,HI分子总数为0.2 NA
C.23g钠与1 L0.1 ml·L-1盐酸反应,生成的H2分子的数目为0.05 NA
D.46g 乙醇含有的极性共价键数目为8 NA
12.一定条件下,反应A(g)+3B(g)2C(g)+2D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是
A.单位时间内生成3n ml B,同时消耗2n ml C
B.容器内压强不随时间变化
C.混合气体的密度不随时间变化
D.单位时间内生成n ml A,同时生成2n ml D
13.一种很有研究前景的固态电池电解质(结构如图所示)。其中X、Y、Z为原子序数依次增大的短周期主族元素,三者的核外电子数之和等于35,则下列说法正确的是
A.X单质可以在空气中燃烧
B.工业上常采用电解YCl的饱和溶液制备Y单质
C.Z离子是同周期主族元素简单离子中半径最大的
D.该化合物阴离子中各原子均不满足8电子稳定结构
14.将一定质量的锌粉与足量的浓硝酸反应生成硝酸盐、水及气体,锌粉完全反应时收集到11.2LNO、NO2混合气(标准状况下),该混合气体与3.36LO2(标准状况下)混合后,通入水中能全部被吸收转化为硝酸。则所消耗硝酸的物质的量是
A. B.C. D.
二、非选择题(本题共4小题,每空2分,总计58分。)
15.(14分)I.(1)如图表示某反应的能量变化关系,则此反应为_________ (填“吸热”或“放热”)反应,其中ΔH= _________ (用含有 a、b的关系式表示)。
(2)在一定条件下,反应过程中能量变化不符合上图的是________。
A.氧化钙与水反应B.晶体和NH4Cl晶体反应
C.镁和盐酸反应D.甲烷在氧气中燃烧
II. 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
(3)反应开始至2min,以气体Z表示的平均反应速率为_________。
(4)下列措施能增大反应速率的是_________。
A.升高温度 B.加入高效催化剂
C.保持容器压强不变,充入一定量氦气
D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
Ⅲ. 某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
(5)实验①和②探究的是_________对化学反应速率的影响;为了观察到上述KMnO4溶液紫色褪去,至少需要加入0.20ml·L-1H2C2O4溶液_________mL。
16.(14分)许多无机非金属材料含有硅元素,具有耐高温、抗腐蚀、硬度高等特点,以及特殊的光学、电学等性能。以下为制备高纯硅的主要工艺流程图:
已知:沸点,且能与剧烈反应,并在空气中易自燃。
回答下列问题:
(1)在元素周期表中的位置为___________。
(2)写出上述流程“氧化”步骤中,在300℃条件下,用粗硅制备的化学方程式为_________________。
(3)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是___________(填序号)。
A.压电陶瓷 B.高温结构陶瓷C.生物陶瓷 D.超导陶瓷
(4)上述制备高纯硅的工艺流程中可以循环利用的物质是_______(填化学式)。
(5)若用下图所示装置证明非金属性:,从以下所给物质中选出合适的物质进行验证:①稀盐酸;②稀硫酸;③碳酸钠;④溶液。试剂A为_______(填序号,下同),试剂C为_______。装置B中会生成一种气体,写出该气体的电子式____________。
17.(14分)下列是某学习小组的同学关于氯气与铁反应及产物的探究:
(1)根据上图写出该学习小组制备氯气的化学方程式 。
(2)硬质玻璃管与收集器之间没有用导管连接,这样做的优点是________________。
(3)上图中浓硫酸的作用是________________,碱石灰的作用是________________和防止空气中的水蒸气进入收集器中,造成FeCl3潮解。
(4)反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入一定量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
新制氯水
固体
产物
KSCN溶液
少许植物油
溶液
一定量稀盐酸
溶液不
变色
溶液
变红
固体产物的成分可能为_____(填字母)。
A.Fe和FeCl3 B.FeCl2和FeCl3 C.Fe、FeCl2和FeCl3 D.Fe和FeCl2
(5)反应过程中不振荡的原因是_________________________________________。
(6)现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe)∶n(Cl)=1∶2.1,则该样品中FeCl3的物质的量分数为__________。(计算结果保留两位有效数字)
18.(16分)乳酸乙酯主要用于调配苹果、凤梨、焦糖、乳香等食用香精,也用于朗姆酒、白酒等酒用香精中,还可用作纤维素酯、树脂、涂料等的溶剂。乳酸乙酯发生如图变化(已知:①烃A是衡量一个国家石油化工发展的重要标志;②G属于酯类化合物)。
(1)B物质的结构简式为 ,D的名称是 。
(2)E中官能团的名称是 ,B生成C的反应类型是 。
(3)反应⑤中浓硫酸的作用是 。
(4)写出F、D两种物质生成G的化学方程式 。
(5)乙烯与氢气反应得到乙烷,下列物质与乙烷互为同系物的有 。
①CH2=CH2 ②CH3CH2OH ③HOCH2CH2OH
④ ⑤
其中④的二氯代物有 种。装置或
操作
预期目的
实验室制取SO2
熔化NaOH
检验二氧化硫的漂白性
比较Na2CO3和NaHCO3的稳定性
选项
A
B
C
D
编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/ml·L-1
体积/mL
浓度/ml·L-1
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
2.0
0.010
4.0
25
③
0.20
2.0
0.010
4.0
50
湖南省多校联考2023-2024学年高一下学期期末考试化学试题(含答案): 这是一份湖南省多校联考2023-2024学年高一下学期期末考试化学试题(含答案),文件包含湖南省多校联考2023-2024学年高一下学期期末考试化学试题docx、高一化学答案pdf等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
湖南省怀化市2023-2024学年高一下学期期末考试 化学试题: 这是一份湖南省怀化市2023-2024学年高一下学期期末考试 化学试题,共10页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
湖南省岳阳市华容县2023-2024学年高一下学期期末考试化学试题(含答案): 这是一份湖南省岳阳市华容县2023-2024学年高一下学期期末考试化学试题(含答案),共8页。试卷主要包含了考试结束时,将答题卡交回, 羧基,蒸馏,温度,分液漏斗等内容,欢迎下载使用。












