
2024年江苏省徐州市中考一模化学试卷
展开选择题(每题2分,共20分)
传统工艺是中华优秀传统文化的重要组成部分。下列传统工艺不涉及化学变化的是( )
A.青铜器制造 B.铁的冶炼 C.瓷器烧制 D.楠木造船
2. 下列关于酸和碱的说法错误的是( )
A. 正常的雨水中因溶有二氧化碳,通常显酸性
B. 锰(Mn)比锌活泼,所以能与稀硫酸反应生成氢气
C. 37%的盐酸可以加热浓缩为98%的浓盐酸
D. 滴人酚酞试液后变红的溶液一定呈碱性
3. 化学实验操作要科学规范。下列实验操作正确的是( )
A. 蒸发结晶过程中,停止加热时仍不断搅拌
B. 测定溶液的pH时,应先将pH试纸润湿
C. 过滤操作时将悬浊液直接倒人漏斗内
D. 配制溶液时,将多余的药品直接放回原瓶
4. 如图,向装满二氧化碳的软塑料瓶里注入1/3的水,然后旋紧瓶盖振荡。下列叙述错误的是( )
A. 充分振荡后,塑料瓶会变瘪
B. 该实验说明二氧化碳能与水反应
C. 塑料瓶内的溶液中存在二氧化碳分子
D. 塑料瓶内的溶液能使紫色石蕊试液变红色
5.下列物质的性质与用途对应关系正确的是( )
A.镁有银白色光泽,可用于生产烟花 B.金刚石硬度大,可用于切割玻璃
C.浓硫酸具有吸水性,可用来干燥氨气 D.碳酸氢铵受热易分解,可作化肥
6. 硝酸钾、氯化钠的溶解度曲线如图所示。下列有关说法错误的是( )
A. 硝酸钾的溶解度受温度影响比氯化钠大
B.40℃时,硝酸钾饱和溶液的溶质质量分数为63.9%
C. t℃时,等质量的两种物质的饱和溶液中溶质质量相等
D.40℃时,将163.9g硝酸钾的饱和溶液降温至20℃,析出晶体的
质量是32.3g
7. 下列对有关化学事实的分析正确的是( )
A. 蔗糖水溶液不导电,说明蔗糖以分子的形式存在于水中
B. 铝制品有良好的耐腐蚀性,说明常温下铝不易与氧气反应
C. 碳铵和草木灰混合使用,可以供给农作物更多营养元素
D. 能够给人体提供能量的物质只有食物中的糖类和油脂
8.奥司他韦胶囊是治疗甲型流感的特效药,奥司他韦化学式为C16H28N2O4,下列说法正确的是( )
A.从微观结构上看:奥司他韦中含有1个氮气分子
B. 从物质分类上看:奥司他韦属于有机高分子化合物
C. 从宏观组成上看:奥司他韦由碳、氢、氮、氧四种元素组成
D. 从质量占比上看:奥司他韦中氢元素和氧元素的质量比为7:1
9. 下列实验操作能达到实验目的的是( )
A. 鉴别蚕丝与羊毛:取样,灼烧,闻气味
B. 除去二氧化碳中少量一氧化碳: 将气体在密闭容器中进行点燃
C. 检验氢氧化钠溶液是否变质: 取样,滴加过量稀盐酸,观察有无气泡生成
D. 分离氯酸钾制取氧气后的混合物获得二氧化锰: 溶解、过滤、蒸发结晶
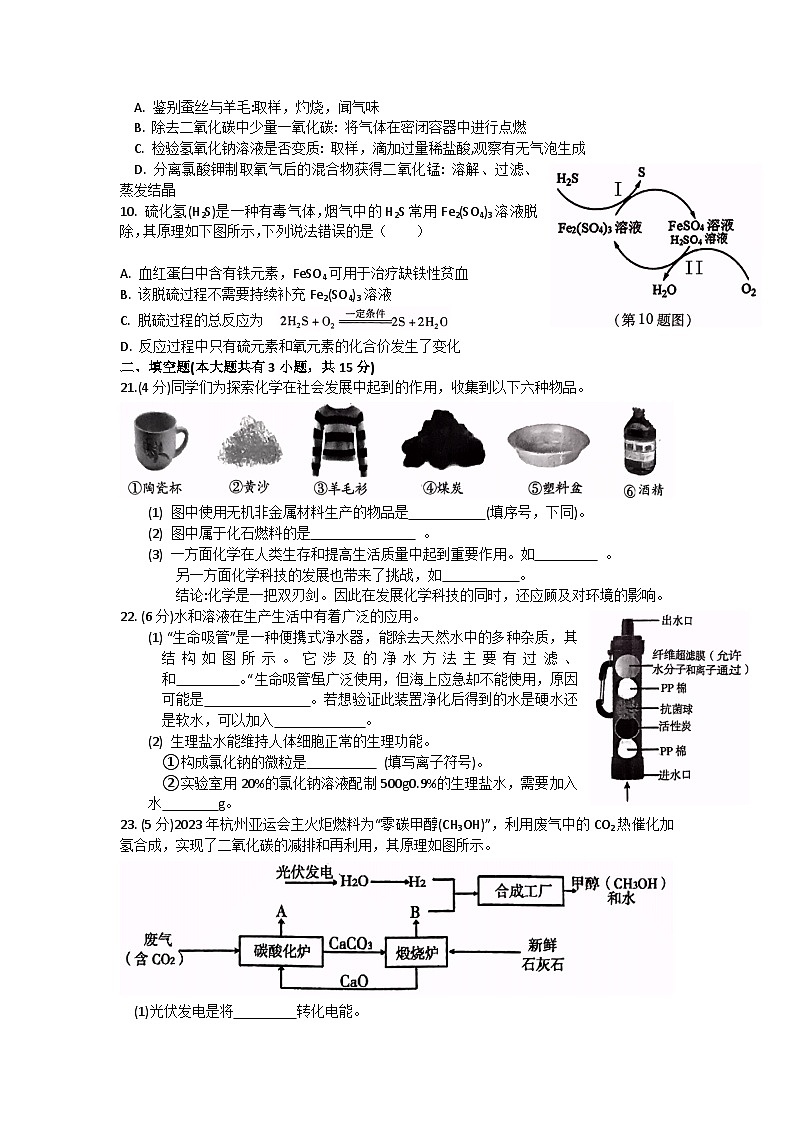
10. 硫化氢(H2S)是一种有毒气体,烟气中的H2S常用Fe2(SO4)3溶液脱除,其原理如下图所示,下列说法错误的是( )
A. 血红蛋白中含有铁元素,FeSO4可用于治疗缺铁性贫血
B. 该脱硫过程不需要持续补充Fe2(SO4)3溶液
C. 脱硫过程的总反应为
D. 反应过程中只有硫元素和氧元素的化合价发生了变化
二、填空题(本大题共有3小题,共15分)
21.(4分)同学们为探索化学在社会发展中起到的作用,收集到以下六种物品。
(1) 图中使用无机非金属材料生产的物品是 (填序号,下同)。
(2) 图中属于化石燃料的是 。
(3) 一方面化学在人类生存和提高生活质量中起到重要作用。如 。
另一方面化学科技的发展也带来了挑战,如 。
结论:化学是一把双刃剑。因此在发展化学科技的同时,还应顾及对环境的影响。
22. (6分)水和溶液在生产生活中有着广泛的应用。
(1) “生命吸管”是一种便携式净水器,能除去天然水中的多种杂质,其结构如图所示。它涉及的净水方法主要有过滤、 和 。“生命吸管”虽广泛使用,但海上应急却不能使用,原因可能是 。若想验证此装置净化后得到的水是硬水还是软水,可以加入 。
(2) 生理盐水能维持人体细胞正常的生理功能。
①构成氯化钠的微粒是 (填写离子符号)。
②实验室用20%的氯化钠溶液配制500g0.9%的生理盐水,需要加入水 g。
(5分)2023年杭州亚运会主火炬燃料为“零碳甲醇(CH3OH)”,利用废气中的CO2热催化加氢合成,实现了二氧化碳的减排和再利用,其原理如图所示。
(1)光伏发电是将 转化电能。
(2)煅烧炉中发生反应的化学方程式为 ,其基本反应类型是 。
(3)合成甲醇的过程中,参加反应的H2和B的分子个数比为 。
三、实验与探究题(本大题共有2小题,共25分)
24. (16分)请根据下列实验装置图回答有关问题。
(1) 装置 B中作为反应容器的仪器名称是 。
(2) 若用装置B和F制取二氧化碳,有关反应的化学方程式为 ,收集气体时应将a和 (填“b” 或“c”)相连,为验证二氧化碳的性质,另一端连接G装置,右图表示G中溶液的pH与实验时间的变化关系曲线。已知:此实验条件下Na2CO3溶液的pH = 11.6,NaHCO3溶液的pH=8.3。实验50s时烧杯中的溶质是 。
(3)若将装置A和E连接制取氧气,则A中反应的化学方程式为 ,试管中棉花的作用是 ,根据燃烧条件分析棉花没有燃烧的主要原因是 。
(4)收集某种气体时仅能选用装置D,说明该气体具有的物理性质是 和 。
(5)如图装置可用于实验室多次连续进行氧气的制取和性质的实验。
①打开弹簧夹,在燃烧匙中点燃硫粉,丁试管中为稀 KMnO4溶液,丁装置可观察到现象是 。
② (4分)实验过程中需要0. 64g氧气,至少需要准备 5%的过氧化氢溶液多少克?(写出计算过程)
25. (9分)宋朝王希孟的《千里江山图》历经千年,依旧色彩艳丽的关键在于使用了石青、石绿、赭石等传统颜料。某化学兴趣小组对石青和石绿的性质进行了以下探究。
查阅资料:石青的主要成分是2CuCO3•Cu(OH)2,石绿的主要成分是CuCO3 • Cu(OH)2,都可称为碱式碳酸铜;碱式碳酸铜的化学式可表示为xCuCO3 • yCu(OH)2,其中“•”表示合的意思,x、y为正整数;CuCO3、Cu(OH)2受热时会分解得到相应的氧化物。
Ⅰ探究石青和石绿的化学性质
(1)《本草纲目》载:铜得紫阳之气(二氧化碳、水蒸气、氧气)而生绿,绿久则成石,谓之石绿。请用化学方程式表示石绿的形成过程: 。
(2)取少量石青粉末于试管中,充分加热后观察到试管中固体变黑,产生的气体通人到盛有澄清石灰水的烧杯中,溶液变浑浊。该黑色固体为 (填化学式)。
(3)取少世石绿粉末于试管中,加入足量稀硫酸,观察到固体溶解,产生气泡,溶液由无色变成 蓝色。溶液中含有的盐类物质为 (填化学式)。
结论:碱式碳酸铜受热可分解,且可与酸反应。
Ⅱ测定某种碱式碳酸铜[为xCuCO3 • yCu(OH)2]的组成。
利用如图所示装置进行实验(实验中每一步吸收都是完全的)。
(4)实验步骤如下:①连接好装置, ;②装入药品:③打开活塞K,鼓人空气;④一段时间后关闭活塞K, 称量相关装置的质量;⑤点燃酒精灯,至装置B中无气泡产生;⑥打开活塞K,鼓入空气;⑦熄灭酒精灯;⑧一段时间后关闭活塞K,称量相关装置质量。
注:碱石灰主要成分为氢氧化钠和氧化钙固体,能吸收水和二氧化碳。
(5)C装置中U形管内碱石灰的作用是 。
(6)若碱式碳酸铜已完全分解,实验后装置B增重4. 5g,装置C增重4.4g,则该碱式碳酸铜的 化学式可表示为 。
Ⅲ感悟青绿
在古代,广义上青色可以代指绿色一蓝色一紫色一黑色,“青色”在文化意义上是一种虚指的颜色,常见的有玄青(氧化铜),曾青(硫酸铜),丹青(铜),青绿(碱式碳酸铜),这些颜色是中国文化的一个缩影。
(7)“曾青转化为丹青”的化学反应原理是 (用化学方程式表示)。
2024年江苏省徐州市中考一模化学试题: 这是一份2024年江苏省徐州市中考一模化学试题,共7页。试卷主要包含了选择题,填空与简答题,实验与探究题等内容,欢迎下载使用。
2024年江苏省徐州市中考一模化学试题: 这是一份2024年江苏省徐州市中考一模化学试题,共4页。
2023年江苏省徐州市中考化学三模试卷(含解析): 这是一份2023年江苏省徐州市中考化学三模试卷(含解析),共18页。试卷主要包含了单选题,填空题,流程题,实验题,探究题,计算题等内容,欢迎下载使用。












