
江苏省扬州大学附属中学东部分校2023-2024学年高二下学期3月月考化学试卷(含答案)
展开1.《可再生能源法》倡导碳资源的高效转化及循环利用。下列做法与该理念相违背的是( )
A.大力发展煤的气化及液化技术B.加快石油等化石燃料的开采和使用
C.以为原料生产可降解塑料D.将秸秆进行加工转化为乙醇燃料
2.根据价层电子对互斥模型,判断下列分子或离子的空间结构正确的是( )
A.①②B.①④C.②④D.②③
3.已知的结构如图,在KOH溶液中可发生反应:
,设为阿伏加德罗常数的值,下列说法正确的是( )
A.产物分子中所有的原子可能共平面
B.中P原子为杂化
C.含有个P-P键(P的相对原子质量:31)
D.为非极性分子
4.实验室可用反应制备三氯化氨合钴。下列有关说法正确的是( )
A.的基态核外电子排布式为
B.的电子式为
C.中子数为18的氯原子可表示为
D.含有共价键、配位键和离子键
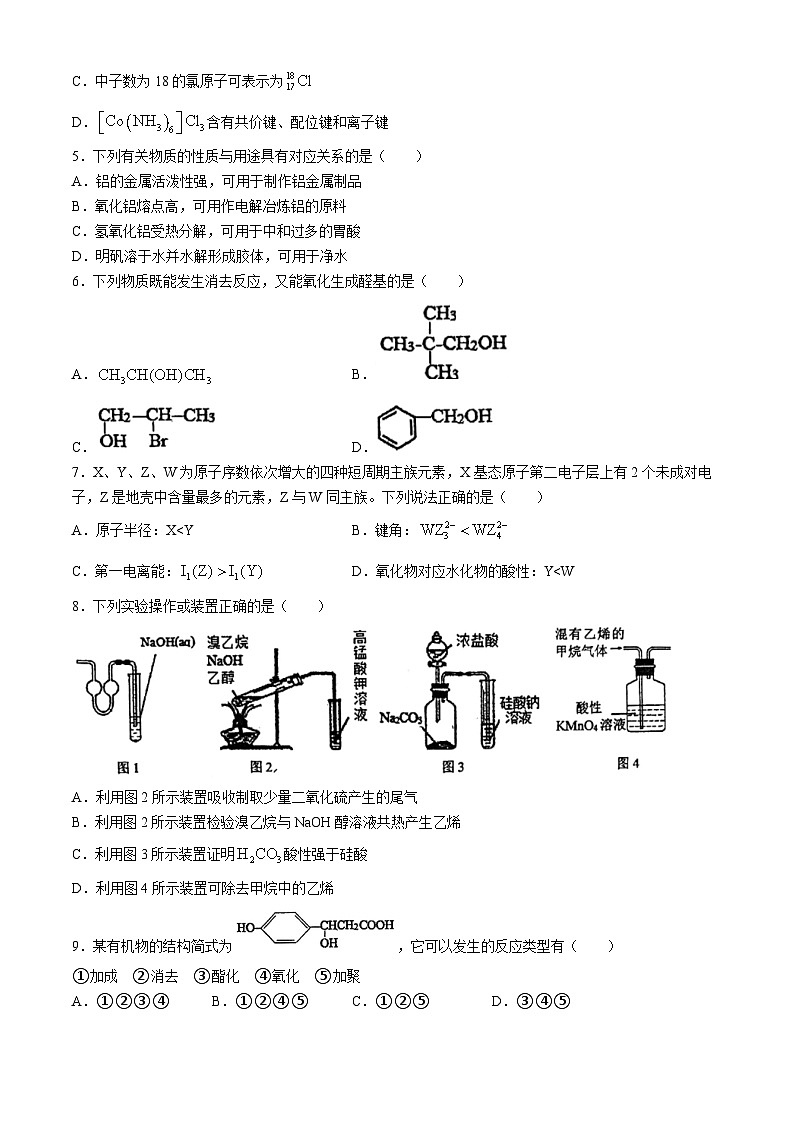
5.下列有关物质的性质与用途具有对应关系的是( )
A.铝的金属活泼性强,可用于制作铝金属制品
B.氧化铝熔点高,可用作电解冶炼铝的原料
C.氢氧化铝受热分解,可用于中和过多的胃酸
D.明矾溶于水并水解形成胶体,可用于净水
6.下列物质既能发生消去反应,又能氧化生成醛基的是( )
A.B.
C.D.
7.X、Y、Z、W为原子序数依次增大的四种短周期主族元素,X基态原子第二电子层上有2个未成对电子,Z是地壳中含量最多的元素,Z与W同主族。下列说法正确的是( )
A.原子半径:X
A.利用图2所示装置吸收制取少量二氧化硫产生的尾气
B.利用图2所示装置检验溴乙烷与NaOH醇溶液共热产生乙烯
C.利用图3所示装置证明酸性强于硅酸
D.利用图4所示装置可除去甲烷中的乙烯
9.某有机物的结构简式为,它可以发生的反应类型有( )
①加成 ②消去 ③酯化 ④氧化 ⑤加聚
A.①②③④B.①②④⑤C.①②⑤D.③④⑤
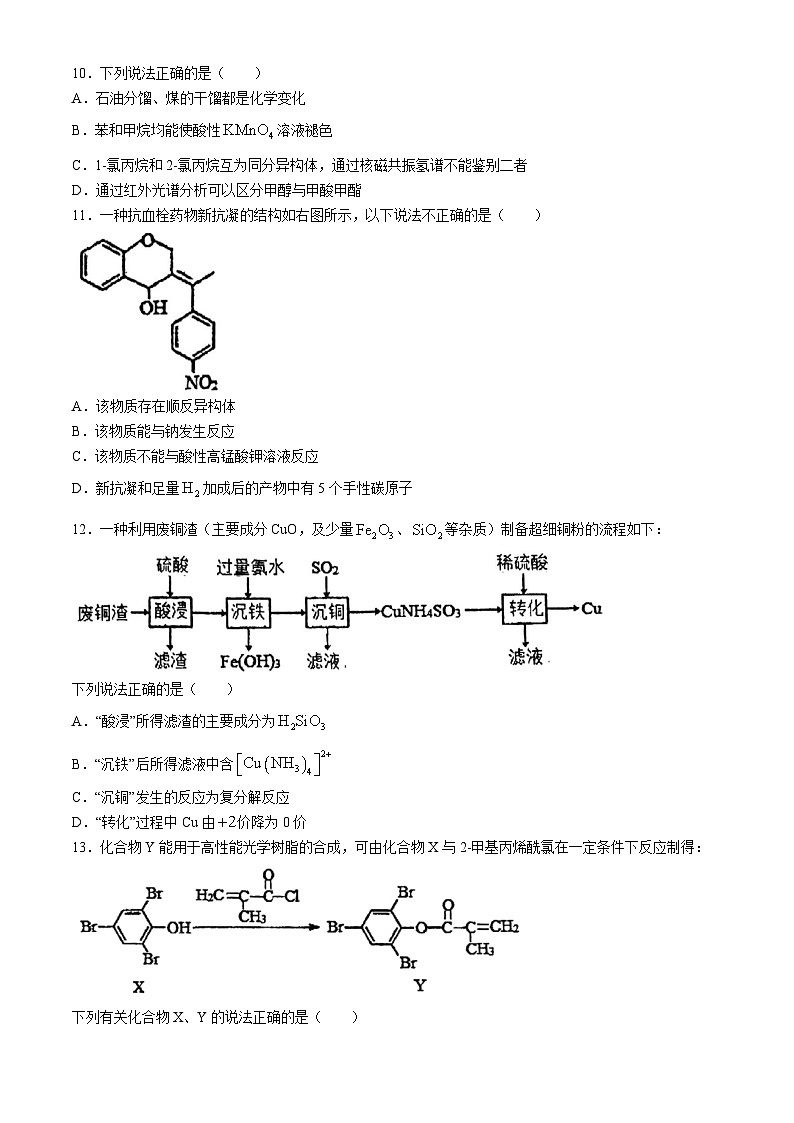
10.下列说法正确的是( )
A.石油分馏、煤的干馏都是化学变化
B.苯和甲烷均能使酸性溶液褪色
C.1-氯丙烷和2-氯丙烷互为同分异构体,通过核磁共振氢谱不能鉴别二者
D.通过红外光谱分析可以区分甲醇与甲酸甲酯
11.一种抗血栓药物新抗凝的结构如右图所示,以下说法不正确的是( )
A.该物质存在顺反异构体
B.该物质能与钠发生反应
C.该物质不能与酸性高锰酸钾溶液反应
D.新抗凝和足量加成后的产物中有5个手性碳原子
12.一种利用废铜渣(主要成分CuO,及少量、等杂质)制备超细铜粉的流程如下:
下列说法正确的是( )
A.“酸浸”所得滤渣的主要成分为
B.“沉铁”后所得滤液中含
C.“沉铜”发生的反应为复分解反应
D.“转化”过程中Cu由价降为0价
13.化合物Y能用于高性能光学树脂的合成,可由化合物X与2-甲基丙烯酰氯在一定条件下反应制得:
下列有关化合物X、Y的说法正确的是( )
A.X分子中所有原子一定在同一平面上
B.Y与的加成产物分子中含有手性碳原子
C.X与溴苯()互为同系物
D.X→Y的反应为消去反应
二、填空题:
14.(14分)2-甲基-1,3-丁二烯()是一种重要的化工原料。可以发生以下反应。
请回答下列问题:
(1)2-甲基-1,3-丁二烯的键线式是:________。
(2)2-甲基-1,3-丁二烯与发生加成反应。
①足量时,所得有机产物的结构简式:________。
②发生1,2-加成反应时的化学方程式为(写一个):________。
③发生1,4-加成所得有机产物的结构简式为:________。
(3)上述流程图中反应①的机理为:
B为含有六元环的有机物,写出反应①的化学方程式:
________。
(4)Y()是天然橡胶的主要成分,在一定条件下,能与Y发生反应的物质有________(填标号)。
A.溴水B.酸性高锰酸钾溶液C.钠D.氢氧化钠溶液
(5)已知:
上述流程中X的分子式为,则其结构简式为:________。
15.(10分)广泛应用于太阳能电池领域。以、NaOH和抗坏血酸为原料,可制备。
(1)基态核外电子排布式为________。
(2)的空间构型为________(用文字描述);与反应能生成,中的配位原子为________(填元素符号)。
(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为________;推测抗坏血酸在水中的溶解性:________(填“难溶于水”或“易溶于水”)。
16.(12分)是一种难溶于水、易溶于硫酸的白色固体,主要用于制造磷酸铁锂电池材料、催化剂及陶瓷等,制备电池级超细磷酸铁的主要工艺流程图如下:
(1)“氧化”过程中发生反应的离子方程式为________。
(2)“沉铁”生成沉淀为羟基磷酸铁晶体,若“沉铁”恰好反应完全,则滤液1的成分为________(写化学式)。
(3)检验“沉铁”步骤中沉淀洗涤是否完全的方法是________。
(4)已知(铁氰化钾)溶液与反应产生深蓝色沉淀,与不反应;不同pH对沉淀的影响如图所示。
①在pH大于时,随pH增大,磷的沉淀率开始下降,其可能原因是________。
②实验室以为原料制备,补充完整相应的实验方案:取一定量的溶解于稍过量的溶液中,________。(实验中须使用的试剂:溶液、溶液、溶液、蒸馏水)
17.(22分)某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。
已知:(苯胺,易被氧化)
(1)写出X分子式:________;F的结构简式:________。
(2)X生成A所需的试剂及反应条件:________。
(3)反应②③两步能否互换________,(填“能”或“不能”)理由是________。
(4)反应④的化学方程式是________;
反应⑤的化学方程式是________。
(5)写出同时满足下列条件的的一种同分异构体的结构简式________
①含苯环 ②份子中不同化学环境的氢原于数目比为
(6)已知:(R表示烃基,表示烃基或氢),利用已知和所学知识写出以为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例如下:
)。
扬州大学附属中学东部分校2023-2024学年高二下学期3月月考
(化学)答案
一、选择题:
二、填空题:
14.(14分)(每空2分)
(1)
(2)①
②或
③或
(3)
15.(10分)(每空2分)
(1)或 (2)正四面体 (3)O
(4)、 (5)易溶于水(2分)
16.(12分)(每空2分)
(1)
(2)
(3)取最后一次洗涤滤液,加入盐酸酸化的氯化钡溶液,没有生成沉淀,说明已经洗涤干净
(4)①溶液碱性过强,导致铁离子转化为氢氧化铁沉淀,使得磷的沉淀率下降
②加入溶液(1分)至反位后溶液加入溶液不产生深蓝色沉淀(1分),反应后溶液加入溶液调节溶液的pH至左右(1分),得到沉淀过滤,使用蒸馏水洗涤、烘干得到(1分)
17.(22分)
(1)X;(3分) E; (2)、光照
(3)不能(1分)若互换,还原得到的氮基能再次被氧化(意思相近均给分)(1分)
(4)(3分)
(3分)
(5)或(其它合理结构也给分)
(6)(5分)
编号
分子式
价层电子对互斥模型
分子或离子的空间结构
①
正四面体形
三角锥形
②
HCHO
平面三角形
三角锥形
③
平面三角形
平面三角形
④
正四面体形
正四面体形
1
2
3
4
5
6
7
8
9
10
11
12
13
B
B
C
D
D
C
B
A
A
D
C
B
B
湖南省师范大学附属中学2023-2024学年高三下学期+月考化学试卷: 这是一份湖南省师范大学附属中学2023-2024学年高三下学期+月考化学试卷,共13页。
江苏省扬州中学2023-2024学年高二下学期3月考试化学试题: 这是一份江苏省扬州中学2023-2024学年高二下学期3月考试化学试题,共7页。试卷主要包含了化学处处呈现美, 下列实验操作合理的是,下列化学用语或表述正确的是等内容,欢迎下载使用。
江苏省扬州大学附属中学2023-2024学年高二上学期12月阶段测试化学试题含答案: 这是一份江苏省扬州大学附属中学2023-2024学年高二上学期12月阶段测试化学试题含答案,共14页。试卷主要包含了5 Mn-55,4 L,20~9,27等内容,欢迎下载使用。












