





备战2025届新高考化学一轮总复习第3章金属及其化合物第11讲铁盐和亚铁盐含铁物质的转化课件
展开1.结合真实情境中的应用实例或通过实验探究,了解铁盐和亚铁盐的主要性质,了解这些物质在生产、生活中的应用。2.结合实例认识金属及其化合物的多样性,了解通过化学反应可以探索物质的性质、实现物质转化,认识物质及其转化的重要价值。
考点二 含铁物质的转化
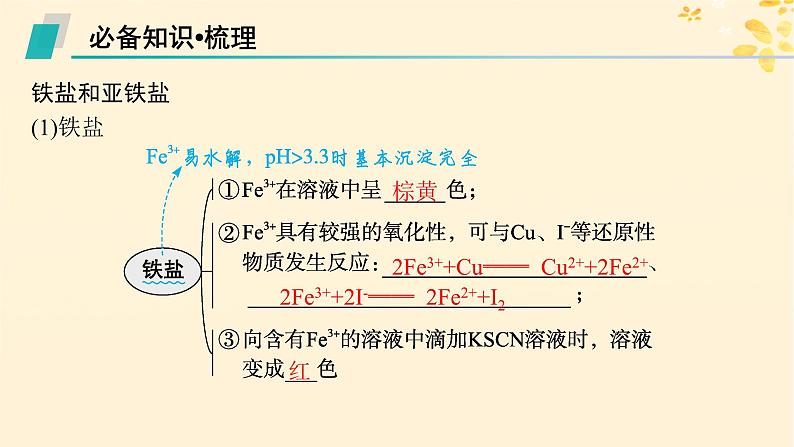
铁盐和亚铁盐(1)铁盐
2Fe3++Cu══ Cu2++2Fe2+
2Fe3++2I-══ 2Fe2++I2
2Fe2++Cl2══ 2Fe3++2Cl-
Zn+Fe2+══ Fe+Zn2+
【应用示例】在CuCl2、FeCl3的混合溶液中加入一定量铁粉和铜粉的混合物。(1)从氧化还原角度分析,氧化性:CuCl2 ________(填“>”或“<”,下同)FeCl3,还原性:Fe ________ Cu。 (2)若金属全部溶解,则溶液中一定存在的金属阳离子有_______________,可能存在的金属阳离子有________。 (3)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有________,一定不存在的金属阳离子有_____________。
考向1 铁盐和亚铁盐的性质及转化例1(教材改编题)欲探究铁及其化合物的还原性或氧化性,可供选用的试剂有:铁粉、FeCl3溶液、FeCl2溶液、氯水、酸性KMnO4溶液、锌片。下列说法中不正确的是( )A.在FeCl2溶液中加入锌片,溶液由浅绿色变为无色:Zn+Fe2+═Zn2++FeB.在FeCl3溶液中加入足量铁粉,溶液由棕黄色变为浅绿色,体现Fe3+的氧化性C.在酸性KMnO4溶液中滴加足量FeCl2溶液,溶液的紫红色逐渐褪去,体现Fe2+的还原性D.在FeCl2溶液中滴加氯水,溶液由浅绿色变为棕黄色:2Fe2++Cl2═2Fe3++2Cl-
[对点训练1] 硫酸亚铁的用途广泛,可以制备如图所示物质,下列说法错误的是( )
A.Fe4(OH)2(SO4)5属于碱式盐,可用作净水剂
C.可用稀硫酸和K3[Fe(CN)6]溶液检验铁红中是否含有FeCO3D.“冷却结晶”后的操作是过滤,“煅烧”操作的主要仪器有酒精灯、坩埚、玻璃棒
考向2 Fe2+和Fe3+的检验原理及方法例2(教材改编题)某实验小组同学为了检验某FeCl3溶液中是否含有FeCl2,设计了如下实验方案,其中最合理的是( )A.加入适量铜粉,观察溶液是否变蓝B.先滴加氯水,再滴加KSCN溶液,观察溶液是否变红C.滴加酸性KMnO4溶液,观察溶液是否褪色D.滴加K3[Fe(CN)6]溶液,观察是否生成蓝色沉淀
解析 加入适量铜粉无法检验FeCl2,A错误;先滴加氯水,Cl2可将FeCl2氧化生成FeCl3,不能判断是否含有FeCl2,B错误;Fe2+、Cl-都能被酸性KMnO4溶液氧化,不能判断是否含有FeCl2,C错误;若FeCl3溶液中含有FeCl2,滴加K3[Fe(CN)6]溶液,反应生成蓝色沉淀KFe[Fe(CN)6],实验现象最明显,该方案最合理,D正确。
[对点训练2] 为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其结论正确的是( )A.滴加KSCN溶液,溶液变红,说明铁粉变质B.滴加KSCN溶液,溶液未变红,说明铁粉未变质C.依次滴加氯水、KSCN溶液,溶液变红,说明铁粉全部变质D.滴加KSCN溶液,溶液未变红,再滴加氯水,溶液变红,说明铁粉全部变质
解析 取少量样品溶于盐酸,滴加KSCN溶液,溶液变红,则含有Fe3+,说明铁粉变质,A正确;滴加KSCN溶液,溶液未变红,则不含Fe3+,但还原铁粉有可能被氧化为Fe2+,B错误;依次滴加氯水、KSCN溶液,溶液变红,不能判断铁粉是否变质,C错误;滴加KSCN溶液,溶液未变红,再滴加氯水,溶液变红,说明溶液中含有Fe2+,但不能说明铁粉全部变质,D错误。
情境思考某兴趣小组用油性笔在一小块覆铜板上写上“化学”,然后浸入盛有FeCl3溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干(如图)。
(1)上述实验的原理是_______________________(用离子方程式表示)。 (2)该实验利用了FeCl3的________性,据此________(填“能”或“不能”)比较铁和铜的活泼性。 (3)为使使用后的“腐蚀液”能得到充分利用,应先加入足量________(填试剂名称,下同),充分反应后,过滤,再向滤液中加入足量________即可。
2Fe3++Cu══ 2Fe2++Cu2+
1.基于“价—类”二维图理解含铁物质的转化从物质类别和铁元素化合价两个维度总结、归纳铁及其重要化合物的性质与转化关系是掌握该部分内容的重要方法之一。
2.分析铁元素“价—类”二维图的3个角度(1)横向转化体现了铁元素同种价态不同类别物质(氧化物、碱、盐)之间的转化。①碱性氧化物(FeO、Fe2O3)都能与酸(H+)反应转化为盐(亚铁盐、铁盐);②盐(Fe2+、Fe3+)与碱(OH-)反应生成相应的碱[Fe(OH)2、Fe(OH)3];③难溶性碱受热分解一般生成对应的氧化物,如Fe(OH)3分解生成Fe2O3。(2)纵向转化体现铁元素不同价态同种类别物质之间的转化,主要体现物质的氧化性或还原性。(3)斜向转化体现铁元素不同价态、不同类别物质之间的转化,主要体现物质的氧化性和还原性。
考向1 铁元素的“价—类”二维图及应用例1(2023·广东梅州三模)价—类二维图和实验是学习元素及其化合物的重要方法。铁及其化合物的价—类二维图如图所示。下列说法正确的是( )
A.高温时,a与水蒸气反应转化为cB.若f、g都是盐酸盐,则这两种物质均可通过化合反应获得C.d可与足量的HI溶液发生复分解反应得到gD.若b和c的混合物中n(Fe)∶n(O)=5∶6,则b和c的质量比为20∶27
解析 根据铁元素的化合价以及物质种类可知,a为铁单质,b为FeO,c为Fe2O3, d为Fe(OH)3,e为Fe(OH)2,f为亚铁盐,g为铁盐,h为高铁酸盐。a为Fe,高温时Fe与水蒸气反应转化为Fe3O4,A项错误;f、g分别为FeCl2、FeCl3,两者均可通过化合反应获得,即Fe+2FeCl3═3FeCl2、2FeCl2+Cl2═2FeCl3,B项正确;d为氢氧化铁,Fe(OH)3中的+3价铁具有氧化性,HI具有还原性,两者发生氧化还原反应生成亚铁盐,得不到铁盐,C项错误;b和c分别为FeO和Fe2O3,设FeO的物质的量为x ml,Fe2O3的物质的量为y ml,则有(x+2y)∶(x+3y)=5∶6,解得x∶y=3∶1,则FeO和Fe2O3的质量比为(3×72)∶(1×160)=27∶20,D项错误。
[对点训练1] 如图为铁元素的“价—类”二维图,下列说法正确的是( )
解析 铁在高温下与水蒸气反应生成四氧化三铁和氢气,不能实现转化①,A错误;FeO为黑色固体,在空气中受热转化为Fe3O4,B错误;高铁酸盐中铁元素显+6价,处于高价态,具有强氧化性,C错误;加热Fe(OH)3发生分解反应生成氧化铁和水,可实现转化⑥;加盐酸,盐酸和氢氧化铁反应生成氯化铁和水,可实现转化③,D正确。
考向2 含铁化合物制备的流程“微设计”例2(2023·广东广州检测)从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体(FeCl3·6H2O)的流程如下。下列说法不正确的是( )
A.用酸性KMnO4溶液可检验溶液W中是否含有Fe2+B.试剂a是铁、试剂b是稀盐酸C.操作Ⅰ、操作Ⅱ均需用到漏斗,操作Ⅲ需用蒸发皿D.试剂c是氯气,在该流程中做氧化剂
解析 从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜,工业废液中加入试剂a为过量的铁,操作为过滤,得到滤渣Y为Fe、Cu,滤液X为氯化亚铁溶液,滤渣Y中加入试剂b为稀盐酸,溶解过量的铁生成氯化亚铁溶液,铜不溶,过滤得到铜和滤液Z为氯化亚铁溶液,滤液Z和X合并通入氯气,氧化氯化亚铁为氯化铁,溶液W蒸发结晶,过滤、洗涤、干燥得到氯化铁晶体。亚铁离子、氯离子都可以被高锰酸钾溶液氧化,用酸性KMnO4溶液不能检验溶液W中是否含有Fe2+,A错误;由最终得到FeCl3及其流程图可知,a是铁、b为稀盐酸,B正确;操作Ⅰ、Ⅱ是过滤,需用漏斗,操作Ⅲ是蒸发结晶,需用蒸发皿, C正确;c为氯气,氧化亚铁离子为铁离子的反应为2Fe2++Cl2═2Cl-+2Fe3+,D正确。
[对点训练2] 以赤铁矿(主要成分为Fe2O3,含少量Al2O3)为原料制备无水FeCl2的工艺流程如下。下列说法错误的是( )
A.“试剂1”可以是NaOH溶液B.鉴别“溶液2”中金属阳离子可用KSCN溶液C.“反应3”为化合反应D.将“溶液3”蒸干可制得无水FeCl2
解析 “试剂1”可以是NaOH溶液,加入试剂的目的是将Al2O3溶解转化为Na[Al(OH)4],从而除去杂质,A正确;“溶液2”为FeCl3溶液,鉴别溶液中的Fe3+应选择KSCN溶液,B正确;“反应3”为FeCl3溶液与Fe发生化合反应生成FeCl2,C正确;FeCl2中Fe2+具有还原性且易发生水解,若直接将溶液蒸干无法制得无水FeCl2,应隔绝空气,在HCl气流中蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到无水FeCl2,D错误。
进阶1 练易错·避陷阱1.(2023·广东汕头二模)铁及其化合物在生活中应用广泛,下列有关离子方程式书写正确的是( )A.将铁片投入稀硝酸中:Fe+2H+═Fe2++H2↑B.向FeCl3溶液中通入少量H2S:2Fe3++H2S═2Fe2++2H++S↓C.用铁氰化钾溶液检验Fe2+:Fe2++K3[Fe(CN)6]═KFe[Fe(CN)6]↓+2K+D.往Fe2(SO4)3溶液中加入过量Zn粉:2Fe3++Zn═2Fe2++Zn2+
解析 铁片与稀硝酸反应生成一氧化氮,不生成氢气,A错误;Fe3+具有较强的氧化性,可将H2S氧化为硫单质,离子方程式为2Fe3++H2S═2Fe2++2H++S↓,B正确;铁氰化钾溶于水可拆为离子的形式,离子方程式为Fe2++[Fe(CN)6]3-+K+═KFe[Fe(CN)6]↓,C错误;过量Zn将Fe3+还原为铁单质,离子方程式为2Fe3++3Zn═2Fe+3Zn2+,D错误。
2.根据下列实验操作和现象所得到的结论不正确的是( )
解析 向FeCl3溶液中滴加KI溶液,发生反应2Fe3++2I-═2Fe2++I2,再滴加淀粉溶液,溶液显蓝色,则氧化性:Fe3+>I2,B正确;向FeCl3溶液中滴加几滴KSCN溶液,溶液显红色,再加入少量铁粉,发生反应:2Fe3++Fe═3Fe2+,溶液红色褪去,则还原性:Fe>Fe2+,C正确;向FeSO4溶液中通入氯气,再滴加几滴KSCN溶液,溶液显红色,证明Fe2+被氧化为Fe3+,不能判断是否被完全氧化,D错误。
进阶2 练热点·提素能3.(2023·广东韶关期末)高铁酸钾(K2FeO4)是一种环保、高效、多功能的水处理剂。在水处理过程中,高铁酸钾转化为Fe(OH)3胶体。制备高铁酸钾流程如图所示:
下列叙述错误的是( )A.用FeCl2溶液吸收反应Ⅰ中尾气所得产物可再利用B.可利用丁达尔效应检验K2FeO4处理饮用水时有无Fe(OH)3胶体形成C.反应Ⅱ中氧化剂与还原剂的物质的量之比为2∶3D.溶解度大小:K2FeO4
A.通过化合反应和复分解反应均能直接得到dB.a→f→g→d的每步转化均可一步实现C.h具有强氧化性,在日常生活中可用于生活用水的消毒与净化D.c溶于氢碘酸的离子方程式为Fe2O3+6H+═2Fe3++3H2O
解析 如图,根据含铁化合物的价态可知,a为铁单质,b为FeO,c为Fe2O3,d为Fe(OH)3,e为Fe(OH)2,f为氯化亚铁等,g为氯化铁等,h为高铁酸盐。得到Fe(OH)3的方法有Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4或4Fe(OH)2+O2+2H2O═4Fe(OH)3,即通过化合反应和复分解反应均能直接得到氢氧化铁,A正确;a→f:2H++Fe═Fe2++H2↑,f→g:Cl2+2Fe2+═2Fe3++2Cl-,g→d:Fe3++3OH-═Fe(OH)3↓,故能实现a→f→g→d的转化关系,B正确;高铁酸盐具有强氧化性,在日常生活中可用于生活用水的消毒与净化,C正确;氧化铁与HI反应时,三价铁能将碘离子氧化,其反应的离子方程式为Fe2O3+6H++2I-═2Fe2++I2+3H2O,D错误。
进阶3 研真题·明考向5.(2022·湖南卷)为探究FeCl3的性质,进行了如下实验(FeCl3和Na2SO3溶液浓度均为0.1 ml·L-1)。
6.探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是( )
第16讲 铁盐、亚铁盐及相互转化-【精梳精讲】2024年高考化学大一轮精品复习课件(新教材): 这是一份第16讲 铁盐、亚铁盐及相互转化-【精梳精讲】2024年高考化学大一轮精品复习课件(新教材),共42页。PPT课件主要包含了复习目标,内容索引,专项突破,归纳整合,Fe3+,Fe2+与,Fe3+与,不共存,2分离除杂,Fe2+的盐溶液等内容,欢迎下载使用。
第13讲 铁盐、亚铁盐及相互转化-2024年高考化学一轮复习高频考点精讲(新教材新高考)课件PPT: 这是一份第13讲 铁盐、亚铁盐及相互转化-2024年高考化学一轮复习高频考点精讲(新教材新高考)课件PPT,共46页。PPT课件主要包含了复习目标,考点一,必备知识,易错辨析,专项突破,特别提醒,考点二,含铁物质的转化与制备,热点强化等内容,欢迎下载使用。
人教版 (2019)必修 第一册第二节 金属材料教案配套ppt课件: 这是一份人教版 (2019)必修 第一册第二节 金属材料教案配套ppt课件,共42页。PPT课件主要包含了目录索引等内容,欢迎下载使用。












