



备战2025届新高考化学一轮总复习第10章化学实验基础和综合探究第55讲离子的检验物质的鉴别与推断课件
展开1.掌握常见离子或物质的检验方法。2.会利用离子的特征检验方法进行物质的鉴别。3.能根据实验现象推断溶液中的某些离子或混合物中的某些物质。
考点一 常见离子的检验
考点二 物质的鉴别与推断
答题模板5离子检验的操作及现象描述
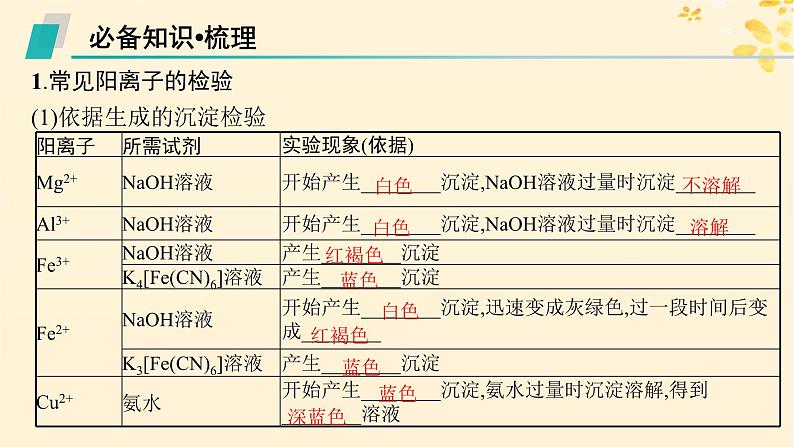
1.常见阳离子的检验(1)依据生成的沉淀检验
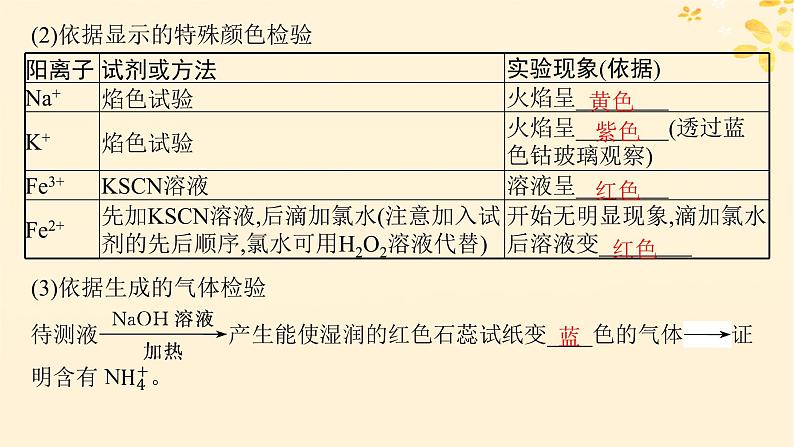
(2)依据显示的特殊颜色检验
(3)依据生成的气体检验
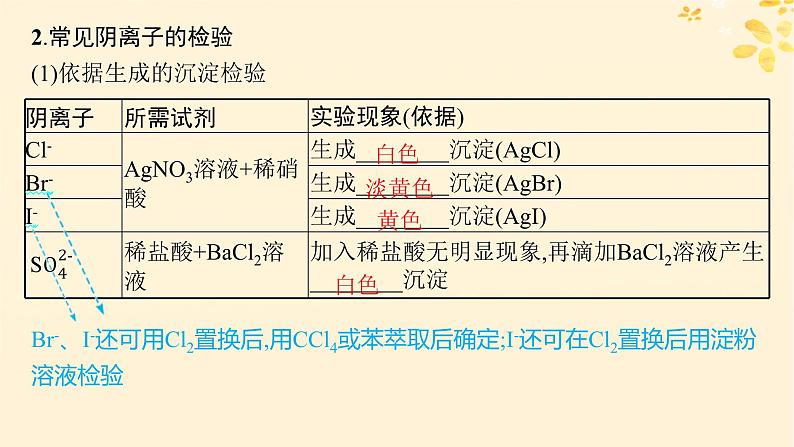
2.常见阴离子的检验(1)依据生成的沉淀检验
Br-、I-还可用Cl2置换后,用CCl4或苯萃取后确定;I-还可在Cl2置换后用淀粉溶液检验
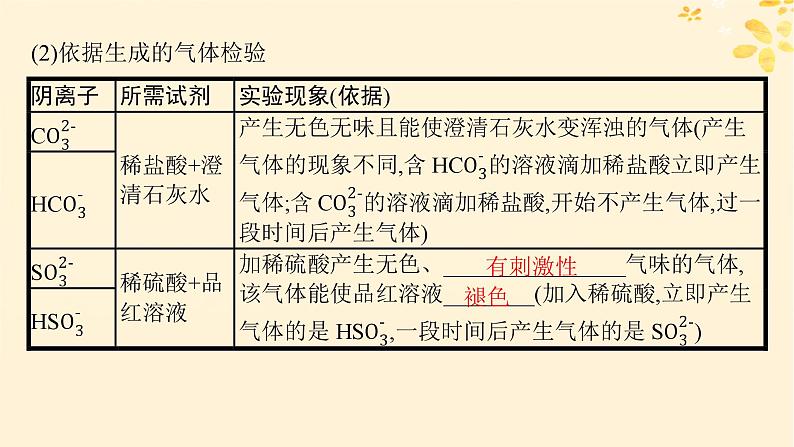
(2)依据生成的气体检验
[对点训练1] 下列关于离子检验的说法正确的是( )A.检验溶液中是否含有Ba2+:取少量待测液,向其中加入少量稀硫酸,若有白色沉淀产生,则溶液中含有Ba2+B.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是酸性KMnO4溶液
考向2 从定性、定量的角度推断离子例2某溶液X含有下表中的5种离子,且其物质的量浓度均为0.1 ml·L-1(不考虑水的电离与离子的水解)。向溶液X中加入足量稀盐酸,有无色气体产生,经分析反应前后阴离子种类不变。
思路导引推断溶液X中离子种类的思路如下:
A.向原溶液中加K3[Fe(CN)6]溶液,无明显现象B.原溶液中c(Cl-)≥0.1 ml·L-1C.用洁净的铂丝蘸取原溶液,在酒精灯上灼烧,火焰呈黄色D.将湿润的红色石蕊试纸靠近实验产生的气体,试纸变蓝
归纳总结(1)解答溶液中离子综合推断题的思维流程
(2)离子推断的“四原则”
物质的鉴别:根据物质特有的性质对两种或两种以上的物质进行区分。如NaCl和KNO3两种无色溶液可以用AgNO3溶液来区分。1.物质鉴别的思路(1)鉴别主要是寻找各物质的特殊现象,包括颜色、状态、气味、反应情况等。(2)如果要加入试剂进行鉴别,一定要先取样,不能直接对样品进行鉴别。(3)选用鉴别方法时先简单后复杂,先考虑物理方法后考虑化学方法。
考向1 物质的鉴别方法例1(2023·山东卷)鉴别浓度均为0.1 ml·L-1的NaClO、Ba(OH)2、Al2(SO4)3三种溶液,仅用下列一种方法不可行的是( )A.测定溶液pHB.滴加酚酞试剂C.滴加0.1 ml·L-1 KI溶液D.滴加饱和Na2CO3溶液
解析 ClO-水解使NaClO溶液显碱性,Ba(OH)2属于强碱,Al3+水解使Al2(SO4)3溶液显酸性,因此可以通过测定溶液pH的方法鉴别这三种浓度相等的溶液,A项不符合题意。三种溶液中滴加酚酞试剂的现象分别为NaClO溶液先变红后褪色,Ba(OH)2溶液变红,Al2(SO4)3溶液无明显现象,B项不符合题意。KI溶液与Ba(OH)2、Al2(SO4)3都不反应,二者无法鉴别,C项符合题意。三种溶液中滴加饱和Na2CO3溶液的现象分别为NaClO溶液无明显现象,Ba(OH)2溶液中产生白色沉淀,Al2(SO4)3溶液中既有白色沉淀又有气体产生,D项不符合题意。
[对点训练1] (2023·湖南卷)取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为0.1 ml·L-1),反应现象没有明显差别的是( )
解析 向氨水中滴加AgNO3溶液,开始产生白色沉淀,且沉淀立即消失,当AgNO3溶液滴加到一定量时,可较长时间出现白色沉淀;向AgNO3溶液中滴加氨水,开始产生白色沉淀,一段时间后,继续滴加氨水,白色沉淀消失,A项不符合题意。向NaOH溶液中滴加Al2(SO4)3溶液,开始无明显现象,当Al2(SO4)3溶液滴加到一定量时,产生白色沉淀;向Al2(SO4)3溶液中滴加NaOH溶液,开始产生白色沉淀,后白色沉淀消失,B项不符合题意。向H2C2O4溶液中滴加酸性KMnO4溶液,紫红色立即褪去,一段时间后,酸性KMnO4溶液过量,溶液呈现紫红色;向酸性KMnO4溶液中滴加H2C2O4溶液,开始酸性KMnO4溶液不褪色,一段时间后,H2C2O4溶液过量,酸性KMnO4溶液褪色,C项不符合题意。KSCN溶液与FeCl3溶液,无论二者滴加顺序怎样,反应的现象一样,溶液都呈现红色,D项符合题意。
考向2 混合物成分的推断例2(2022·全国乙卷)某白色粉末样品,可能含有Na2SO4、Na2SO3、Na2S2O3和Na2CO3。取少量样品进行如下实验:①溶于水,得到无色透明溶液。②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出,离心分离。③取②的上层清液,向其中滴加BaCl2溶液有沉淀生成。该样品中确定存在的是( )A.Na2SO4、Na2S2O3B.Na2SO3、Na2S2O3C.Na2SO4、Na2CO3D.Na2SO3、Na2CO3
[对点训练2] (2020·全国Ⅱ卷)某白色固体混合物由NaCl、KCl、MgSO4、CaCO3中的两种组成,进行如下实验:①混合物溶于水,得到澄清透明溶液;②做焰色试验,通过蓝色钴玻璃可观察到紫色;③向溶液中加碱,产生白色沉淀。根据实验现象可判断其组成为( )A.KCl、NaClB.KCl、MgSO4C.KCl、CaCO3D.MgSO4、NaCl
解析 ①混合物溶于水,得到澄清透明溶液,则不含CaCO3;②做焰色试验,通过蓝色钴玻璃可观察到紫色,可确定含有钾元素,即含有KCl;③向溶液中加碱,产生白色沉淀,则应含有MgSO4,综合以上分析可知,混合物由KCl和MgSO4两种物质组成。
进阶1 练易错·避陷阱1.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
进阶2 练热点·提素能3.(2023·广东肇庆检测)下列实验操作能达到实验目的的是( )
解析 碳碳双键具有还原性,能使酸性高锰酸钾溶液褪色,则向苯中加入适量酸性高锰酸钾溶液可检验苯分子中是否含碳碳双键,A符合题意;加入AgNO3溶液之前,需加稀硝酸酸化,因为NaOH能和AgNO3反应从而干扰实验,B不符合题意;苯酚和溴水反应生成的三溴苯酚会溶于苯,通过分液不能将其除去,C不符合题意;检验酸性条件下淀粉的水解产物中是否含有葡萄糖,先向水解液中加入氢氧化钠溶液将溶液调成碱性,再加入新制Cu(OH)2加热煮沸,D不符合题意;故选A。
4.下列实验操作及现象与结论均一定正确的是( )
解析 焰色为黄色,说明含有钠元素,可能含有NaOH,A项错误;乙烯使酸性高锰酸钾溶液褪色体现的是还原性,B项错误;将硫酸滴加到纯碱中,产生的气体通入水玻璃中,产生白色沉淀,说明酸性:H2SO4>H2CO3>H2SiO3,即非金属性:S>C>Si,C项正确;原溶液中本来就含有Fe3+也产生同样现象,D项错误。
进阶3 研真题·明考向5.(2023·辽宁卷)下列鉴别或检验不能达到实验目的的是( )A.用石灰水鉴别Na2CO3与NaHCO3B.用KSCN溶液检验FeSO4是否变质C.用盐酸酸化的BaCl2溶液检验Na2SO3是否被氧化D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
解析 Na2CO3和NaHCO3与石灰水反应都能生成难溶的CaCO3沉淀,A项符合题意;KSCN与Fe3+能生成红色物质,可用于检验FeSO4是否变质,B项不符合题意;Na2SO3被氧化为Na2SO4,Na2SO4与BaCl2反应生成的BaSO4不溶于盐酸,C项不符合题意;乙醛能与银氨溶液发生银镜反应,而乙醇不能,D项不符合题意。
6.(2023·全国新课标卷)根据实验操作及现象,下列结论中正确的是( )
例(2023·浙江1月选考卷,18节选)化合物X由三种元素组成,某学习小组按如下流程进行实验:
设计实验检验溶液I(含硝酸和硝酸铵)中的阳离子: ___________________。
1.(1)(2021·广东卷节选)某氯水久置后不能使品红溶液褪色,可推测氯水中________已分解。检验此久置氯水中Cl-存在的操作及现象是_________________________________。
向溶液中加入过量稀硝酸,再加入少量AgNO3溶液,若有白色沉淀生成,则证明原溶液中含有Cl-
备战2025届新高考化学一轮总复习第10章化学实验基础和综合探究第59讲物质含量测定和性质探究综合实验课件: 这是一份备战2025届新高考化学一轮总复习第10章化学实验基础和综合探究第59讲物质含量测定和性质探究综合实验课件,共60页。PPT课件主要包含了课标指引,目录索引,素养发展进阶,必备知识•梳理,关键能力•提升,分液漏斗,5×10-5,棕色细口瓶,溶液变蓝,溶液蓝色褪去等内容,欢迎下载使用。
备战2025届新高考化学一轮总复习第10章化学实验基础和综合探究第58讲以物质制备为主的综合实验课件: 这是一份备战2025届新高考化学一轮总复习第10章化学实验基础和综合探究第58讲以物质制备为主的综合实验课件,共58页。PPT课件主要包含了课标指引,考点一无机物的制备,目录索引,素养发展进阶,必备知识•梳理,关键能力•提升,缺少尾气处理装置,蒸馏烧瓶,相关信息列表如下,球形冷凝管等内容,欢迎下载使用。
备战2025届新高考化学一轮总复习第10章化学实验基础和综合探究第57讲简单实验方案的设计与评价课件: 这是一份备战2025届新高考化学一轮总复习第10章化学实验基础和综合探究第57讲简单实验方案的设计与评价课件,共31页。PPT课件主要包含了课标指引,目录索引,素养发展进阶,必备知识•梳理,关键能力•提升等内容,欢迎下载使用。












