

江苏省泰州市靖江市八校联考2024届九年级上学期12月月考化学试卷(含答案)
展开一、单选题
1.全国文明城市建设关系淮安长远发展,事关各行各业,惠及全市人民,人人都是主力军,个个都是责任人。淮安市民的下列生活方式中,你认为不可行的是( )
A.乘电动公交车,提倡低碳出行B.淘米水浇花,节约淡水资源
C.实施绿化工程,防治扬尘污染D.回收垃圾,直接露天焚烧处理
2.丝绸之路将我国古代发明与技术传送到了国外。下列我国古代生产工艺中没有发生化学变化的是( )
A.烧制瓷器B.湿法炼铜C.高粱酿酒D.纺纱织布
3.下列物质的用途中,主要利用化学性质的是( )
A.用酒精作实验室燃料B.用液氮作医疗冷冻剂
C.用干冰制造舞台云雾D.用武德合金作保险丝
4.实验室用锌和一定体积稀硫酸制取氢气,下列操作正确的是( )
A.检查气密性B.加入锌粒
C.制取氢气D.收集氢气
5.门捷列夫说:“没有观察就没有接踵而来的前进。”下列实验现象描述正确的是( )
A.硫在氧气中燃烧发出淡蓝色的火焰
B.镁带在空气中燃烧,发出耀眼的白光,生成白色的氧化镁
C.将生铁粉末投入盛有过量的稀盐酸的烧杯中,充分反应后仍有黑色残渣
D.将铜片投入到稀硫酸中,产生大量气泡
6.目前主流的新能源车都采用锂电池储能,结合图示,有关锂的说法正确的是( )
A.属于非金属元素B.锂离子符号是
C.表示核内有3个电子D.相对原子质量是6.941g
7.“上善若水,水善利万物而不争”。下列有关水的说法正确的是( )
A.明矾可以将硬水转化为软水
B.水资源可以循环利用,没必要担心淡水资源不足
C.经过沉淀、过滤、吸附、消毒以后得到的自来水仍然不是纯净物
D.电解水说明水由氢气和氧气组成
8.如图所示,实验室模拟粉尘爆炸试验.连接好装置,在小塑料瓶中放入下列干燥的粉末,点燃蜡烛,快速鼓入大量的空气,肯定观察不到爆炸现象的是( )
A.镁粉B.面粉C.煤粉D.大理石粉
9.金银花作为常见的中药材,具有清热解毒、消炎退肿等功效,其有效成分之一是绿原酸。下列有关绿原酸的说法正确的是( )
A.绿原酸分子由碳、氢、氧三个元素组成
B.绿原酸中碳元素的质量分数最大
C.绿原酸的相对分子质量是354g
D.绿原酸中碳、氢、氧元素的质量比为
10.下列归纳和总结完全正确的一组是( )
A.AB.BC.CD.D
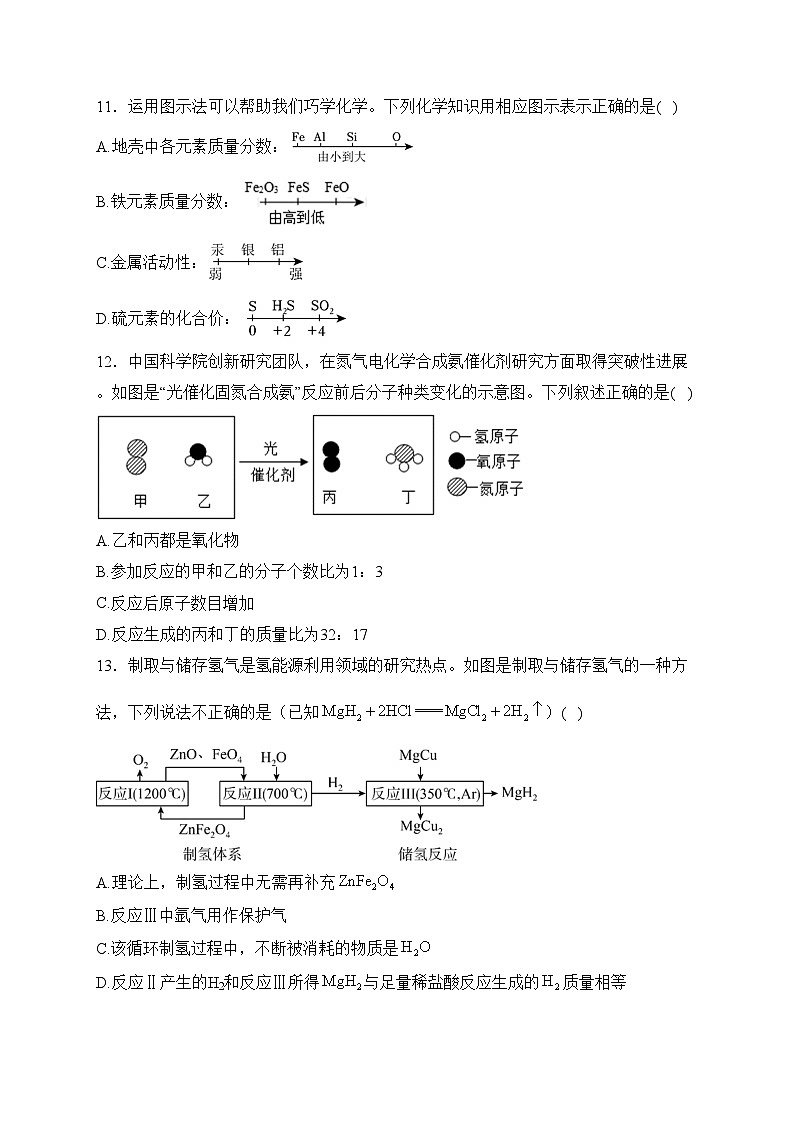
11.运用图示法可以帮助我们巧学化学。下列化学知识用相应图示表示正确的是( )
A.地壳中各元素质量分数:
B.铁元素质量分数:
C.金属活动性:
D.硫元素的化合价:
12.中国科学院创新研究团队,在氮气电化学合成氨催化剂研究方面取得突破性进展。如图是“光催化固氮合成氨”反应前后分子种类变化的示意图。下列叙述正确的是( )
A.乙和丙都是氧化物
B.参加反应的甲和乙的分子个数比为1:3
C.反应后原子数目增加
D.反应生成的丙和丁的质量比为32:17
13.制取与储存氢气是氢能源利用领域的研究热点。如图是制取与储存氢气的一种方法,下列说法不正确的是(已知)( )
A.理论上,制氢过程中无需再补充
B.反应Ⅲ中氩气用作保护气
C.该循环制氢过程中,不断被消耗的物质是
D.反应Ⅱ产生的H2和反应Ⅲ所得与足量稀盐酸反应生成的质量相等
二、多选题
14.物质的鉴定、鉴别和除杂是重要的实验技能。下列实验方法不能达到实验目的的是( )
A.AB.BC.CD.D
15.推理是化学学习中常用的思维方法。下列推理正确的是( )
A.原子在化学变化中不能再分,则分子在化学变化中也不能再分
B.同种元素质子数相同,因此质子数相同的原子一定是同种元素
C.稀有气体元素的原子(除外)最外层电子数都为8,而最外层电子数为8的粒子不一定是稀有气体元素的原子
D.过氧化氢溶液能分解产生氧气,因此过氧化氢中含有氧分子
三、填空题
16.2023年5月30日“神舟十六号”太空飞船成功发射,标志着我国载人航天进入新的发展阶段。
Ⅰ.航天材料
(1)航天员头盔的面窗两层之间充有高纯氮气,从空气中分离出氮气的过程属于_______(填“物理”或“化学”)变化。
(2)太阳能电池板需要使用铝合金箔片,铝合金能加工成箔片是利用了金属的_______性。
Ⅱ.生命保障
(3)太空舱的氧气主要来自于水的电解,电解水反应的化学方程式为_______。
(4)航天员呼出的水蒸气经冷凝、净化可作为核心舱中的饮用水,净化采用RO反渗透膜(只允许水分子和少部分离子通过),原理类似于实验操作中的_______。
(5)空间站的呼吸循环系统和水循环系统中都会用到活性炭去除杂质,主要利用活性炭的_______性。
Ⅲ.能源系统
(6)长征2F型火箭使用的推进剂为偏二甲肼和四氧化二氮,其中四氧化二氮中,氮元素的化合价为_______。
(7)太空舱使用锂电池。可以通过与在高温下发生置换反应得到,该反应的化学方程式为_______。
四、实验题
17.根据如图所示装置图,回答有关问题:
(1)写出图中标号仪器的名称:①_______。
(2)实验室中用A装置制取氧气,反应的化学方程式为_______。
(3)用大理石和稀盐酸制取二氧化碳,反应的化学方程式为_______,如用G装置收集,验满的方法是:_______。发生装置选用C装置代替B装置的优点是_______,下图中哪些装置与C装置有相同的优点_______。
(4)实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,制取甲烷可选择的发生装置是_______,如选择E装置收集甲烷,证明甲烷气体已收集满的现象是_______。
(5)用一定浓度、一定体积的稀硫酸和足量的锌粒反应制取氢气,记录实验数据如表:
分析表中数据,随着反应的进行,反应的速率逐渐_______(选填“加快”、“减慢”或“不变”),引起反应速率变化的主要原因是_______,写出该反应的化学方程式_______。
18.我国力争在2060年前实现“碳中和”。“碳中和”是指在一定时间内的排放量和吸收量基本相当。
(1)工业上化石燃料的大量燃烧是排放逐年升高的主要原因,的过度排放会导致_______的加剧。
【的封存】
(2)地质封存:将在高压、低温的条件下转化为液态,注入地层中。从微观角度分析,从气态转化为液态,分子的间隙_______。
(3)海洋封存:将运输到封存地点,灌注于海洋深处。该方案可能导致海水逐渐酸化,原因是_______(用化学方程式表示)。
【的转化】
(4)已知和在合适催化剂和一定温度下可以发生反应,生成两种氧化物。某研究小组设计如图1装置(固定装置省略)探究该反应的产物。
查阅资料:
①无水硫酸铜是一种白色固体,遇水变成蓝色。
②碱石灰能充分吸收二氧化碳且不与氢气、一氧化碳反应。
③是一种还原性气体,高温下可还原氧化铜、氧化铁等金属氧化物。
实验现象及结论:B中白色固体变成蓝色,说明和反应生成了_______;D中红棕色固体变为黑色,E中澄清石灰水变浑浊,说明与反应生成了_______。装置D中反应的化学方程式_______。
实验反思:图1装置中有一处明显不足,请指出_______。若去掉装置E,则不能证明与反应生成了,理由是_______。
【的捕集】
(5)二氧化碳的“捕集”技术实现了二氧化碳的捕捉、封存和资源化利用。图2为捕集二氧化碳流程图。
已知:反应Ⅰ的化学方程式为:;不稳定,受热易分解。
请回答相关问题:
①反应Ⅰ需控制在一定温度范围内进行,原因是_______。
②上述捕集的流程中,可循环利用的物质是_______。
19.我国高铁创造的中国速度令世界瞩目,某学习小组对高铁建设中的钢铁锈蚀进行探究。
【提出问题】铁锈蚀与哪些因素有关。
【查阅资料】碳粉可加快铁的锈蚀,碳粉不与盐酸反应;氧化铁能与盐酸反应,不产生气体。
【设计实验】
实验一:定性探究铁锈蚀的因素
取四枚大小相同的洁净无锈铁钉分别放入试管,进行图1实验,现象如下表。
(1)对比A、B、C试管中实验现象,说明铁锈蚀是与空气中的_______发生化学反应。
(2)对比A和D试管中实验现象,说明铁锈蚀快慢与_______有关。
(3)生活中铁制品易生锈而铝制品不易生锈的原因是_______(用化学方程式表示)。
实验二:定量探究影响铁锈蚀的因素
小组设计了图2装置,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,时刻加入2mL饱和溶液后,再将一只装有5mL稀盐酸的注射器插到烧瓶上(此时没有推动注射器活塞),采集数据。
(4)据图3,说明铁生锈是_______(填“放热”或“吸热”),~这段时间反应并未停止但温度却开始降低,原因是_______。
(5)根据图2、图4分析,时刻后压强突然变大,原因是_______。
实验三:测定部分生锈的铁粉中铁的含量
(6)连接如图5装置。取部分生锈的铁粉(铁和氧化铁的混合物)0.6g于锥形瓶中,加入足量稀盐酸进行实验。完全反应后,测得生成气体体积为0.2L,已知该条件下氢气密度为0.09g/L,根据以上数据,请计算该固体中铁的质量分数。(写出计算过程)
(7)学习小组有同学提出;用这种方法测得的气体体积不够准确,可能会导致测定的铁的质量分数变大,可能的原因是_______(填序号)。
a、装置的气密性不好
b、铁与盐酸反应放热
c、生成的气体会部分滞留在锥形瓶中
d、没有扣掉加入的盐酸的体积
【反思评价】
(8)小丽同学猜测:铁锈蚀的快慢还可能与氧气的浓度有关,为判断该猜测是否正确,请你设计实验验证小丽同学的猜想,简述实验方案_______。(实验方案包括操作、现象和结论)
参考答案
1.答案:D
解析:A、乘电动公交车,提倡低碳出行可以减少二氧化碳的排放,缓解温室效应,措施可行;
B、淘米水浇花,节约淡水资源,这有助于保护水资源,措施可行;
C、实施绿化工程,防治扬尘污染可以防止空气污染,措施可行;
D、露天焚烧垃圾会产生大量的烟尘和有害气体而造成空气污染,措施不可行。
故选:D。
2.答案:D
解析:A、烧制瓷器过程中有新物质生成,属于化学变化;
B、湿法炼铜过程中有新物质铁生成,属于化学变化;
C、高粱酿酒过程中有新物质生成,属于化学变化;
D、纺纱织布过程中只是形状发生改变,没有新物质生成,属于物理变化。
故选D。
3.答案:A
解析:A、酒精作燃料是因为酒精具有可燃性,可燃性属于化学性质,故正确;
B、液氮作冷冻剂是因为液氮挥发吸热,不需要发生化学变化就能表现出来,属于物理性质,故错误;
C、干冰为固体二氧化碳,干冰升华吸热,则可制造舞台云雾,不需要发生化学变化就能表现出来,属于物理性质,故错误;
D、合金作保险丝是因为其熔点低,熔点属于物理性质,故错误。
故选:A。
4.答案:A
解析:A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴试管外壁,若导管口有气泡冒出,装置不漏气,图中所示操作正确。
B、锌粒是金属颗粒,加入试管时,先把试管横放,然后用镊子夹取锌粒,放在试管口,再把试管慢慢竖起来,使锌粒缓缓滑到试管底部,避免打破试管,图中所示操作错误。
C、锌粒与稀硫酸反应生成氢气,长颈漏斗要伸入液面以下,防止生成的氢气逸出,图中所示操作错误。
D、氢气的密度比空气的小,应用向下排空气法收集,图中所示操作错误。
故选:A。
5.答案:C
解析:A、硫在氧气中燃烧,产生明亮的蓝紫色火焰,产生一种具有刺激性气味的气体,故选项说法错误。
B、镁带在空气中燃烧,发出耀眼的白光,生成白色的氧化镁是实验结论而不是实验现象,故选项说法错误。
C、生铁的主要成分是铁,含有碳等杂质,将生铁粉末投入盛有过量的稀盐酸的烧杯中,铁能与稀盐酸反应生成氯化亚铁和氢气,碳不能与稀盐酸反应,充分反应后仍有黑色残渣,故选项说法正确。
D、将铜片投入到稀硫酸中,不反应,无明显现象,故选项说法错误。
故选:C。
6.答案:B
解析:A、锂为金字旁,属于金属元素,该选项说法不正确;
B、锂原子最外层电子数为1,在化学变化中易失去1个电子形成带1个单位正电荷的离子,则符号为,该选项说法正确;
C、圆圈内的数字表示原子的质子数,即核内有3个质子,该选项说法不正确;
D、相对原子质量的单位为“1”,而不是“g”,该选项说法不正确。
故选B。
7.答案:C
解析:A、活性炭具有吸附性,吸附色素和异味,不能降低可溶性钙、镁化合物的含量,不能降低水的硬度,故选项说法错误。
B、地球上的水总储备虽然很大,但大部分是海水,淡水只约占全球水储量的2.53%,可利用的淡水资源不到全球总储水量的1%,故选项说法错误。
C、经过沉淀、过滤、吸附、消毒以后得到的自来水仍含有可溶性杂质,仍然不是纯净物,故选项说法正确。
D、电解水的实验中,水分解生成氢气和氧气,氢气是由氢元素组成,氧气是由氧元素组成,在化学反应中元素的种类不变,说明了水是由氢元素和氧元素组成的,水是纯净物,不是由氢气和氧气组成,故选项说法错误。
故选:C。
8.答案:D
解析:A、煤粉具有可燃性,点燃蜡烛,快速吸入大量的空气,可能会发生爆炸,故选项错误。
B、面粉具有可燃性,点燃蜡烛,快速吸入大量的空气,可能会发生爆炸,故选项错误。
C、镁粉具有可燃性,点燃蜡烛,快速吸入大量的空气,可能会发生爆炸,故选项错误。
D、大理石粉末不具有可燃性,点燃蜡烛,快速吸入大量的空气,肯定观察不到爆炸现象,故选项正确。
故选:D。
9.答案:B
解析:A.元素只讲种类,不讲个数,绿原酸由碳、氢、氧三种元素组成,故A不正确;
B.元素的质量分数=,而绿原酸中碳、氢、氧三种元素质量比为(16×12):(18×1):(9×16)=32:3:24
,由此可知碳元素的质量分数最大,故B正确;
C.相对分子质量的单位为“1”,而不是“g”,故绿原酸的相对分子质量是354,故C不正确;
D.绿原酸中碳、氢、氧三种元素质量比为(16×12):(18×1):(9×16)=32:3:24,故D不正确。
故选:B。
10.答案:C
解析:A、氯化钠是由钠离子和氯离子构成的,故A错误;
B、房屋失火,用水灭火是为了降低可燃物的温度到着火点以下,故B错误;
C、海水中含量最多的元素是氧元素,人类利用最早的金属是铜,故C正确;
D、中的2表示一个二氧化氮分子中含有2个氧原子,故D错误。
故选C。
11.答案:A
解析:A、地壳中元素含量由高到低的四种元素分别是氧、硅、铝、铁,与数轴关系一致,正确;
B、中铁元素的质量分数为,中铁元素的质量分数为,中硫元素的质量分数为,与数轴关系不一致,错误;
C、三种金属活动性由弱到强的顺序是银、汞、铝,与数轴关系不一致,错误;
D、在化合物中,各元素的正负化合价代数和为0。S为单质,硫元素为0价,中氢元素显+1价,则硫元素显-2价,中氧元素显-2价,则硫元素显+4价,与数轴关系不一致,错误;
故选A。
12.答案:B
解析:A、乙和丙分别是水和氧气,水属于氧化物,氧气属于单质,故选项说法错误。
B、由“光催化固氮合成氨”反应前后分子种类变化的示意图,该反应是氮分子和水分子反应生成氧分子和氨分子,反应的化学方程式为则参加反应的甲和乙的分子个数比为2:6=1:3,故选项说法正确。
C、反应前后原子的数目不变,故选项说法错误。
D、反应的化学方程式为反应生成的丙和丁的质量比为(32×3):(17×4)=24:17,故选项说法错误。
故选:B。
13.答案:D
解析:A、制氢体系中的反应原理可知,可以循环使用,无需添加,故A正确;
B、氢气的化学性质比较活泼,与氧气混合加热极易发生爆炸,所以反应川中氩气用作保护气,故B正确;
C、制氢体系中的反应是水在一定条件下反应生成氢气和氧气,所以该循环制氢过程中,不断被消耗的物质是,故C正确;
D、由可知,氢化镁生成的氢气的质量包括氢化镁中氢元素、盐酸中氢元素的质量之和,所以反应Ⅱ产生的和反应Ⅲ所得与足量稀盐酸反应生成的质量不相等,故D错误。
故选:D。
14.答案:AC
解析:A、在二氧化锰的催化作用下、在加热条件下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,故选项实验方法不能达到实验目的。
B、铜与氧气在加热条件下反应生成氧化铜,分别灼烧,无明显现象的是黄金,表面逐渐变黑的是假黄金(铜锌合金),可以鉴别,故选项实验方法能达到实验目的。
C、溶解后,铁和硫酸铜溶液反应生成硫酸亚铁溶液和铜,不能分离出和,故选项实验方法不能达到实验目的。
D、将铁丝插入溶液中,铁丝的表面覆盖一层银白色物质,溶液颜色由无色变为浅绿色,说明铁比银的金属活动性强,故选项实验方法能达到实验目的。
故选:AC。
15.答案:BC
解析:A、在化学变化中原子不能再分,但不能类推出分子也不能再分,分子在化学变化中是可以再分的,故A错误;
B、元素是指具有相同核内质子数的一类原子的总称,所以同种元素质子数相同,因此质子数相同的原子一定是同种元素,故B说法正确;
C、稀有气体元素原子的最外层电子数一般为8,则最外层电子数为8的粒子不一定是稀有气体元素的原子,如最外层电子为8,但不是稀有气体元素的原子,故C说法正确;
D、过氧化氢溶液能分解产生氧气,因此过氧化氢中含有氧元素,过氧化氢中含有过氧化氢分子,不含有氧分子,故D说法错误。
故选:BC。
16.答案:(1)物理
(2)延展
(3)
(4)过滤
(5)吸附
(6)+4价
(7)
解析:(1)空气中本来就有氮气,所以分离氮气没有新物质生成是物理变化;
(2)铝合金能加工成箔片是因为金属通常有良好的延展性,所以是利用金属有良好的延展性来加工的;
(3)水在通电的条件下生成氢气和氧气,化学方程式为:;
(4)净化可作为核心舱中的饮用水,净化采用RO反渗透膜(只允许水分子和少部分离子通过)进行,这一操作与化学实验操作过滤的原理一致,都是利用颗粒大小不同进行分离的;
(5)呼吸循环系统和水循环系统中都会用到活性炭去除杂质,主要利用活性炭具有疏松多孔的结构,可吸附一些杂质的性质;
(6)四氧化二氮中,氧元素通常显-2价,则设氮元素的化合价为x,
2x+(-2)×4=0,则x=+4价;
(7)可以通过与在高温下发生置换反应得到,由于发生的是置换反应,所以生成物应是氧化铝和锂,化学方程式为:。
17.答案:(1)长颈漏斗
(2)
(3);将燃着的木条放在b口,若木条熄灭,则说明已收集满;控制反应的开始与停止;②④或④②
(4)A;集气瓶口有大气泡产生
(5)减慢;硫酸浓度减小;
解析:(1)由图可知,仪器①的名称是长颈漏斗;
(2)装置A适用于固体加热制氧气,因为试管口处有一团棉花,所以是加热高锰酸钾制氧气,高锰酸钾受热分解成锰酸钾、二氧化锰和氧气,反应的化学方程式为;
(3)用大理石和稀盐酸制取二氧化碳,同时生成氯化钙和水,反应的化学方程式为,如用G装置收集,二氧化碳的密度比空气大,二氧化碳应从导管a端通入,二氧化碳不燃烧,也不支持燃烧,则验满的方法是将燃着的木条放在导管6端,若木条熄灭,说明二氧化碳已收集满,装置C带有多孔隔板和活塞开关,关闭活塞开关,内部气体增多,压强增大,液体被压入长颈漏斗,固液分离,反应停止,打开活塞开关,气体导出,压强减小,液体重新进入试管,固液接触,反应发生,则C装置的优点是可以控制反应的发生和停止;①中固体在容器的最底部,不能使固液分离,不能控制反应的发生和停止,故①不符合题意;
②中导管关闭后,气体将盐酸压回烧杯,固液分离,反应停止,可以控制反应的发生和停止,故②符合题意;
③中导管伸入液面以下气体无法排出,容易使胶塞冲出,故3不符合题意;
④中导管关闭后,气体将盐酸压向左侧,固液分离,反应停止,可以控制反应的发生和停止,故④符合题意;
故选:②④;
(4)实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,属于固固加热型,则制取甲烷可选择的发生装置是A,如选择E装置排水法收集甲烷,证明甲烷气体已收集满的现象是集气瓶口有大气泡向外冒出;
(5)分析表中数据,随着反应的进行,增加的氢气体积逐渐减小,则说明反应的速率逐渐减慢,随着反应的进行,硫酸的浓度减小,则反应的速率减慢,锌和硫酸反应生成硫酸锌和氢气,反应的化学方程式为。
18.答案:(1)温室效应
(2)变小
(3)
(4)水或;一氧化碳或;;缺少尾气处理装置;高温条件下氢气也能和氧化铁反应生成铁和水
(5)不稳定,受热易分解;碳酸钾或
解析:(1)工业上化石燃料的大量燃烧是排放逐年升高的主要原因,的过度排放会导致温室效应的加剧。
故答案为:温室效应。
(2)地质封存:将在高压、低温的条件下转化为液态,注入地层中。从微观角度分析,从气态转化为液态,分子的间隙变小。故答案为:变小。
(3)海洋封存:将运输到封存地点,灌注于海洋深处。该方案可能导致海水逐渐酸化,原因是。故答案为:。
(4)实验现象及结论:B中白色固体变成蓝色,是因为水和硫酸铜反应生成蓝色固体五水硫酸铜,说明与反应生成了水;D中红棕色固体变为黑色,E中澄清石灰水变浑浊,是因为高温条件下一氧化碳和氧化铁反应生成铁和二氧化碳,二氧化碳能使澄清石灰水变浑浊,说明与反应生成了一氧化碳。装置D中反应的化学方程式是。图1装置中有一处明显不足,即没有处理尾气。若去掉装置E,则不能证明与反应生成了,理由是过量的氢气也能和氧化铁反应。
19.答案:(1)氧气、水蒸气
(2)氯化钠或
(3)
(4)放热;铁生锈放出的热量小于热量的散失
(5)铁生锈消耗氧气,使得三颈瓶内压强变小,注射器中的稀盐酸被吸入三颈瓶内与铁接触发生反应产生氢气,使瓶内压强迅速变大
(6)解:生成气体的质量为0.2L×0.09g/L=0.018g,设固体中铁的质量为x,
x=0.504g
则该固体中铁的质量分数为:
答:该固体中铁的质量分数为84%。
(7)bd或db
(8)分别将铁放入不同浓度氧气的试管中,并且试管中有等量的水,若观察到氧气浓度较高的试管中铁生锈严重,则说明氧气浓度越高,铁生锈越快
解析:
A物质的构成
B化学安全
①氯化钠由氯化钠分子直接构成
②和的分子构成不同
①进入久未开启的菜窖前,做灯火实验
②房屋失火,用水灭火是为了降低可燃物的着火点
C化学之最
D数字含义
①海水中含量最多的元素是氧元素
②人类利用最早的金属是铜
①:1个亚铁离子带3个单位正电荷
②:二氧化氮中含有2个氧原子
选项
实验目的
实验方法
A
除去固体中的
加入少量二氧化锰,并加热至质量不变
B
鉴别黄金和假黄金(铜锌合金)
用灼烧的方法
C
分离和的固体混合物
溶解、过滤、洗涤、干燥、蒸发结晶
D
验证铁比银的金属活动性强
将铁丝插入溶液中
时间(min)
1
2
3
4
5
体积(mL)
200
362
442
482
484
试管编号
A
B
C
D
一周后铁钉表面现象
有一层铁锈
无明显变化
无明显变化
有较厚铁锈
2022-2023学年江苏省泰州市靖江市九年级上学期化学期中试题及答案: 这是一份2022-2023学年江苏省泰州市靖江市九年级上学期化学期中试题及答案,共16页。试卷主要包含了 下列物质中,属于纯净物的是, 下列物质中由离子构成的是, 学习化学需要进行化学实验, 阅读下面短文,完成下列小题, 下列归纳和说法完全正确的是等内容,欢迎下载使用。
江苏省泰州市靖江市实验学校2023-2024学年九上化学期末教学质量检测模拟试题含答案: 这是一份江苏省泰州市靖江市实验学校2023-2024学年九上化学期末教学质量检测模拟试题含答案,共7页。试卷主要包含了答题时请按要求用笔,下列化学用语书写正确的是,下列实验方案可行的是等内容,欢迎下载使用。
江苏省泰州市靖江市靖城中学校际联盟2023-2024学年九年级上学期第一次学情调查化学试卷(月考): 这是一份江苏省泰州市靖江市靖城中学校际联盟2023-2024学年九年级上学期第一次学情调查化学试卷(月考),文件包含试卷docx、试卷pdf、答案卷docx、答案docx等4份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。












