

重庆市南岸区2023年九年级上学期期末化学试卷附答案
展开1.下列物质属于纯净物的是
A.空气B.矿泉水C.液氮D.可燃冰
2.冰雪埋忠骨,历史有温度。电影《长津湖》场景中所示变化属于化学变化的是
A.金色晨光中的长城B.零下40℃呼气结冰
C.用手榴弹炸坦克D.铅笔书写绝笔信
3.在劳动实践和化学实验中要保证安全,下列做法安全的是( )
A.用天然气填充玩具气球
B.用手拿润湿的玻璃管插入橡胶管
C.向燃着的酒精灯里添加酒精
D.在加油站、加气站等处打电话
4.下列实验基本操作,正确的是
A.取用NaClB.称取NaCl
C.量取水D.溶解NaCl
5.2022年6月5日世界环境日,我国的主题是“共建清洁美丽世界”。下列做法不符合这一主题的是
A.不使用一次性餐具B.使用新能源公交车
C.生活污水直接排放D.积极参与植树造林
6.下列实验现象的描述,错误的是( )
A.将铁丝伸入盛有氧气的集气瓶中,火星四射,生成黑色固体
B.拉瓦锡在密闭容器中将汞连续加热12天,部分银白色的液态汞变成了红色粉末
C.木炭在氧气中燃烧发出白光、放热,产生使澄清石灰水变浑浊气体
D.在盛有浑浊河水的烧杯中加入明矾,搅拌静置后有难溶物沉降
7.下列关于使用打火机(充入的液态物质是丁烷)的说法,正确的是
A.打火机不使用时,丁烷分子停止运动
B.按下开关释放液态丁烷,丁烷分子的体积变大
C.电火花引燃丁烷时,使丁烷的着火点升高
D.松开开关火焰熄灭,是因为断绝了丁烷的来源
8.建立模型是学习化学的重要方法,下列模型正确的是( )
A. 原子结构模型
B. 物质分类模型
C. 燃烧条件模型
D. 空气组成模型
9.宏观辨识与微观探析是化学核心素养之一。下列宏观事实的微观解释错误的是( )
A.5mLH2O和5mL酒精混合后体积小于10mL﹣﹣水分子和酒精分子间有间隔
B.金刚石和石墨的物理性质明显不同﹣﹣构成它们的原子排列方式不同
C.钠原子(Na)和钠离子(Na+)的化学性质不同﹣﹣它们的原子核内质子数不同
D.化学反应前后质量不变﹣﹣反应前后原子种类和数目没有改变
10.新鲜大蒜中含有蒜氨酸(C6H10S2O),蒜氨酸受撞击后,转化为大蒜素。大蒜素(C6H11NSO3)有较强的抗菌作用,易挥发,遇热或碱立即失去抗菌活性。下列有关说法正确的是( )
A.拍碎过程中仅发生物理变化B.煮熟食用比生食抗菌效果更好
C.两者组成元素种类相同D.两者碳元素的质量分数不同
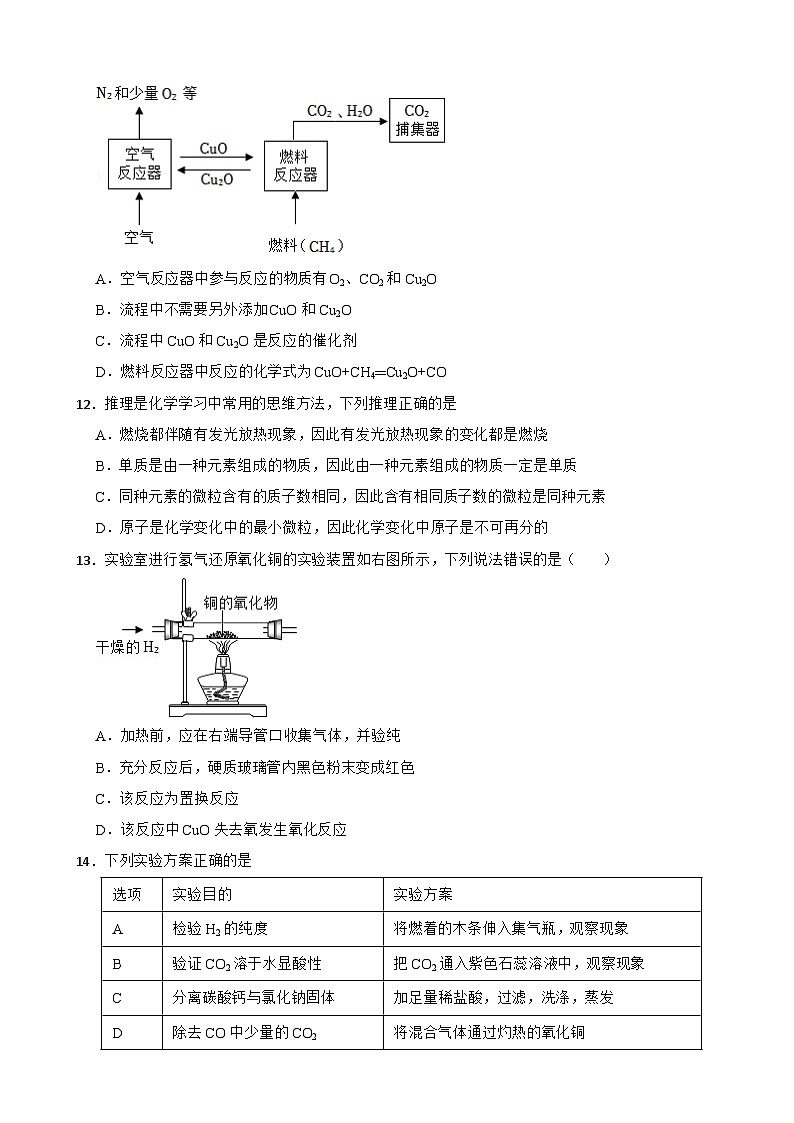
11.一种以甲烷为燃料、含铜氧化物为载氧体的化学链燃烧反应原理如下(流程中各反应物、生成物均已标出)。下列说法正确的是( )
A.空气反应器中参与反应的物质有O2、CO2和Cu2O
B.流程中不需要另外添加CuO和Cu2O
C.流程中CuO和Cu2O是反应的催化剂
D.燃料反应器中反应的化学式为CuO+CH4═Cu2O+CO
12.推理是化学学习中常用的思维方法,下列推理正确的是
A.燃烧都伴随有发光放热现象,因此有发光放热现象的变化都是燃烧
B.单质是由一种元素组成的物质,因此由一种元素组成的物质一定是单质
C.同种元素的微粒含有的质子数相同,因此含有相同质子数的微粒是同种元素
D.原子是化学变化中的最小微粒,因此化学变化中原子是不可再分的
13.实验室进行氢气还原氧化铜的实验装置如右图所示,下列说法错误的是( )
A.加热前,应在右端导管口收集气体,并验纯
B.充分反应后,硬质玻璃管内黑色粉末变成红色
C.该反应为置换反应
D.该反应中CuO失去氧发生氧化反应
14.下列实验方案正确的是
A.AB.BC.CD.D
15.下列关于氯酸钾受热分解的图像中,纵坐标的化学意义错误的是
A. 固体混合物中钾元素的质量分数
B. 固体混合物中钾元素和氯元素的质量比
C. 反应过程中生成O2的质量
D. 固体混合物中氧元素的质量分数
16.在密闭容器中加入甲、乙、丙、丁四种物质进行反应,测得反应中各物质的质量如表:下列说法正确的是( )
A.丙一定是该反应的催化剂
B.该反应为分解反应
C.充分反应后,甲和乙的质量之和应等于丁的质量
D.如果有2g甲完全反应,可生成2.5g丁
二、填空题:(本题共6个小题,共39分)
17.我国成功研发氮化镓(GaN)晶体技术,使“5G”建设全球领先。
(1)画出氮原子的结构示意图 。
(2)镓元素在元素周期表中的部分信息如图所示,镓的相对原子质量为 ,该元素属于 (填“金属”或“非金属”)元素。
(3)GaN中Ga元素的化合价为 ;在高温下,Ga与NH3反应生成GaN晶体和H2,写出该反应的化学方程式 。
18.我国科技力量日益强大,航天事业迅速发展。
(1)火箭推进剂发生的化学反应是偏二甲肼(化学式C2H8N2)与四氧化二氮(化学式N2O4)反应生成二氧化碳、氮气和水,写出反应的化学方程式 。
(2)载人航天器中“氧再生系统”的物质转化如右图所示:排出舱外的物质是 (用化学式填空),处理掉1个CO2分子,需要 个H2O分子。
(3)太空教师王亚平将泡腾片(主要成分是Na2CO3)和柠檬酸(C6H8O7),塞入蓝色水球,产生很多小气泡,说明有 (填化学式)生成,还闻到阵阵香气,说明分子具有 的性质。
19.水是万物之源、生命之本。
(1)自来水厂的净水流程为:取水→沉降→过滤→活性炭净水→含氯物质消毒杀菌,流程中体现了活性炭的 性。
(2)水的硬度过大,对健康有害,生活居家常用 方法降低水的硬度。
(3)实验室电解水的装置如右图所示:写出电解水的化学方程式 ,a管中产生的气体和b管中产生的气体的质量比约为 。
(4)1785年,拉瓦锡将水蒸气通过红热的铁制枪管产生“易燃空气”,同时生成Fe3O4,上述反应的化学方程式为 。
20.我国科学家已实现由CO2到淀粉的全人工合成,主要过程如图1:
(1)自然界中,绿色植物实现CO2到葡萄糖的转化过程称为 。
(2)阶段I反应的微观过程如图2所示。写出甲醇的化学式: 。
(3)阶段Ⅱ是用H2O2将甲醇氧化为甲醛(HCHO),同时生成H2O,写出反应的化学方程式 。
(4)如果在CO2全人工合成淀粉的流程中,碳元素的转化率为60%,则26.4kgCO2可合成 kg淀粉【化学式为(C6H10O5)n】。
21.人类文明的进步离不开对火的探索与利用。
(1)化石燃料是当今人类获得能量的主要来源,其中有石油、 和天然气,化石燃料都属于 (“可再生”或“不可再生”)资源。
(2)某化学兴趣小组设计了如图1所示实验来探究燃烧的条件:白磷1燃烧而白磷2不燃烧,说明燃烧需要 ,白磷1燃烧而红磷不燃烧,说明燃烧需要 ,气球的作用是 。
(3)家用燃气热水器的工作原理如图2所示:若空气进气孔被部分堵塞,导致天然气燃烧不充分,会产生的有毒气体是 。
(4)某阻燃剂主要成分为碱式碳酸镁【Mga(OH)2(CO3)b】,它吸热分解生成MgO、H2O、CO2三种氧化物,请说出阻燃剂能够阻燃的原因 (只要说出一点即可)。
22.CO2的吸收是碳封存的首要环节:
(1)膜吸收法中,3种吸收剂(一乙醇胺、二乙醇胺、氨基乙酸钾)对烟气中CO2的脱除效果(如图1所示);当吸收剂相同时,随烟气流速增大,CO2脱除效果 (填“增强”或“减弱”);当烟气流速相同时,CO2脱除效果最好的是 。
(2)捕捉烟气中的CO2流程如图2:
①写出“捕捉室”中反应的化学方程式为 。
②根据流程分析“颗粒反应室”中的两种生成物是 。
③上述流程中可循环使用的物质有 (填化学式)。
三、实验题(本题共2个小题,共19分)
23.请结合如图实验装置,回答下列问题:
(1)写出仪器①的名称: 。
(2)加热高锰酸钾制取并收集一瓶较纯净的氧气,应选用的装置组合是 (填字母序号),并写出该反应的化学方程式 。
(3)写出用锌粒和稀硫酸反应制H2的化学方程式 ,实验室常用装置B来制备H2,其优点是 。
(4)写出实验室制CO2的化学方程式 ,用装置C制CO2的优点是 。
24.兴趣小组同学在老师的带领下,探究金属氧化物的催化作用:
(1)常温下,写出MnO2催化过氧化氢溶液分解的化学方程式: ,在反应前后MnO2的 和 都没有改变。
(2)小明类比推测:CuO、Fe2O3也可以催化H2O2分解。用如图所示装置进行三次实验:在锥形瓶中分别加入0.5gCuO、0.5 g Fe2O3和不加物质,然后均加入6mL5%过氧化氢溶液,测定均收集到50mLO2的实验时间依次是108.5秒、87秒、496秒。注射器的作用是 ,得出的结论是 。
(3)根据以上实验,小刚大胆猜想:CuO、Fe2O3对加热氯酸钾制氧气也有催化作用,并进行实验,数据如下表:通过上述对比实验,a= ,三种催化剂的催化能力由强到弱的顺序是 ,实验1的作用是: 。
四、计算题:(本题共2个小题,共10分)
25.某品牌的电热蚊香液的驱虫剂为氯氟醚菊酯,化学式为C17H16Cl2F4O3。
(1)计算各元素的质量比:C%:H%:O%:F%:Cl%= 。
(2)计算碳元素的质量分数: 。
26.2022年1﹣9月重庆火力发电量为729.3亿千瓦时,占全市发电总量的75.63%,发电用煤约1960万吨,煤中质量分数为0.7%的硫元素会燃烧产生SO2。火力发电厂在煤中加入石灰石粉末,除去燃烧时生成的SO2,同时生成CaSO4(用于生产石膏)。其中涉及的化学反应如下:SO2+CaCO3CaSO3+CO2,2CaSO3+O2=2CaSO4。
(1)计算1960万吨煤中硫元素的质量;
(2)计算燃烧1960万吨煤可生成CaSO4的质量。
1.B
2.C
3.B
4.C
5.C
6.A
7.D
8.D
9.C
10.D
11.B
12.D
13.D
14.C
15.C
16.D
17.(1)
(2)69.72;金属
(3)+3价;2Ga+2NH32GaN+3H2
18.(1)C2H8N2+2N2O42CO2+2N2+4H2O
(2)CH4;2
(3)CO2;不断运动
19.(1)吸附
(2)煮沸
(3)2H2O2H2↑+O2↑;8:1
(4)3Fe+4H2OFe3O4+4H2
20.(1)光合作用
(2)CH3OH
(3)CH3OH+H2O2=HCHO+2H2O
(4)9.72
21.(1)煤;不可再生
(2)氧气;温度达到着火点;吸收五氧化二磷,防止污染空气
(3)一氧化碳
(4)降低可燃物的温度到着火点以下
22.(1)减弱;氨基乙酸钾
(2)2NaOH+CO2=Na2CO3+H2O;碳酸钙、氢氧化钠;NaOH、CaO
23.(1)长颈漏斗
(2)AE;2KMnO4K2MnO4+MnO2+O2↑
(3)Zn+H2SO4═ZnSO4+H2↑;可以控制反应的速率
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑;可以控制反应的发生和停止
24.(1)2H2O22H2O+O2↑;质量;化学性质
(2)平衡气压;CuO、Fe2O3可以催化H2O2分解
(3)0.5;Fe2O3>MnO2>CuO;对比实验
25.(1)204:16:48:76:71
(2)49.2%
26.(1)解:硫元素的质量为:1960t×0.7%=13.72t;
答:1960万吨煤中硫元素的质量为13.72t
(2)解:S+O2SO2,SO2+CaCO3CaSO3+CO2,2CaSO3+O2=2CaSO4。
设可生成CaSO4的质量为x。
由化学方程式可知
=
x=58.31万吨
答:燃烧1960万吨煤可生成CaSO4的质量为:58.31万吨。选项
实验目的
实验方案
A
检验H2的纯度
将燃着的木条伸入集气瓶,观察现象
B
验证CO2溶于水显酸性
把CO2通入紫色石蕊溶液中,观察现象
C
分离碳酸钙与氯化钠固体
加足量稀盐酸,过滤,洗涤,蒸发
D
除去CO中少量的CO2
将混合气体通过灼热的氧化铜
甲
乙
丙
丁
加入
6.5g
2g
1.5g
0.5g
一段时间后
2.5g
1g
1.5g
5.5g
实验
KClO3质量(克)
物质
产生O2质量(mL)
耗时(秒)
化学式
质量(克)
1
1.5
﹣
﹣
100mL
480
2
1.5
MnO2
0.5
300mL
76.5
3
1.5
CuO
a
300mL
128.5
4
1.5
Fe2O3
0.5
300mL
68.7
S
~
CaSO4
32
136
13.72t
x
重庆市南岸区南开(融侨)中学2023-2024学年九年级化学第一学期期末教学质量检测模拟试题含答案: 这是一份重庆市南岸区南开(融侨)中学2023-2024学年九年级化学第一学期期末教学质量检测模拟试题含答案,共9页。试卷主要包含了下列实验操作正确的是,下列有关水的说法错误的是,下列做法可以达到目的的是,下列有关化学史的说法不正确的是等内容,欢迎下载使用。
重庆市2023年九年级上学期期末化学试题附答案: 这是一份重庆市2023年九年级上学期期末化学试题附答案,共8页。试卷主要包含了单选题,填空题,综合题,计算题等内容,欢迎下载使用。
2023年重庆市南岸区中考一模化学试题(无答案): 这是一份2023年重庆市南岸区中考一模化学试题(无答案),共9页。试卷主要包含了单选题,未知等内容,欢迎下载使用。












