





人教版 (2019)必修 第一册第一节 原子结构与元素周期表教学ppt课件
展开2.阅读元素周期表的发展;
1.结合原子结构示意图,归纳出元素周期表的编排原则及结构,根据原子序数确定元素在周期表中的位置;
4.通过事实,了解核素的含义及符号,了解元素、核素、同位素的内含与外延。
3.熟悉 中各微粒数间的关系,比较元素、核素、同位素异同;
1.元素是指原子核内___________________相同的一类原子的总称。2.原子一般由_______、_______和___________构成,其中_______数等于___________数。3.碳原子、氯原子中的质子数分别为____、_____,Na+、Cl-中的电子数分别为_____、_____。4.金刚石和石墨、O2和O3互为_____________。
1869年以前,科学家已经陆续发现了63种元素,这些元素之间似乎没有任何联系,好像互不相干。俄国科学家门捷列夫(Dmitry Ivanvich Mendeleev,1834~1907)在前人工作的基础上,对元素及其性质进行了系统的研究,他将当时已知的63种元素依据相对原子质量大小规律进行排列,制成的表格成为现代元素周期表的雏形。利用周期表,门捷列夫成功预测了当时尚未发现的元素(镓、钪、锗)。
1913年英国科学家莫色勒利用阴极射线撞击金属产生X射线,发现原子序数越大,X射线的频率就越高,因此他认为原子核的正电荷数决定了元素的化学性质,并把元素依照核内正电荷数(即质子数)排列,经过多年修订后才成为当代的元素周期表。随着人们对元素地进一步认识,元素周期表得到了完善,现在元素周期表已经成为人们研究化学、研究物质的一个必备的工具。在化学学科领域中使用的元素周期表提供的信息更突出了元素的原子结构信息。让我们走进教材,充分认识元素周期表和核素。
1.元素周期表的出现与演变
1869年,俄国化学家门捷列夫首制
将元素按照相对原子质量由大到小排列,将化学性质相似的元素放在一起
揭示了化学元素间的联系
为未知元素留下的空位先后被填满
排序依据由相对原子质量改为原子的核电荷数
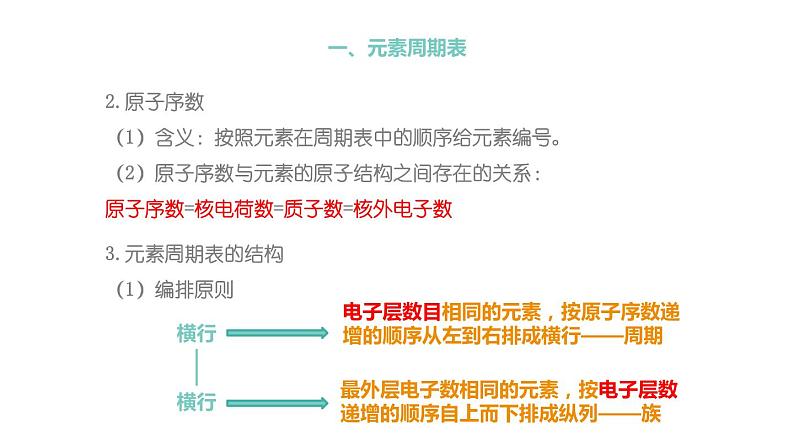
2.原子序数(1)含义:按照元素在周期表中的顺序给元素编号。(2)原子序数与元素的原子结构之间存在的关系:原子序数=核电荷数=质子数=核外电子数
3.元素周期表的结构(1)编排原则
电子层数目相同的元素,按原子序数递增的顺序从左到右排成横行——周期
最外层电子数相同的元素,按电子层数递增的顺序自上而下排成纵列——族
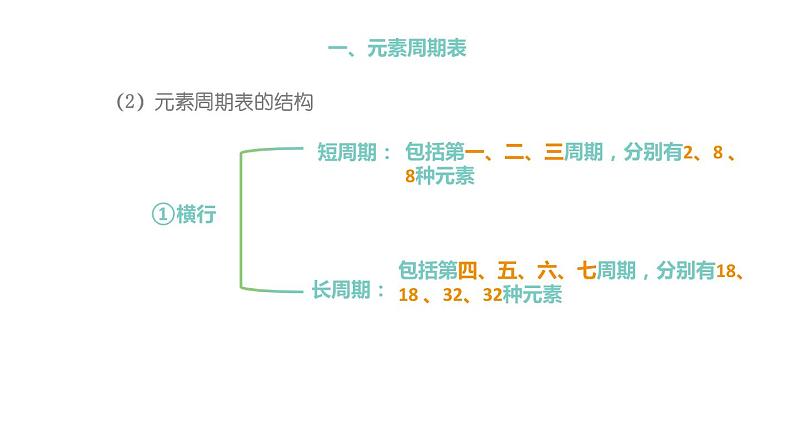
(2)元素周期表的结构
包括第一、二、三周期,分别有2、8 、8种元素
包括第四、五、六、七周期,分别有18、18 、32、32种元素
由短周期元素和长周期元素共同构成,表示在族序数后标A;包括第ⅠA族~第ⅦA族,共7个主族
完全由长周期元素构成,表示:在族序数后标B;包括第ⅢB族~第ⅡB族、第ⅠB族~第ⅡB族,共7个副族
包括第8、9、10三个纵列,位于第ⅦB和第ⅠB族之间
占据周期表的第18纵列,最外层电子数是8(He是2)
(4)常见族的别称:第ⅠA族(除氢外)——碱金属元素,ⅦA——卤族元素,0族——稀有气体元素,ⅣA、ⅤA、ⅥA族依次又叫碳族、氮族、氧族。
(5)元素周期表中方格中的符号的意义
2.核素与同位素(1)核素:把具有一定数目质子和一定数目中子的一种原子叫做核素。(2)同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。如11H、D、T互称为同位素。
(3)核素(原子)符号质量数为A、质子数为Z的核素(原子)表示为______.(4)同位素的特征①同一种元素的各种同位素的化学性质几乎完全相同;物理性质略有差异。②在天然存在的某种元素里,不论是游离态还是化合态,同位素相互之间保持一定的比率。
(5)同位素的用途①146C在考古工作中用于测定一些文物的年代。②21H、31H用于制造氢弹。③利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病等。④利用18O作为示踪原子探究有机反应机理。
注意:①11H原子中不含中子。②核素的种类由质子数、中子数共同决定。
全面熟悉元素周期表的结构与定量关系
2.第三周期和第四周期中的ⅡA、ⅢA族元素的原子序数差分别为多少?
3.Na与K、Cl与Br的原子序数差分别为多少?
4.88号元素在周期表中的位置如何?
(1)列序数与族序数的关系①列序数<8,主族和副族的族序数=列序数;②列序数=8或9或10,为第Ⅷ族;③列序数>10,主族和副族的族序数=列序数-10(0族除外)。(2)三个定量关系①周期序数=电子层数②主族序数=最外层电子数③原子序数=核电荷数=质子数=核外电子数
(3)原子序数的定量关系①同周期,ⅡA与ⅢA族原子序数差可能为1,11,25②同族,相邻周期原子序数差:ⅠA~ⅡA:上一周期元素种类数;ⅢA~0族:下一周期元素种类数。如Na与K相差8,Cl与Br相差18。
2.据原子序数确定元素位置的方法——稀有气体定位法(1)比大小定周期比较该元素的原子序数与0族元素的序数大小,找出与其相邻近的0族元素,那么该元素就和序数大的0族元素处于同一周期。
(2)求差值定族数①若某元素原子序数比相应的0族元素多1或2,则该元素应处在该0族元素所在周期的下一个周期的ⅠA族或ⅡA族。②若比相应的0族元素少1~5时,则应处在同周期的ⅦA~ⅢA族。③若差为其他数,则由相应差数找出相应的族。如84号元素的位置为与86号稀有气体氡在同一周期(第六周期),在ⅥA族。
3.理解元素、核素、同位素、同素异形体的差异(1)差别
4.记忆口诀横行叫周期,现有一至七,四长三个短,第七已排满。纵列称为族,共有十六族,一八依次现,一零再一遍。一纵一个族,Ⅷ族搞特殊,三纵算一族,占去8、9、10。镧系与锕系,蜗居不如意,十五挤着住,都属ⅢB族。
关于元素周期表,下列叙述中不正确的是 ( )A.元素周期表中共有18列,16族B.元素周期表中的族分为主族、副族、0族C.元素周期表中第3纵列为ⅢA族D.主族都是由短周期元素和长周期元素共同组成
下列叙述正确的是 ( )A.元素的原子序数越大,其族序数也越大B.同周期的第ⅡA族与第ⅢA族的原子序数一定相差1C.在元素周期表中,第14列元素所形成的化合物种类最多D.主族元素原子的最外层电子数为奇数,其族序数不一定为奇数
假设x是第ⅡB族中某元素的原子序数,那么原子序数为x+1的元素位于( )A.第ⅠB族 B.第ⅢB族C.第ⅢA族D.第ⅡA族
近20年来,稳定同位素分析法在植物生理学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。下列说法中正确的是( )A.34S原子核内的中子数为16B.16O转换成18O不是化学变化C.2H+的酸性比1H+的酸性更强D.13C和15N的质子数相差2
俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成功合成4个第115号元素的原子,中文名“镆”,读音是mò。这4个原子生成数微秒后衰变成第113号元素,中文名“鉨”,读作nǐ。请回答:(1)115号元素原子的电子层数和最外层电子数分别为________、________。(2)若115号元素的一种核素质量数为289,则该元素的质子数与中子数的差为________。(3)113号元素原子的核外电子数为________。
A元素的原子最外层电子数是a,次外层电子数是b;B元素的原子M层电子数是(a-b),L层电子数是(a+b),则A、B两元素形成化合物的化学式最可能表示为( )A.B3A2 B.BA2C.A3B2 D.AB2
据报道,放射性同位素钬16667H可有效治疗肝癌。该同位素原子核内的中子数与核外电子数之差是( )A.32 B.67 C.99 D.166
2018年9月27日,中国化学会发布IUPAC化学元素周期表(中文版)。如图是元素周期表的一部分,已知两块阴影中间的3列属于同一族。有关阴影部分的元素,下列说法正确的是( )A.都是主族元素B.都是副族元素C.有5种副族元素和2种主族元素D.有5种主族元素和2种副族元素
玉兔二号,嫦娥四号任务月球车,于2019年1月3日22时22分完成与嫦娥四号着陆器的分离,驶抵月球表面。首次实现月球背面着陆,成为中国航天事业发展的又一座里程碑。月球车一般用23894Pu作为热源材料。下列关于23894Pu的说法正确的是( )A.23894Pu与23892U互为同位素B.23894Pu与23994Pu互为同素异形体C.23894Pu与23894U具有完全相同的化学性质D.23894Pu与23994Pu具有相同的最外层电子数
高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表教学课件ppt,共36页。PPT课件主要包含了素养要求,元素周期表,典例剖析,同位素,当堂练习等内容,欢迎下载使用。
人教版 (2019)必修 第一册第一节 原子结构与元素周期表集体备课课件ppt: 这是一份人教版 (2019)必修 第一册第一节 原子结构与元素周期表集体备课课件ppt,共27页。PPT课件主要包含了电子层,“四素”的区别等内容,欢迎下载使用。
化学必修 第一册第四章 物质结构 元素周期律第一节 原子结构与元素周期表说课ppt课件: 这是一份化学必修 第一册第四章 物质结构 元素周期律第一节 原子结构与元素周期表说课ppt课件,共36页。PPT课件主要包含了▶思路一,▶思路二,周期七个横行,短周期,长周期,个主族A,个副族B,族的别称,第ⅣA族碳族元素,第ⅤA称氮族元素等内容,欢迎下载使用。













