





高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学ppt课件
展开理解气体摩尔体积的概念以及标准状况下的气体摩尔体积。
会利用公式“n=V/Vm”进行标准状况下气体摩尔体积、物质的量和气体体积之间的转化。
重点:(1)标准状况下的气体摩尔体积;(2)标准状况下的气体摩尔体积、物质的量和气体体积之间的转化。
难点:气体摩尔体积的概念
01.决定物质体积大小的因素02.气体摩尔体积03.气体摩尔体积的理解与有关计算
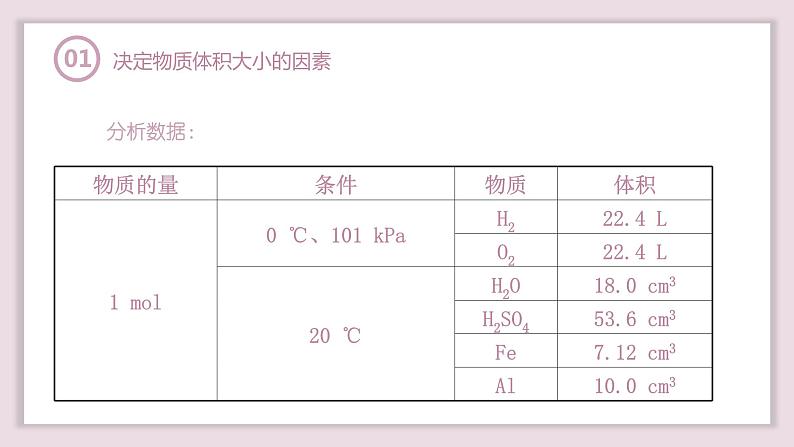
决定物质体积大小的因素
回忆一下1、我们学习了“物质的量(n)”及其单位摩尔(ml),由n可以求出哪些物理量?
2、在实验室或在生产中,对于气态物质常使用它的体积而不是质量。那么物质的量与气体体积之间有什么关系?1ml气态物质占据的体积有多大?
结论:(1)1 ml气体在相同温度和压强下,体积_____;(2)1 ml固体或液体,在相同温度下,体积_______。(3)物质体积的大小取决于构成这种物质的_________、粒子大小和粒子之间的距离三种因素。
等物质的量的固体、液体和气体体积的决定因素:
远远大于粒子本身的直径
1.气体体积规律:在相同的_____和_____下,相同体积的任何气体都含有_____数目的粒子(分子)。2.气体摩尔体积:(1)含义:单位_________的气体所占的体积叫做气体摩尔体积,符号为___。(2)表达式:__________;(3)单位:_________________和m3·ml-1(或m3/ml)。
L·ml-1(或L/ml)
结论:(1)气体摩尔体积的影响因素:温度越高,Vm越___,压强越大,Vm越___。(2)标准状况(__ ℃,101 kPa)下的气体摩尔体积:Vm=____________。
概念理解(1)在相同条件下,1 ml任何物质的体积均相同?
不对,在相同条件下,1 ml不同的固体和液体物质体积不同。
(2)同温同压下,1 ml气体的体积均为22.4 L?
不对,在标准状况下,1 ml任何气体的体积约为22.4 L。
(3)标准状况下,1 ml任何物质的体积都约为22.4 L?
不对,在标准状况下,1 ml任何气体物质的体积约为22.4 L。
(4)同温同压下,相同体积的任何气体都含有相同数目的原子?
不对,同温同压下,相同体积的任何气体都含有相同数目的分子,不同分子所含原子可能不同。
(5)同温同压下,相同体积的物质含有相同数目的分子?
不对,阿伏加德罗定律只适用于气体物质,对液体、固体物质不适用。
教材中描述“气体摩尔体积的数值不是固定不变的,它取决于气体所处的温度和压强。”请思考只有在标准状况下,气体摩尔体积的数值才为22.4 L·ml-1吗?举例说明。
不一定。在很多状况下气体摩尔体积的数值为22.4 L·ml-1,如273 ℃、202 kPa下。
排球的充气量经常影响球员的手感。用打气筒给气量不足的排球打气时,气体源源不断被打进去,而排球的体积却不发生很大变化。气体体积与什么因素有关?两种气体体积相同,含有的气体分子数一定相同吗?
影响气体体积大小的主要因素是气体分子之间的距离,给排球打气时,排球的体积不发生很大变化是因为气体分子之间的距离在不断缩小。两种气体体积相同,含有的气体分子数不一定相同,因为气体的体积还受温度和压强的影响。
气体摩尔体积的理解与有关计算
随着人们生活水平的提高,家用轿车已成为常用的交通工具。汽车尾气的排放会给环境带来一定的影响,汽车尾气中含有CO、NO、NO2等有毒气体,因此汽车尾气是否达标是衡量汽车性能的重要指标之一。
(1)标准状况下,1000L汽车尾气的物质的量约为多少?实际情况排出1000L汽车尾气的物质的量也是这些吗?
(2)与5.6gCO中氧原子个数相等的CO2气体在标准状况下的体积是多少?
(3)在汽车排气管中安装催化剂转换器,可将CO、NO转化为N2、 催化剂CO2,反应的化学方程式为2NO+2CO=====N2+2CO2。反应产物中N2和CO2的质量之比是多少?相同条件下的体积之比为多少?
1.标准状况下的气体摩尔体积: (1)1个条件:必须为标准状况。非标准状况下,1ml气体的体积不一定是22.4L。因此在使用气体摩尔体积时,一定要看清气体所处的状态。(2)1种状态:必须为气体。如水、酒精、CCl4等物质在标准状况下不是气体。(3)2个数据:“1 ml”“约22.4L”。
2.气体摩尔体积的适用范围:气体摩尔体积的适用范围是气体,可以是单一气体,也可以是混合气体,如0.2mlH2与0.8mlO2的混合气体在标准状况下的体积约为22.4L。需要注意的是混合气体中气体之间不能发生化学反应。3.气体摩尔体积的计算:
下列说法中正确的是( )A.1mlO2和1mlN2所占的体积约为22.4LB.标准状况下,H2的气体摩尔体积约为22.4LC.在标准状况下,1mlH2和1mlH2O所占的体积都约为22.4LD.在标准状况下,22.4L由N2、N2O组成的混合气体中所含有的N原子的物质的量约为2ml
【解析】选D。气体体积受温度、压强影响,A项未指明温度、压强;B项气体摩尔体积单位为L•ml-1;C项标准状况下,水为非气态,不适用于气体摩尔体积;标准状况下,22.4L混合气体中分子总数为NA,N2和N2O每个分子都含有两个N,则混合气体中所含有的N原子的数目为2NA,物质的量为2ml,D正确。
在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为______ml,其中CO2为_______ml,CO占总体积的__________,混合气体的摩尔质量为_______________________。
某同学在元旦晚会上表演的化学节目为猜气球——他先在实验室中用等质量的CH4、CO2、O2、SO2分别吹出四个气球,然后在晚会的现场让同学猜测气球是用哪种气体吹起的。
探究阿伏加德罗定律及其推论(1)等质量的CH4、CO2、O2、SO2的物质的量大小顺序如何?含有的分子数大小顺序如何?同种状况下的体积最小的是哪种气体?
CH4>O2>CO2>SO2 CH4>O2>CO2>SO2 SO2。由n=m/M知,等质量的物质摩尔质量越大,物质的量越小,含有的分子数越少,在同种状况下的体积越小。
(2)上述气球A、B、C、D依次相应吹入的气体是什么?为什么?
SO2、CO2、O2、CH4,在相同的温度和压强下,SO2、CO2、O2、CH4的物质的量SO2<CO2<O2<CH4,故体积SO2<CO2<O2<CH4。
(3)分析上述气球中气体的密度最大的是哪一种气体?由此可以得出什么结论?
上述气体质量相等,但充入SO2的气球的体积最小,故密度最大。由此得出,在相同的温度和压强下,气体的密度之比等于气体的摩尔质量之比(或相对分子质量之比)。
(4)若上述气球中通入等物质的量的四种气体,气球的体积如何?
相等。在相同的温度和压强下,气体的物质的量相等,气体的体积相等。
总结1.阿伏加德罗定律:(1)内容:同温同压下,相同体积的任何气体都含有相同数目的粒子。(2)适用范围:阿伏加德罗定律及其推论适用于气体,可以是单一气体,也可以是混合气体,对固体和液体不适用。(3)“三同定一同”规律:同温、同压、同体积、同分子数中只要有“三同”,则必有“第四同”。
2.阿伏加德罗定律的推论:
高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学ppt课件,共14页。PPT课件主要包含了数目不同,粒子大小不同,粒子间距离不同,a粒子的数目,b粒子的大小,c粒子间的距离,固体物质,液体物质,粒子间距离都很小,气体物质等内容,欢迎下载使用。
人教版 (2019)必修 第一册第三节 物质的量背景图ppt课件: 这是一份人教版 (2019)必修 第一册第三节 物质的量背景图ppt课件,共24页。PPT课件主要包含了÷NA,×NA,÷Vm,×Vm等内容,欢迎下载使用。
化学必修 第一册第三节 物质的量评课ppt课件: 这是一份化学必修 第一册第三节 物质的量评课ppt课件,共21页。PPT课件主要包含了粒子的数目,粒子的大小即直径,粒子间的距离,气体摩尔体积,阿伏加德罗定律,课堂练习等内容,欢迎下载使用。














