

2022年高中化学必修二同步检测:第六章 化学反应与能量 Word版含答案
展开
这是一份2022年高中化学必修二同步检测:第六章 化学反应与能量 Word版含答案,共5页。
化学反应与能量单元复习 一.选择题(每题7分,共70分)1.下列关于能源和作为能源的物质的叙述中错误的是 ( )A.化石能源物质内部蕴储着大量的能量B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来C.物质的化学能可以在不同条件下转化为热能、电能,为人类所利用D.吸热反应没有利用价值,放热反应在发生时都不需要加热2.等质量的固体硫和硫蒸气分别在相同条件下完全燃烧,放出的热量 ( )A.前者多 B.后者多 C.二者相等 D.无法比较3.下列说法正确的是( )A.化学电池的放电过程就是电能转换为化学能的过程B.化学电池中电子由正极流出,经外电路流向负极C.物质燃烧总是放热的,燃料电池两极板均发生氧化还原反应D.燃料电池工作时,通常是将空气通向正极4.科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机酸转化为氢气,氢气进入以磷酸为电解质的燃料电池发电。电池的负极反应为( )A.H2-2e-+2OH-=2H2O B.O2+4e-+4H+=2H2OC.H2-2e-=2H+ D.O2+4e-+2H2O=4OH-5.已知中和热数值是57.3KJ/mol。下列反应物混合时,产生的热量等于57.3KJ的是( )A.1mol/L稀HCl(aq)和1mol/L稀NaOH(aq) B.500mL2.0mol/L的HCl(aq)和500mL2.0mol/L的NaOH(aq)C.500mL2.0mol/L的CH3COOH(aq)和500mL2.0mol/L的NaOH(aq)D.1mol/L稀CH3COOH(aq)和1mol/L稀NaOH(aq)6.最近,科学家用巨型计算机进行模拟化确认,由60个N原子可结合成N60分子,N60变成N2时放出巨大能量,下列说法中不正确的是( )A.N60与N2都是氮的同素异形体 B.1个N60分子中含60个N原子C.N60 的相对分子质量为840,属高分子化合物D.N60 变成N2的反应是放热反应,说明N2比N60更稳定7.对于密闭容器中进行的反应:C+O2 = CO2,下列叙述中错误的是 ( )A.将炭块磨成粉末可以加快反应速率 B.升高温度可以加快反应速率C.增大压强可以加快反应速率 D.恒容下充入N2可以加快反应速率8.在一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到反应限度的标志是 ( )A.容器内的总压强不随时间变化 B.单位时间内生成2n molAB的同时生成n molB2C.c(A2):(B2):c(AB)=1:1:2 D.A2和B2的物质的量之和与AB的物质的量相等9.某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+能实现该反应的原电池是( )A.正极为Cu,负极为Fe,电解质溶液为FeCl3B.正极为C,负极是Fe,电解质溶液为FeCl2C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3D.正极为Ag,负极为Fe,电解质溶液为CuSO410.下列关于化学反应限度的说法正确的是( )A.一个可逆反应达到的平衡状态,就是这个反应在这个条件下所能达到的限度B.当一个可逆反应达到平衡状态时,其正向反应速率和逆向反应速率相等,且等于零C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变D.化学反应的限度不可以通过改变条件而改变二.填空题(每题10分,共30分)11.键能是指在25℃、1.01×105Pa,将1mol理想气体分子AB拆开为中性气体原子A和B时所需要的能量。显然键能越大,化学键越牢固,含该键的分子越稳定。如H-H的键能是436KJ·mol-1,是指使1molH2分子变成2molH原子需要吸收436KJ的能量。(1)已知H-Cl键的键能为431KJ·mol-1,下列说法正确的是 A.每生成1molH-Cl键放出431KJ能量 B.每生成1molH-Cl键吸收431KJ能量C.每拆开1molH-Cl键放出431KJ能量 D.每拆开1molH-Cl键吸收431KJ能量 (2)已知键能:H-H为436KJ·mol-1;H-F为565KJ·mol-1;H-Cl为431KJ·mol-1;H-Br为366KJ·mol-1。则下列分子受热时最稳定的是 A.HF B.HCl C.HBr D.H2(3)能用键能大小解释的是 A.氮气的化学性质比氧气稳定 B.常温常压下溴呈液态,碘呈固态.C.稀有气体一般很难发生化学反应 D.硝酸易挥发而硫酸难挥发 SO2O2SO3反应开始时的浓度(mol·L-1)3.01.5010min后的浓度(mol·L-1) 平均反应速率 (mol·L-1·min-1) 0.112.工业制硫酸中,SO2的催化氧化是一个可逆反应:2SO2+O2
2AB(g)达到反应限度的标志是 ( )A.容器内的总压强不随时间变化 B.单位时间内生成2n molAB的同时生成n molB2C.c(A2):(B2):c(AB)=1:1:2 D.A2和B2的物质的量之和与AB的物质的量相等9.某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+能实现该反应的原电池是( )A.正极为Cu,负极为Fe,电解质溶液为FeCl3B.正极为C,负极是Fe,电解质溶液为FeCl2C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3D.正极为Ag,负极为Fe,电解质溶液为CuSO410.下列关于化学反应限度的说法正确的是( )A.一个可逆反应达到的平衡状态,就是这个反应在这个条件下所能达到的限度B.当一个可逆反应达到平衡状态时,其正向反应速率和逆向反应速率相等,且等于零C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变D.化学反应的限度不可以通过改变条件而改变二.填空题(每题10分,共30分)11.键能是指在25℃、1.01×105Pa,将1mol理想气体分子AB拆开为中性气体原子A和B时所需要的能量。显然键能越大,化学键越牢固,含该键的分子越稳定。如H-H的键能是436KJ·mol-1,是指使1molH2分子变成2molH原子需要吸收436KJ的能量。(1)已知H-Cl键的键能为431KJ·mol-1,下列说法正确的是 A.每生成1molH-Cl键放出431KJ能量 B.每生成1molH-Cl键吸收431KJ能量C.每拆开1molH-Cl键放出431KJ能量 D.每拆开1molH-Cl键吸收431KJ能量 (2)已知键能:H-H为436KJ·mol-1;H-F为565KJ·mol-1;H-Cl为431KJ·mol-1;H-Br为366KJ·mol-1。则下列分子受热时最稳定的是 A.HF B.HCl C.HBr D.H2(3)能用键能大小解释的是 A.氮气的化学性质比氧气稳定 B.常温常压下溴呈液态,碘呈固态.C.稀有气体一般很难发生化学反应 D.硝酸易挥发而硫酸难挥发 SO2O2SO3反应开始时的浓度(mol·L-1)3.01.5010min后的浓度(mol·L-1) 平均反应速率 (mol·L-1·min-1) 0.112.工业制硫酸中,SO2的催化氧化是一个可逆反应:2SO2+O2 ![]() 2SO3 ,设该反应在一定条件下, 10min达到一定限度,在反应物和生成物之间建立一种动态平衡(即化学平衡),填空: 13.反应A(g)+B(g)错误!未找到引用源。C(g) +D(g)过程中的能量变化如下图所示,回答下列问题。
2SO3 ,设该反应在一定条件下, 10min达到一定限度,在反应物和生成物之间建立一种动态平衡(即化学平衡),填空: 13.反应A(g)+B(g)错误!未找到引用源。C(g) +D(g)过程中的能量变化如下图所示,回答下列问题。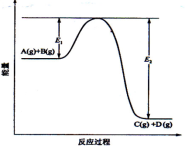 (1)该反应是_____反应(填“吸热”“放热”); (2)反应体系中加入催化剂对反应热是否有影响?_________________________,原因是______________________________________________(从能量说明)
(1)该反应是_____反应(填“吸热”“放热”); (2)反应体系中加入催化剂对反应热是否有影响?_________________________,原因是______________________________________________(从能量说明)
第二章 化学反应与能量单元复习 1、D;2、B; 3、D;4、C;5、B 6、C 7、D 8、B 9、A 10、A 11.AD;A;A 6.最近,科学家用巨型计算机进行模拟化确认,由60个N原子可结合成N60分子,N60变成N2时放出巨大能量,下列说法中不正确的是A.N60与N2都是氮的同素异形体 B.1个N60分子中含60个N原子C.N60 的相对分子质量为840,属高分子化合物D.N60 变成N2的反应是放热反应,说明N2比N60更稳定 这是高考必考内容:化学基本概念。有同素异形体、相对分子质量、高分子化合物、吸放热反应等。同素异形体是同种元素形成的性质不同的单质。高分子化合物是指由众多原子或原子团主要以共价键结合而成的相对分子质量在一万以上的化合物。答案为C12. SO2O2SO3反应开始时的浓度 10min后的浓度(mol·L-1)2.0 1.01.0 平均反应速率(mol·L-1min-1)0.10.05 13、反应A(g)+B(g)错误!未找到引用源。C(g) +D(g)过程中的能量变化如上图所示,回答下列问题。(1)该反应是_____反应(填“吸热”“放热”); (2)反应体系中加入催化剂对反应热是否有影响?_______ ________,原因是___________ 这是高考必考内容:化学反应中的能量变化。 由图可以知道,由于该反应的反应物的总能量高于生成物的总能量,所以该反应属于放热反应,所以升高温度,平衡向逆反应进行,所以A的转化率减小;当在反应体系中加入催化剂,能同倍数改变正逆反应速率,因此对化学平衡的移动无影响,即对反应热也无影响。因为化学反应速率增大,所以E1和E2同时降低。答案为(1)放热,(2)不影响;催化剂不改变平衡的移动。






