2023年高考押题预测卷02(上海卷)-化学(考试版)
展开★绝密 启用前
2023年高考押题预测卷02【上海卷】
化 学
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
一.选择题(合计20题,每题2分,共40分)
1.化学创造美好生活,下列物质用途与所述的化学知识没有关联的是
选项 | 物质用途 | 化学知识 |
A | 二氧化硫用作红酒防腐剂 | 溶于水显弱酸性 |
B | 乙炔用于金属切割与焊接 | 燃烧放出大量热 |
C | 碳酸氢钠用作面团膨松剂 | 受热分解会产生 |
D | 铁触媒用作合成氨的催化剂 | 催化剂可以提高反应速率 |
A.A B.B C.C D.D
2.已知A、B、C、D为短周期元素构成的四种物质,它们有转化关系,且D为强电解质(其他相关物质可能省略)。下列说法不正确的是
A.若A为非金属单质,C转化为D可能为氧化还原反应
B.若A为非金属单质,其所含的元素在周期表中可能处于第二周期第IVA族
C.不论A为单质还是化合物,D都有可能是同一种物质
D.若A是共价化合物,0.1 mol A分子中含有的电子数可能为NA
3.春季是流感、诺如病毒等疾病的高发期,需要对重点场所做好定期清洁消毒。下列物质中,不是消毒剂的是
A.漂粉精 B.洁厕灵 C.碘酒 D.臭氧
4.反应8NH3+3Cl2=6NH4C1+N2可用于氯气管道的检漏。下列化学用语正确的是
A.中子数为1的氢原子:
B.N2分子结构式N≡N
C.NH4Cl的电子式:
D.Cl-的结构示意图:
5.用括号内试剂及操作方法除去下列各物质中的少量杂质,不正确的是
A.二氧化碳中的氯化氢(饱和碳酸钠溶液、洗气)
B.乙酸乙酯中的乙酸(饱和碳酸钠溶液、分液)
C.溴乙烷中的乙醇(水、分液)
D.溴苯中的溴(NaOH溶液、分液)
6.在稀硫酸中加入铜粉,铜粉不溶解,再加入物质X后铜粉逐渐溶解,X可能是
A.HCl B.Fe2(SO4)3 C.K2S D.FeSO4
7.某中德联合研究小组制造了一种“水瓶”,用富勒烯(C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。下列说法正确的是
A.“水瓶”是纯净物 B.水分子空间构型是V型
C.C60是极性分子 D.富勒烯与石墨是同位素
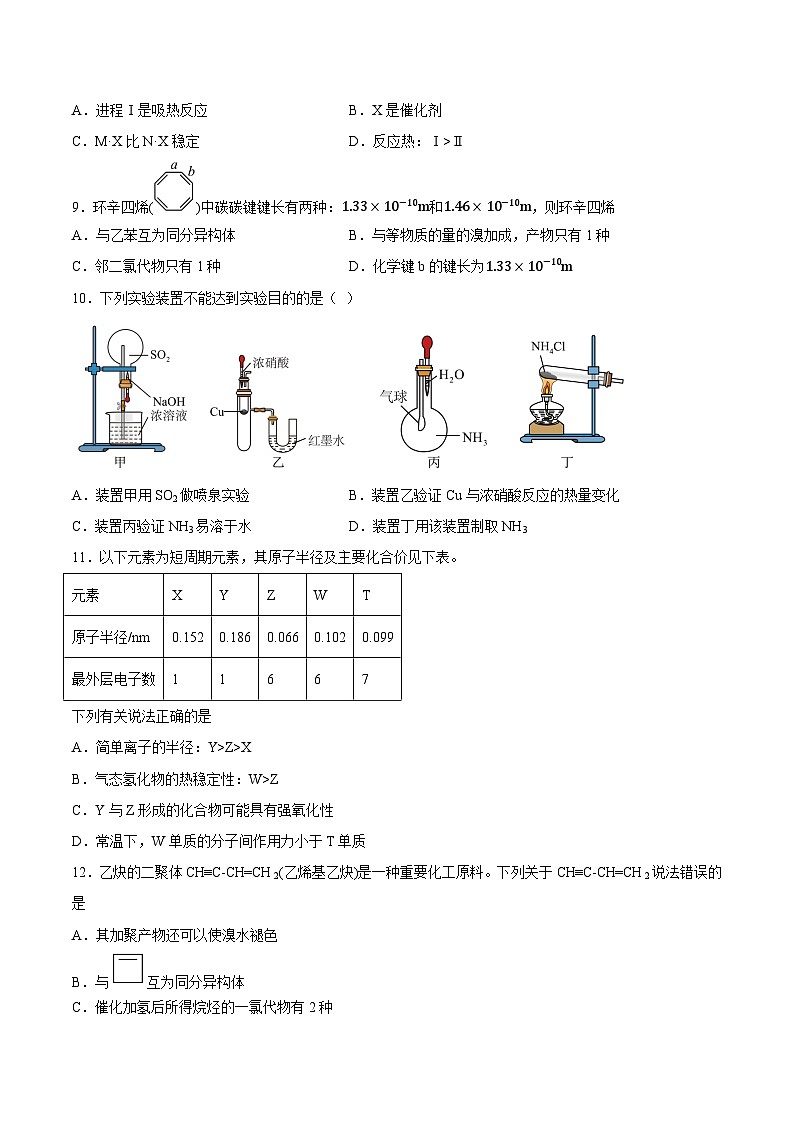
8.反应过程Ⅰ、Ⅱ都能将反应物(M)转化为产物(N)。其能量与反应进程的关系如下:
下列有关说法正确的是
A.进程Ⅰ是吸热反应 B.X是催化剂
C.M·X比N·X稳定 D.反应热:Ⅰ>Ⅱ
9.环辛四烯()中碳碳键键长有两种:和,则环辛四烯
A.与乙苯互为同分异构体 B.与等物质的量的溴加成,产物只有1种
C.邻二氯代物只有1种 D.化学键b的键长为
10.下列实验装置不能达到实验目的的是( )
A.装置甲用SO2做喷泉实验 B.装置乙验证Cu与浓硝酸反应的热量变化
C.装置丙验证NH3易溶于水 D.装置丁用该装置制取NH3
11.以下元素为短周期元素,其原子半径及主要化合价见下表。
元素 | X | Y | Z | W | T |
原子半径/nm | 0.152 | 0.186 | 0.066 | 0.102 | 0.099 |
最外层电子数 | 1 | 1 | 6 | 6 | 7 |
下列有关说法正确的是
A.简单离子的半径:Y>Z>X
B.气态氢化物的热稳定性:W>Z
C.Y与Z形成的化合物可能具有强氧化性
D.常温下,W单质的分子间作用力小于T单质
12.乙炔的二聚体CH≡C-CH=CH2(乙烯基乙炔)是一种重要化工原料。下列关于CH≡C-CH=CH2说法错误的是
A.其加聚产物还可以使溴水褪色
B.与互为同分异构体
C.催化加氢后所得烷烃的一氯代物有2种
D.完全燃烧的耗氧量与等质量乙炔耗氧量相同
13.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是
A.迷迭香酸属于芳香烃
B.迷迭香酸分子式为C17H16O8
C.迷迭香酸可以发生加成反应、水解反应和酯化反应
D.1 mol迷迭香酸最多能和9 mol氢气发生加成反应
14.以Fe3O4为原料炼铁,主要发生如下反应:
反应Ⅰ:Fe3O4(s)+CO(g) 3FeO(s)+CO2(g)+Q1(Q1<0)
反应Ⅱ:Fe3O4(s)+4CO(g) 3Fe(s)+4CO2(g)+Q2
将一定体积CO通入装有Fe3O4粉末的反应器,其它条件不变,反应达平衡,测得CO的体积分数随温度的变化关系如图所示。下列说法正确的是
A.Q2<0
B.反应温度越高,Fe3O4主要还原产物中铁元素的价态越低
C.在恒温、恒容的反应器中,当压强保持不变时,反应Ⅰ、Ⅱ均达到平衡状态
D.温度高于1040℃时,反应I的化学平衡常数K>4
15.体积均为2.0L的恒容密闭容器甲、乙、丙中,发生反应:CO2(g)+C(s) 2CO(g),起始投料量如表,在不同温度下CO平衡浓度随温度变化如下图。下列说法正确的是
容器 | n(CO2)/mol | n(C)/mol | n(CO)/mol |
甲 | 0.2 | 0.6 | 0 |
乙 | 0.4 | 0.8 | 0 |
丙 | X<0.6 | 1 | 0 |
A.曲线Ⅰ、Ⅱ、Ⅲ对应的容器分别是乙、甲、丙
B.a、b、c三点所处状态的压强大小关系:pc>pb>pa
C.1100K时,平衡时容器中混合气体的平均分子量大小关系:甲>乙>丙
D.1000K时,若起始向容器乙中加入CO、CO2、C各1mol,则v(正)>v(逆)
16.为实现碳中和,可通过电解法用制备,电解装置如图,下列说法不正确的是
A.玻碳电极为阳极,发生氧化反应
B.铂电极的电极反应:
C.制得28g时,产生32g
D.电解一段时间后,右池中溶液的pH可能不变
17.下列变化规律正确的是
A.HCl、HBr、HI热稳定性由弱到强
B.H2CO3、HClO、CH3COOH的酸性由弱到强
C.物质的量浓度相等的NaCl、MgCl2、AlCl3三种溶液的pH值由小到大
D.等物质的量的乙烷、乙烯、乙炔充分燃烧,所耗用氧气的量由多到少
18.下列条件下的化学反应,相应的离子方程式一定正确的是
A.将通入的溶液中:
B.向溶液中加入少量溶液:
C.溶液与一定量氯气反应转移的电子数为时,反应的离子方程式为
D.向溶液通入少量:
19.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法错误的是
A.洗气瓶中产生的沉淀是亚硫酸钡
B.在Z导管出来的气体中有二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.在Z导管口有红棕色气体出现
20.实验室制备乙酸丁酯,反应温度要控制在115℃~125℃之间,有关数据如下表:
物质 | 乙酸 | 1−丁醇 | 乙酸丁酯 | 98%浓硫酸 |
沸点 | 117.9℃ | 117.2℃ | 126.3℃ | 338.0℃ |
溶解性 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 微溶于水,溶于有机溶剂 | 与水混溶 |
下列叙述正确的是
A.采用加热回流装置
B.不用水浴加热的原因:乙酸丁酯的沸点高于100℃
C.分离粗品:用NaOH(aq)洗涤反应后混合物,再分液
D.粗品精制:加吸水剂分液
第II卷(非选择题)
请点击修改第II卷的文字说明
21.H2O2 (过氧化氢) 应用领域非常广泛。
已知:2H2O2(l) 2H2O(l)+O2(g)+Q(Q>0)
H2O2(aq) H+(aq)+HO(aq) ,K(25oC)=2.24×10-12
完成下列填空:
(1)氧原子最外层成对电子和未成对电子数目之比为_______。
(2)H2O2的电子式为_______。对H2O2分子结构,有以下两种推测:
要确定H2O2分子结构,需要测定H2O2分子中的_______。(选填序号)
a. H—O键长 b. O—O键长 c. H—O—O键角 d. H—O、O—O键能
(3)H2O2分解反应的平衡常数表达式K=_______。不同温度下H2O2分解反应的平衡常数K(25oC)_______K(40oC) (选填“>”“<”或“=”)。标准状况下,某5mL H2O2溶液60s内产生氧气22.4mL(溶液体积变化忽略不计)。则0~60s v(H2O2)= _______。
(4)25oC,pH(H2O2) _______pH(H2O) (选填“>”“<”或“=”)。研究表明,H2O2溶液中HO浓度越大,H2O2的分解速率越快。某温度下,经过相同时间,不同浓度H2O2分解率与pH的关系如图所示。一定浓度的H2O2,pH增大H2O2分解率增大的原因是_______。相同pH下,H2O2浓度越大H2O2分解率越低的原因是_______。
(5)蒽醌法是过氧化氢主要的生产方法。其生产过程可简单表示如下:
试从绿色化学角度评价该生产方法。_______
22.砷与氮为同主族元素,砷及其化合物可应用于农药、除草剂、杀虫剂等。完成下列填空:
(1)法庭医学常用马氏试砷法来证明是否砒霜(As2O3)中毒:把试样与锌和盐酸混合,若试样中含有砒霜,则会反应生成砷化氢、氯化锌与水,写出该反应的化学方程式_______。
(2)As2S3和SnCl2在盐酸中反应转化为As4S4(其中As为+2价)和SnCl4并放出H2S气体,该反应中氧化产物与还原产物的物质的量之比为_______。
(3)一定条件下,雄黄(As4S4)与O2生成As2O3与物质a。若该反应中1molAs4S4参加反应时,转移28 mol电子。写出物质a的化学式_______。
(4)三元弱酸亚砷酸()溶液中各种微粒的物质的量分数与pH的关系如图所示。
向亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,反应的离子方程式为_______。Na2HAsO3溶液中c(H2AsO)_______c(AsO) (填“>” “<”或“=”)。理由是_______。
(5)已知I2 + AsO+2OH-2I-+AsO+H2O。为验证该反应具有可逆性,将等物质的量浓度的碘水与Na3AsO3溶液按体积比为V1:V2的比例混合(另加入适量的碱)。当V1_______V2 (填“>”或“<”) 时,只需加入_______ (填试剂名称)就可以确定该反应具有可逆性。上述反应显示:AsO能在碱性溶液中被I2氧化成AsO,而H3AsO4又能在酸性溶液中被I-还原成H3AsO3,这表明_______。
23.用N-杂环卡其碱(NHC base)作为催化剂,可合成多环化合物。下面是一种多环化合物H的合成路线(无需考虑部分中间体的立体化学)。
已知:(-R表示烃基,其和苯环相连的碳上有氢原子)
完成下列填空:
(1)A中含氧官能团名称是______________;反应②涉及两步反应,已知第一步反应类型为加成反应,第二步的反应类型为_________。
(2)检验C中“碳碳双键”的操作是___________________________________________。
(3)E的结构简式为_____________________。
(4)化合物X是C的同分异构体,可发生银镜反应,与酸性高锰酸钾溶液反应后可以得到对苯二甲酸(),写出X的结构简式_______________________。
(5)参考上述信息,设计以甲苯和乙醛为原料,合成肉桂醛()的合成路线(其他无机试剂任选) _______________。(合成路线可表示为:)
24.PCl3是重要的化工原料。如图为实验室中制取粗PCl3产品的装置,夹持装置略去。
经查阅资料知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5,PCl3遇水会强烈水解生成H3PO3,PCl3遇O2会生成POCl3,PCl3、POCl3的熔沸点见如表。
物质 | 熔点/ oC | 沸点/ oC |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
完成下列填空:
(1)仪器D的名称是_______。装置F与G由橡胶管a相连通,a的作用是_______。
(2)实验时,检查装置气密性后,先打开K1通入CO2,再迅速加入红磷。通入CO2的作用是_______。
(3)装置D中盛有碱石灰,其作用一与B、E相似,作用二为_______。
(4)装置C中的反应需要65~70 oC,最适合的加热方式为_______加热,该方法的优点是_______。制得的PCl3粗产品中常含有POCl3、PCl5等。加入红磷加热除去PCl5后,通过_______(填实验操作名称),即可得到较纯净的PCl3。
(5)通过实验测定粗产品中PCl3的质量分数,实验步骤如下(不考虑杂质的反应):
第一步:迅速移取20.000 g PCl3粗产品,加水完全水解;
第二步:配成500mL溶液,移取25.00mL溶液置于锥形瓶中;
第三步:加入0. 500mol·L-1碘溶液20.00 mL,碘过量,H3PO3完全反应生成H3PO4,反应方程式为H3PO3+H2O+I2=H3PO4+2HI;
第四步:加入几滴淀粉溶液,用1.000 mol·L-1Na2S2O3标准溶液滴定过量的碘,反应方程式为I2+2Na2S2O3=Na2S4O6+2NaI,滴至终点时消耗Na2S2O3标准溶液12.00mL。
第二步需要的定量仪器名称为_______。根据上述数据,计算该产品中PCl3的质量分数为_______。
2023年高考押题预测卷03(上海卷)-化学(考试版): 这是一份2023年高考押题预测卷03(上海卷)-化学(考试版),共11页。
2023年高考押题预测卷02(浙江卷)-化学(考试版): 这是一份2023年高考押题预测卷02(浙江卷)-化学(考试版),共12页。
2023年高考押题预测卷02(上海卷)-化学(参考答案): 这是一份2023年高考押题预测卷02(上海卷)-化学(参考答案),共3页。试卷主要包含了 干燥管等内容,欢迎下载使用。