





- 化学反应的热效应(2)-课件 课件 0 次下载
- 化学反应的热效应(3)-课件 课件 0 次下载
- 化学能转化为电能(1)-课件 课件 0 次下载
- 化学能转化为电能(2)-课件 课件 0 次下载
- 电能转化为化学能(1)-课件 课件 0 次下载
高中化学鲁科版 (2019)选择性必修1第1章 化学反应与能量转化第1节 化学反应的热效应试讲课课件ppt
展开氯化铵与氢氧化钙的反应
当化学反应在一定的温度下进行时,反应所释放或吸收的热量称为该反应在此温度下的热效应,简称反应热。用Q表示
Q为正值:反应吸热,体系能量升高Q为负值:反应放热,体系能量降低
体系:研究对象(物质系统)环境:体系以外的其他部分
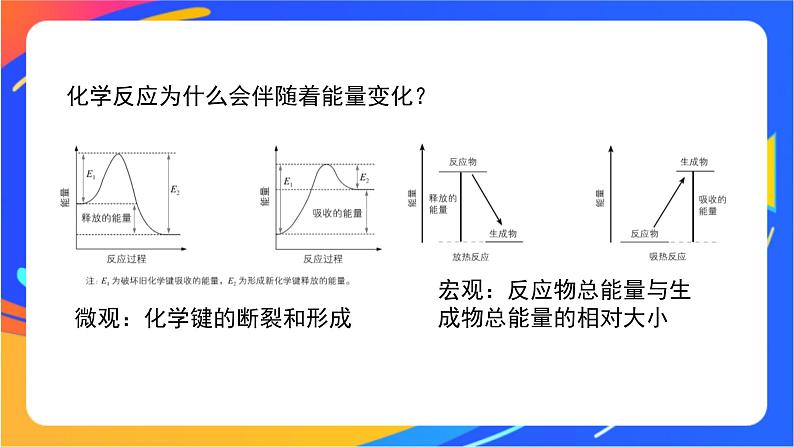
化学反应为什么会伴随着能量变化?
微观:化学键的断裂和形成
宏观:反应物总能量与生成物总能量的相对大小
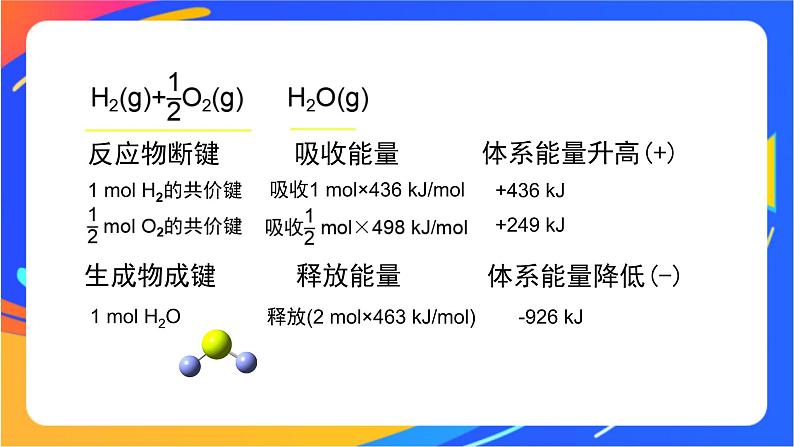
微观角度:旧化学键断裂和新化学键生成
氢氧键键能 463 kJ/ml
1 ml H2的共价键
吸收1 ml×436 kJ/ml
释放(2 ml×463 kJ/ml)
反应热= [(+436 kJ)+( + 249 kJ)] +[-(926 kJ)]
= 436 kJ+249 kJ - 926 kJ
反应热=∑反应物键能- ∑反应产物键能
宏观角度:反应物总能量与生成物总能量的相对大小
二、化学反应的内能变化与焓变
平动、转动、振动,电子运动,原子核运动等各种形式运动
内能:体系内各种微观粒子的能量总和, 包括动能和势能,符号U
微观粒子之间由于相互作用产生的能量,与距离有关。
∆U=U(反应产物)-U(反应物)
U(反应产物)>U(反应物),吸收能量
U(反应产物)
恒容反应热Q和∆U什么关系呢?
U(反应产物)>U(反应物),Q>0,吸热
U(反应产物)
用焓变描述等压反应的反应热
∆H=H(反应产物)-H(反应物)
如何测定反应的反应热呢?
测量反应前后温度的变化值
已知氮气与氢气反应生成2 ml氨气放热92.4 kJ。且H-H键键能(化学键断裂时吸收或形成时释放的能量)为436 kJ/ml,N-H键键能为391 kJ/ml,试计算N≡N键的键能是多少。
N2 + 3H2 2NH3
吸收(1 ml×a kJ/ml)
吸收(3 ml×436 kJ/ml)
反应热=∑反应物键能 - ∑反应产物键能
N2 + 3H2 2NH3
释放(6 ml×391 kJ/ml)
化学选择性必修1专题1 化学反应与能量第一单元 化学反应的热效应完整版ppt课件: 这是一份化学选择性必修1专题1 化学反应与能量第一单元 化学反应的热效应完整版ppt课件,共21页。PPT课件主要包含了思考探究·一,习题探究,作业布置等内容,欢迎下载使用。
鲁科版 (2019)选择性必修1第1章 化学反应与能量转化第1节 化学反应的热效应完美版课件ppt: 这是一份鲁科版 (2019)选择性必修1第1章 化学反应与能量转化第1节 化学反应的热效应完美版课件ppt,共32页。PPT课件主要包含了核心问题1,观察·发现规律,总结规律,思维程序,实际问题解决,摩尔燃烧焓,方法提升等内容,欢迎下载使用。
高中化学鲁科版 (2019)选择性必修1第1节 化学反应的热效应完整版课件ppt: 这是一份高中化学鲁科版 (2019)选择性必修1第1节 化学反应的热效应完整版课件ppt,共22页。PPT课件主要包含了状态需要写吗,H=U+PV,物质变化,反应焓变,物质化学计量数扩大,∆H相应扩大,交流研讨,哪种写法正确呢,放热反应等内容,欢迎下载使用。













