江苏省南通市海安市2022-2023学年九年级上学期期末化学试题
展开2022~2023学年第一学期末质量监测试卷
九年级 化学
可能用到的相对原子质量:H-1;C-12;O-16;Co-59
选择题(每题2分;每题只有一个正确选项)
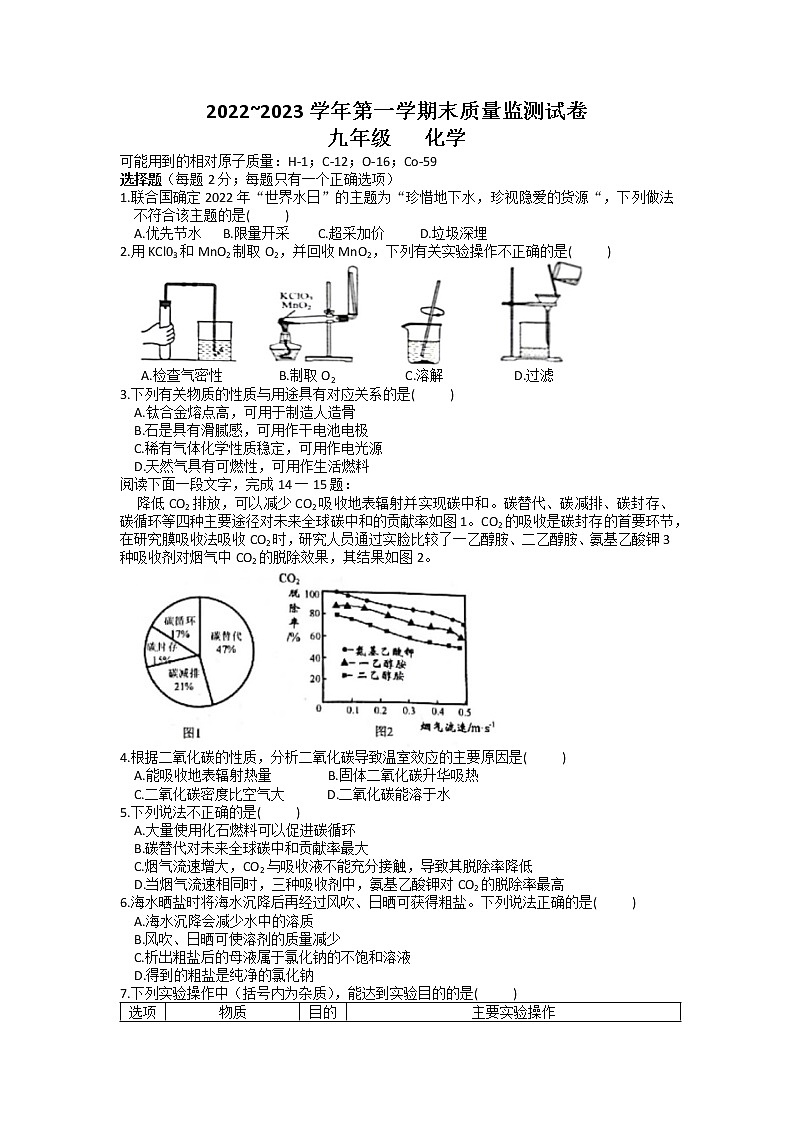
1.联合国确定2022年“世界水日”的主题为“珍惜地下水,珍视隐爱的货源“,下列做法不符合该主题的是( )
A.优先节水 B.限量开采 C.超采加价 D.垃圾深埋
2.用KCl03和MnO2制取O2,并回收MnO2,下列有关实验操作不正确的是( )
A.检查气密性 B.制取O2 C.溶解 D.过滤
3.下列有关物质的性质与用途具有对应关系的是( )
A.钛合金熔点高,可用于制造人造骨
B.石是具有滑腻感,可用作干电池电极
C.稀有气体化学性质稳定,可用作电光源
D.天然气具有可燃性,可用作生活燃料
阅读下面一段文字,完成14一15题:
降低CO2排放,可以减少CO2吸收地表辐射并实现碳中和。碳替代、碳减排、碳封存、碳循环等四种主要途径对未来全球碳中和的贡献率如图1。CO2的吸收是碳封存的首要环节,在研究膜吸收法吸收CO2时,研究人员通过实脸比较了一乙醇胺、二乙醇胺、氨基乙酸钾3种吸收剂对烟气中CO2的脱除效果,其结果如图2。
4.根据二氧化碳的性质,分析二氧化碳导致温室效应的主要原因是( )
A.能吸收地表辐射热量 B.固体二氧化碳升华吸热
C.二氧化碳密度比空气大 D.二氧化碳能溶于水
5.下列说法不正确的是( )
A.大量使用化石燃料可以促进碳循环
B.碳替代对未来全球碳中和贡献率最大
C.烟气流速增大,CO2与吸收液不能充分接触,导致其脱除率降低
D.当烟气流速相同时,三种吸收剂中,氨基乙酸钾对CO2的脱除率最高
6.海水晒盐时将海水沉降后再经过风吹、日晒可获得粗盐。下列说法正确的是( )
A.海水沉降会减少水中的溶质
B.风吹、日晒可使溶剂的质量减少
C.析出粗盐后的母液属于氯化钠的不饱和溶液
D.得到的粗盐是纯净的氯化钠
7.下列实验操作中(括号内为杂质),能达到实验目的的是( )
选项 | 物质 | 目的 | 主要实验操作 |
A | MgCl2溶液和蒸馏水 | 鉴别 | 分别取样,加入等量肥皂水,振荡,比较泡沫的多少 |
B | CO (CO) | 除杂 | 将混合气体点燃 |
C | CO2 | 验满 | 将点燃的木条伸入瓶中,观察是否熄灭 |
D | Fe和Cu的混合物 | 分离 | 加入足量稀盐酸,充分反应后过滤 |
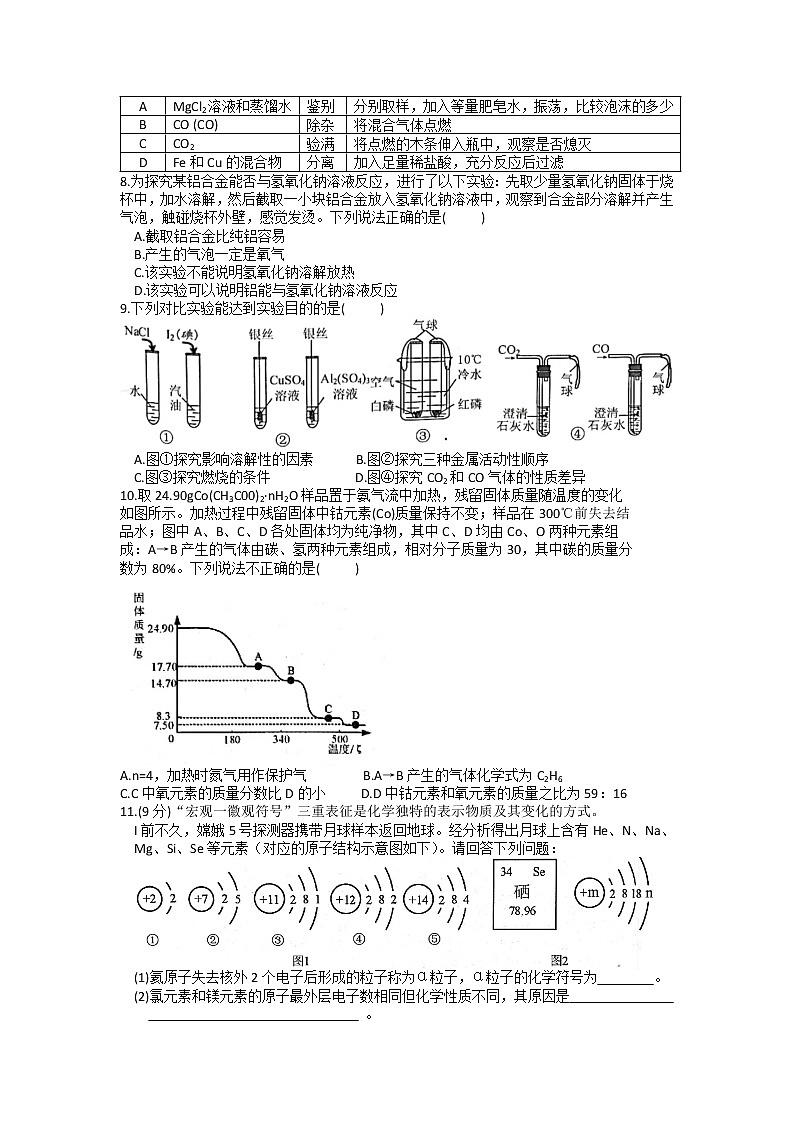
8.为探究某铝合金能否与氢氧化钠溶液反应,进行了以下实验:先取少量氢氧化钠固体于烧杯中,加水溶解,然后截取一小块铝合金放入氢氧化钠溶液中,观察到合金部分溶解并产生气泡,触碰烧杯外壁,感觉发烫。下列说法正确的是( )
A.截取铝合金比纯铝容易
B.产生的气泡一定是氧气
C.该实验不能说明氢氧化钠溶解放热
D.该实验可以说明铝能与氢氧化钠溶液反应
9.下列对比实验能达到实验目的的是( )
A.图①探究影响溶解性的因素 B.图②探究三种金属活动性顺序
C.图③探究燃烧的条件 D.图④探究CO2和CO气体的性质差异
10.取24.90gCo(CH3C00)2∙nH2O样品置于氨气流中加热,残留固体质量随温度的变化
如图所示。加热过程中残留固体中钴元素(Co)质量保持不变;样品在300℃前失去结
品水;图中A、B、C、D各处固体均为纯净物,其中C、D均由Co、O两种元素组
成:A→B产生的气体由碳、氢两种元素组成,相对分子质量为30,其中碳的质量分
数为80%。下列说法不正确的是( )
A.n=4,加热时氮气用作保护气 B.A→B产生的气体化学式为C2H6
C.C中氧元素的质量分数比D的小 D.D中钴元素和氧元素的质量之比为59:16
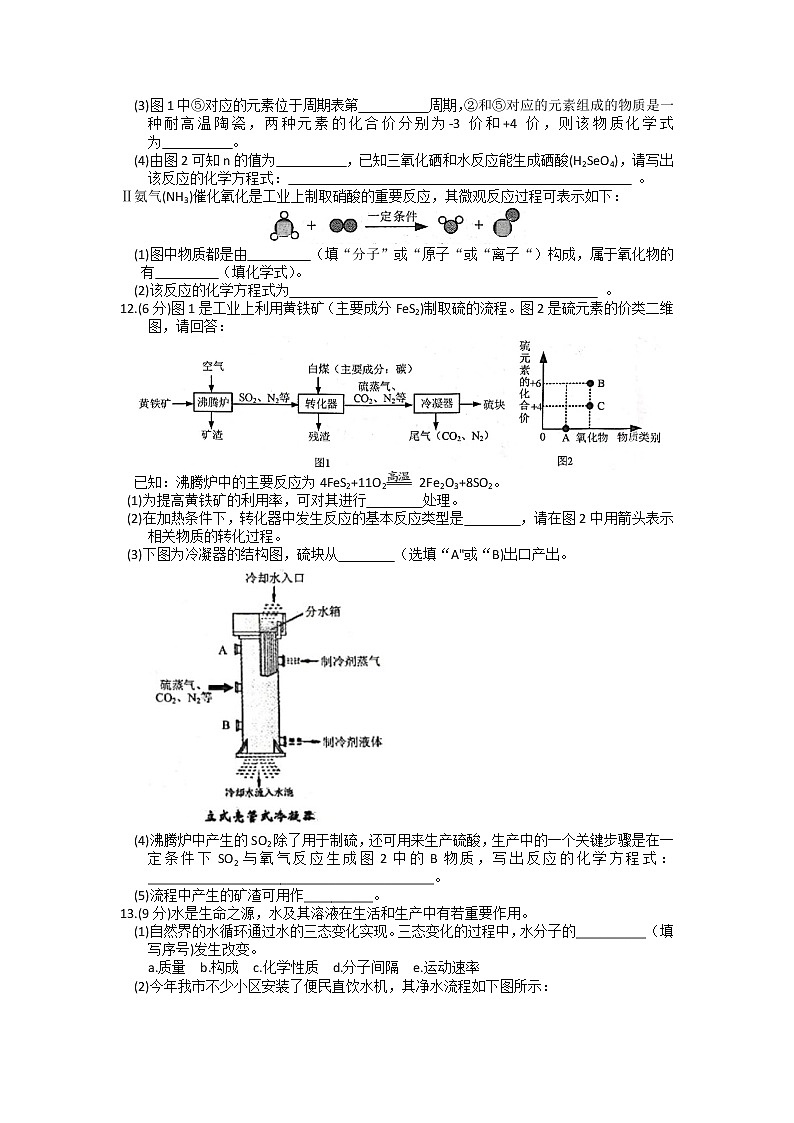
11.(9分)“宏观一徽观符号”三重表征是化学独特的表示物质及其变化的方式。
I前不久,嫦娥5号探测器携带月球样本返回地球。经分析得出月球上含有He、N、Na、
Mg、Si、Se等元素(对应的原子结构示意图如下)。请回答下列问题:
(1)氦原子失去核外2个电子后形成的粒子称为α粒子,α粒子的化学符号为 。
(2)氯元素和镁元素的原子最外层电子数相同但化学性质不同,其原因是
。
(3)图1中⑤对应的元素位于周期表第 周期,②和⑤对应的元素组成的物质是一种耐高温陶瓷,两种元素的化合价分别为-3价和+4价,则该物质化学式为 。
(4)由图2可知n的值为 ,已知三氧化硒和水反应能生成硒酸(H2SeO4),请写出该反应的化学方程式: 。
Ⅱ氨气(NH3)催化氧化是工业上制取硝酸的重要反应,其微观反应过程可表示如下:
(1)图中物质都是由 (填“分子”或“原子“或“离子“)构成,属于氧化物的有 (填化学式)。
(2)该反应的化学方程式为 。
12.(6分)图1是工业上利用黄铁矿(主要成分FeS2)制取硫的流程。图2是硫元素的价类二维图,请回答:
已知:沸腾炉中的主要反应为4FeS2+11O2 2Fe2O3+8SO2。
(1)为提高黄铁矿的利用率,可对其进行 处理。
(2)在加热条件下,转化器中发生反应的基本反应类型是 ,请在图2中用箭头表示相关物质的转化过程。
(3)下图为冷凝器的结构图,硫块从 (选填“A"或“B)出口产出。
(4)沸腾炉中产生的SO2除了用于制硫,还可用来生产硫酸,生产中的一个关键步骤是在一定条件下SO2与氧气反应生成图2中的B物质,写出反应的化学方程式:_________________________________________。
(5)流程中产生的矿渣可用作__________。
13.(9分)水是生命之源,水及其溶液在生活和生产中有若重要作用。
(1)自然界的水循环通过水的三态变化实现。三态变化的过程中,水分子的__________(填写序号)发生改变。
a.质量 b.构成 c.化学性质 d.分子间隔 e.运动速率
(2)今年我市不少小区安装了便民直饮水机,其净水流程如下图所示:
①上述三级处理器涉及的净水原理均为__________(填“物理”或“化学”)变化,
②水中的细菌、病毒等微生物被精滤器中的超滤膜除去,是因为超滤膜的孔径__________(填“大于”或“小于”)细菌、病毒等微生物的粒径。
③若没有砂滤器,则对后续净水造成的影响是____________________________________。
(3)实验室采用蒸馏法将天然水净化,并用于实验。
①请再列举一种工业生产中利用该原理分离混合物的例子:________________________。
②铈的化合物具有良好的光学、电学性质,广泛应用于平板显示和计算机芯片等领域。如图1所示是硝酸钾(KNO3)与硫酸铈[Ce2(SO4)3]的溶解度曲线。若硫酸铈固体中混有少量硝酸钾杂质,则提纯硫酸铈的实验方案是________________________。(写出具体的操作过程)
③硫酸饰[Ce2(SO4)3]可由Ce(SO4)2与H2O2反应制得,同时生氧气和硫酸,试写出该反应的化学方程式:________________________。己知Ce(SO4)2与H2O2反应的速率与温度的关系如图2所示。当温度高于T0时,反应速率逐渐减小的可能原因是_______________________。
14.(10分)某项目学习小组开展“影响铁锈蚀因素及控制实验条件的探究。
I探究铁锈蚀的条件
同学们设计了如图1所示实验进行探究。
(1)设计b试管实验的目的是创设_________________的实验条件。
(2)一周后试管a中的铁钉生锈而试管c中的铁钉没有生锈,由此可得出的结论
是_________________。
(3)铁锈蚀后应及时除锈的原因是_________________。
(4)仔细观察b试管中铁钉,发现也有锈蚀现象。同学们对此展开深入研究。将煮沸冷却
后的蒸馏水倒入烧杯中,迅速倒入植物油铺满水面。然后将溶解氧传感器插入水中,通风环境中持续三天采集得到数据图像如图2所示(室温下,自然状况的水中溶解气约为8~9mgL1)。据此回答:
①b试管中铁钉也出现了锈蚀现象的原因是_________________。
②为达到图1设计实验的目的,针对b试管可采取的改进措施有_________________。
Ⅱ探究植物油隔离对其他气体在水中溶解情况的影响
(1)制取二氧化碳。写出实验室制取CO2的反应方程式:_______________________________。
(2)用两个量筒分别收集100mLCO2并倒置于水槽中,向其中一个量筒内注入少量植物油,使CO2与水被植物油隔开(CO2与植物油不反应)(如图3、图4所示)。图3表
示无植物油隔离时,量筒内气体中存在的CO2分子的微观示意图。
①实验测得量筒内CO2体积随时间变化曲线如图5。由图可得出的结论是__________________________。
②请参照图3的表示方式,在图4方框中画出有植物油隔离时,量简内水中存在的分子的微观示意图____________。
(3)请设计实验方案,检验有植物油隔离时CO2是否会进入水中:_______________________。
15.(6分)标准状况下(0℃,101kPa),向96克水中加入4克氢氧化钠(增加溶液的导电性,
不参与反应),通电一段时间,当收集到44.8L氢气时,剩余溶液的质量为64克。请回答下列问题:
(1)电解水生成的氢气和氧气的质量比为__________。
(2)标准状况下,氧气的密度为__________g/L;(计算结果精确到0.1)
(3)标准状况下,如使44.8L的氢气完全燃烧至少需要多少克氧气?(写出计算过程)
(4)剩余溶液中溶质的质量分数为_______________。
2022-2023学年度第一学期期末化学参考答案
1-10选择题:
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
答案 | D | B | D | A | A | B | A | C | D | C |
11.(9分)I(1)He2+(2)氦原子最外层电子数已满(达到相对稳定结构),镁原子最外层电子数未满(不稳定)(3)三 Si3N4 (4)6 SeO3+H2O=H2SeO4
II.(1)分子H2O和NO (2)4NH3+5O2====4NO+6H2O
12.(6分)(1)粉碎 (2)置换反应 C→A(在图中标注)
(3)B (4)2SO2+O2 ====2SO3(5)炼铁或用作颜料等
13.(9分)(1)d、e (2)①物理②小于③使净水速度变慢,净水效率降低
(3)①分离液态空气或分馏石油
②常温下将固体混和物边加水边搅拌至刚好溶解,然后逐渐加热升温至有大量晶体析出,过滤,洗涤干燥所得固体即纯净硫酸铈(2分)
③ 2Ce (SO4)2+H2O2==Ce2(SO4)3+H2SO4+O2↑
随温度升高,过氧化氢分解加快,使反应物浓度降低,反应速度减慢
14.(10分)I(1)无氧(或隔绝氧气)
(2)铁生锈需要与水接触
(3)铁锈疏松多孔有吸附性,能进一步吸附水和氧气加快铁锈蚀
(4)①在通风环境中,空气中的氧气能穿过植物油层进入水中(或在通风环境中,植物油不能使氧气与水隔离等)
②在b试管口塞上橡皮塞
II(1)CaCO3+2HC1====CaCl2+H2O+CO2↑
(2)①植物油不能完全使CO2与水隔离(或CO2能穿过植物油溶入水中等)
②H2O、CO2、H2CO3(2分)(画对1个得1分,画全得2分)
(3)取少量有植物油隔绝的(图4)量筒内的水,滴加石蕊溶液,若石蕊变红,则说明有CO2进入水中。
15.(6分)(1)1:8 (2)1.4g/L
(3)32g (3分)
方法一:通过计算电解36g水可以得到4g氢气,再计算4g氢气燃烧需要32克氧气;
方法二:通过计算电解36g水可以得到32g氧气,但要强调根据质量守恒定律可知燃烧44.8L氢气也需要32克氧气(否则只得2分)
方法三:根据电解水和氢气燃烧的方程式找出水、氢气和氧气的关系:2H2O~2H2~O2,然后根据关系式法计算电解36g水产生的氢气再燃烧需要32g氧气
(4)6.25%
江苏省南通市海安市2024届九年级上学期期末学业质量监测化学试卷(含答案): 这是一份江苏省南通市海安市2024届九年级上学期期末学业质量监测化学试卷(含答案),共16页。试卷主要包含了单选题,填空题,实验题,计算题等内容,欢迎下载使用。
2022-2023学年江苏省南通市海安市九年级上学期化学期末试题及答案: 这是一份2022-2023学年江苏省南通市海安市九年级上学期化学期末试题及答案,共15页。试卷主要包含了选择题等内容,欢迎下载使用。
江苏省南通市海安市2023-2024学年九年级上学期11月期中化学试题: 这是一份江苏省南通市海安市2023-2024学年九年级上学期11月期中化学试题,共8页。试卷主要包含了亚氯酸钠中氯元素的化合价是,下列说法不正确的是,下列实验方案能达到实验目的的是等内容,欢迎下载使用。












