




所属成套资源:2022年中考化学专题模块习题练本课件
2022年中考化学专题突破篇第27课时工艺流程图题练本课件
展开
这是一份2022年中考化学专题突破篇第27课时工艺流程图题练本课件,共48页。PPT课件主要包含了NaCl,隔绝水,将菱镁矿石粉碎,H2SO4,节约资源环保,二氧化硫,AgCl,置换反应,碳酸钙,玻璃棒等内容,欢迎下载使用。
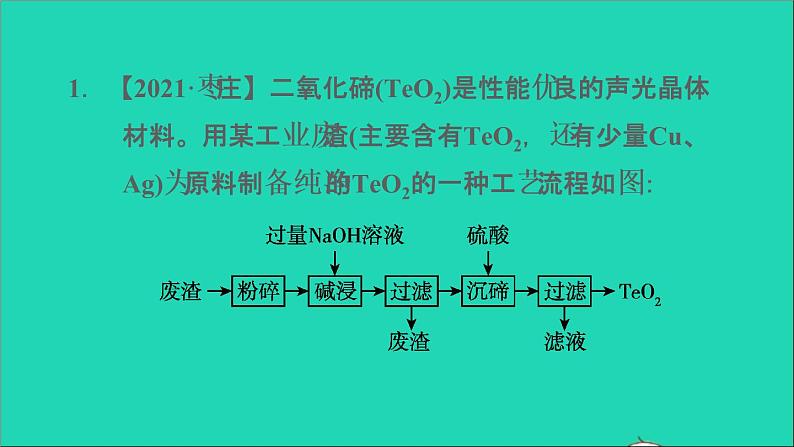
1.【2021·枣庄】二氧化碲(TeO2)是性能优良的声光晶体材料。用某工业废渣(主要含有TeO2,还有少量Cu、Ag)为原料制备纯净的TeO2的一种工艺流程如图:
已知:TeO2微溶于水,能与NaOH发生反应。回答下列问题:(1)粉碎的目的是_________________________________。(2)类比CO2和NaOH反应,写出“碱浸”时发生反应的化学方程式:________________________________。(3)“碱浸”后过滤,此时滤渣成分为 ________。(4)“沉碲”时,加入硫酸的作用为_____________________________________。
增大反应物接触面积,加快反应速率
2NaOH+TeO2===Na2TeO3+H2O
与Na2TeO3反应生成微溶于水的TeO2
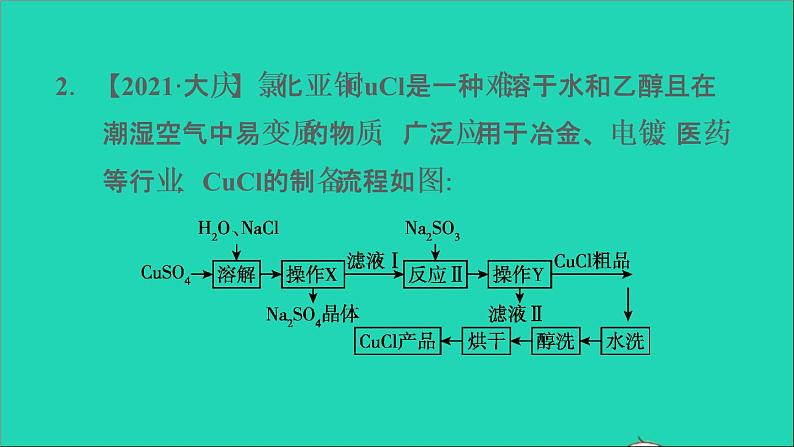
2.【2021·大庆】氯化亚铜CuCl是一种难溶于水和乙醇且在潮湿空气中易变质的物质,广泛应用于冶金、电镀、医药等行业,CuCl的制备流程如图:
(1)“操作Y”的名称是 ________________。(2)CuCl中铜元素的化合价为 ____________。(3)请配平“反应Ⅱ”的化学方程式:____CuCl2+_____ Na2SO3+__________H2O===________CuCl↓+________NaCl+________H2SO4。
(4)在“滤液Ⅱ”中可以循环利用的物质(水除外)是________________(填化学式)。(5)“醇洗”的目的是 ______________________,防止后续过程中氯化亚铜变质。
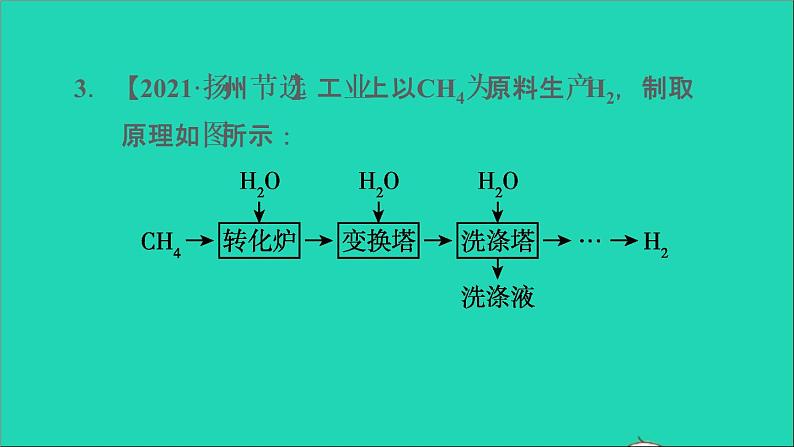
3.【2021·扬州节选】工业上以CH4为原料生产H2,制取原理如图所示:
已知变换塔、洗涤塔发生的主要反应依次是:
使二氧化碳与水充分反应
(2)“洗涤塔”中气体从塔底通入,水从塔顶喷淋。这样操作的优点是 _____________________________。(3)有32 g CH4参与反应(假设各步反应都完全转化),理论上可制得 ____________g H2。
4.【2021·扬州节选】以某菱镁矿石(主要成分是MgCO3,含少量MnCO3、SiO2)制取MgSO4·7H2O,流程如下:
(1)“酸浸”时,为了提高浸取率,除了搅拌、提高硫酸浓度外,还可采取的措施有________________________ (写出一种)。此时,MnCO3发生反应的化学方程式是_____________________________________________。(2)“转化”时主要反应是NaClO+MnSO4+H2O===MnO2↓+NaCl+H2SO4,氯元素反应前后化合价变化情况是________(填“升高”或“降低”)。
MnCO3+H2SO4===MnSO4+CO2↑+H2O
(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
①“操作Ⅰ”的具体操作是:蒸发浓缩滤液至表面有晶膜出现(此时MgSO4溶液已饱和)、______________________________________、过滤、洗涤、低温干燥。②“操作Ⅰ”所得滤液中能分离出一种可循环使用的物质,该物质是__________ (填化学式)。循环使用的目的是___________________。
降温(温度在1.8 ℃~48.1 ℃)结晶
5.【2021·赤峰】工业上可以通过如图工艺流程处理工厂排放的含二氧化硫的尾气,并获得硫酸和氢气。
主反应器中发生反应的化学方程式为SO2+2H2O+I2===H2SO4+2HI。请回答下列问题:(1)该反应涉及的物质中属于氧化物的有_______________。(2)该反应前后,化合价发生变化的元素有碘和____________。
(3)尾气中SO2的质量分数为10%,若吸收该尾气80 t,理论上能够生产硫酸的质量为________t。(4)在整个工艺流程中,能被循环利用的物质是_______。
6.【2021·莆田质检·9分】中央处理器(CPU)是电子计算机的主要设备之一。下图是回收废旧CPU中的金属单质Au(金)、Ag、Cu的部分工艺流程。
(1)操作Ⅰ的名称是________。(2)物质D的化学式是________________。(3)往溶液A中加Fe粉,需过量的目的是__________________________________________。(4)通过反应④,可以判断Fe的金属活动性比Cu的_____ (填“强”或“弱”),其发生反应的化学方程式为______________________________,此反应的基本反应类型是________________。
将Cu(NO3)2中的Cu完全置换出来(合理即可)
Fe+2HCl===FeCl2+H2↑
7. (立德树人·文化自信)【2021·桂林】早在战国时期,《周礼·考工记》就记载了我国劳动人民制取KOH以漂洗丝帛的工艺。大意是:先将干燥的木头烧成灰(含K2CO3),用其灰汁浸泡丝帛,再加入石灰即可。如图为模拟该法制取KOH的工艺流程。请回答有关问题。
(1)桂林有丰富的石灰石资源,石灰石的主要成分是____________。(2)实验室里进行操作②、操作③均用到的玻璃仪器是____________。(3)“反应池”中发生主要反应的化学方程式是______________________________________。
K2CO3+Ca(OH)2===CaCO3↓+2KOH
(4)“制浆”中发生反应的基本反应类型是_____________。(5)流程中可循环使用的物质是_______________。(6)“燃烧窑”中产生的热量可供煅烧和操作______(填“①”、“②”或“③”)利用。
8.【2021·广东】牙膏中常用碳酸钙粉末作摩擦剂,利用石灰石(杂质不溶于水和酸)制备纯净碳酸钙的一种方法如图。
(1)反应①的化学方程式为________________________,操作Ⅰ的名称是________。(2)反应②的化学方程式为 _____________________________________,该反应属于________________ (填基本反应类型)反应。
Na2CO3+CaCl2===CaCO3↓+2NaCl
(3)该方法中,用稀硫酸代替稀盐酸对制备碳酸钙是否有影响?判断并简述理由:_______________________________________________________________________________________________________________________________________。
有影响,因为稀硫酸和氧化钙反应生成的硫酸钙微溶于水,会导致部分钙离子随着不溶物除去,使溶液B中钙离子减少,从而导致碳酸钙产率降低
(4)大气中CO2含量不断上升,会导致_____________。我国在联合国大会上提出:努力争取在2060年前实现“碳中和”。请提出一条实现“碳中和”的措施:________________________________。
植树造林(或低碳出行等)
9.【2021·重庆A】某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图Ⅰ(小部分产物略去)。
查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+。b.Fe3+、Ni2+转化为对应的氢氧化物沉淀时,溶液pH如图。
(1)步骤Ⅰ的操作为________________。(2)滤渣①的成分为________________。(3)单质Fe参与反应的化学方程式为____________________________________(任写一个)。
Fe+H2SO4===FeSO4+H2↑
(4)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为________(填序号)。A.1 B.2 C.6 D.10 (5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为________________________。
10.【2021·山东菏泽三模】科技的发展离不开化学的身影,大数据云平台的时代已经到来,二氧化铬(CrO2)可用于生产电子信息记录材料,制备CrO2的主要流程如下:
(1)上述流程中,Cr元素的化合价有________种,属于氧化物的有______________(填化学式)。(2)推测反应器1放出的气体中含N2,从元素守恒角度说明理由:________________________________________。(3)上述流程中,用于分离提纯的设备有______________。
反应物含有氮元素,则生成物中也会含有氮元素
11.【2021·晋中】造纸术是中国古代四大发明之一。一直以来,传统工艺不断改进。现阶段,利用方解石(主要成分为CaCO3,还含有少量MgO、Fe2O3、SiO2等杂质)造纸已较为普遍,它取代传统的植物纤维造纸,全程无需用水,原料造价仅为传统造纸的1/3。(已知:SiO2、聚乙烯塑料、黏合剂均难溶于水,且不与盐酸反应)分析生产过程,回答下列问题:
(1)将方解石粉碎成纳米级超细粉末的目的是____________________________(合理即可)。(2)混合器内需要进行的操作是____________。(3)利用方解石作原料生产纸张的优点是____________________________(合理即可)。
(4)从绿色环保的角度分析,需要对使用的原料改进的地方是____________________________________(合理即可)。(5)成品纸张在保存过程中应避免与酸接触,若遇到稀盐酸,则可能发生反应的化学方程式为________________________________________________________________(写1个,合理即可)。
使用可降解塑料,使用无毒无害的黏合剂
CaCO3+2HCl===CaCl2+H2O+CO2↑(Fe2O3+6HCl===2FeCl3+3H2O)
12.【2021·苏州节选】硫酸亚铁是一种重要的补铁剂。实验室以废铁屑(含少量Fe2O3)为原料制备硫酸亚铁晶体的流程如图所示:
已知:铁与硫酸铁反应的化学方程式为Fe+Fe2(SO4)3===3FeSO4。(1)“碱洗”是为了洗去铁屑表面的油污。用热的碳酸钠溶液浸泡,过滤,再用蒸馏水洗涤2~3次。取最后一次洗涤液,测其pH,若pH=________,说明洗涤液中无碳酸钠。
(2)“酸溶”是向“碱洗”过的铁屑中加入过量稀硫酸。①写出铁与稀硫酸反应的化学方程式:____________________________。②所用硫酸溶液浓度不能太稀,原因是________________________________________。③废铁屑中的少量Fe2O3不需要进行除杂处理,原因是 ______________________________________________________________。
反应速率太慢,结晶步骤能耗过多
氧化铁与硫酸反应生成硫酸铁,硫酸铁与铁反应生成硫酸亚铁
13. (创新题)温室效应加剧是由以二氧化碳为主的温室气体大量排放导致的,因此控制二氧化碳的排放量对于减缓温室效应具有重要的意义。如图为富氧燃烧技术的工艺流程图,利用富氧燃烧技术产生的烟气中,二氧化碳的浓度高达95%,不需要分离可直接液化回收,有效地减少了温室气体的排放。
(1)设备1的作用是___________,利用的原理是________________________。(2)设备2中加入的煤要提前进行粉碎,目的是________________________________________。设备2中主要发生反应的化学方程式为____________________________。
增大反应物的接触面积,使反应更快更充分
(3)在液化处理以CO2为主的烟气时,SO2也被液化回收,这样又可以缓解__________的环境问题。(4)回收的二氧化碳可用于______(写一点即可)。
14.【2021·泰安】某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如图所示。请回答下列问题:
(1)工厂废液中加入过量A反应的化学方程式为__________________________________。(2)用化学式表示固体甲的成分__________。(3)溶液甲中的金属离子是____________(用离子符号表示)。(4)完成步骤④的化学方程式:4Fe(OH)2+O2+2________ ===4Fe(OH)3。
Fe+CuCl2===FeCl2+Cu
15.【2021·东营】海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图(如图)回答问题:
(1)步骤Ⅰ除杂中,常见的方法有两种:一是物理方法,即用NaCl溶液浸洗粗盐,溶解除去其中的可溶性杂质,则浸洗溶液应选用NaCl的________(填“饱和”或“不饱和”)溶液;二是化学方法,操作步骤依次为:加水溶解→加过量试剂①→加过量试剂②→过滤→加适量盐酸,
以下试剂①②组合选用合理的是________。A.①Ca(OH)2 ②Na2CO3B.①Na2CO3 ②Ca(OH)2C.①KOH ②Na2CO3D.①NaOH ②Na2CO3
相关课件
这是一份安徽中考复习 人教版化学 题型突破 题型四 工艺流程图题 课件,共29页。PPT课件主要包含了专题突破·明技法,Fe和Cu,较多固体出现,玻璃棒,FeSO4+,作钾肥,强化训练·检成效,HCl,H2O,复分解反应等内容,欢迎下载使用。
这是一份中考化学二轮专题复习专题课件- 工艺流程图题 (含答案),共25页。PPT课件主要包含了·类型1物质的制备,类型1物质的制备,SiO2,复分解反应,化合反应,镁氧化铜,ZnOH2,加快反应速率,NaOH等内容,欢迎下载使用。
这是一份中考化学复习第25课时工艺流程图题作业课件,共29页。PPT课件主要包含了氧气和水,SO2,Fe2+,Mg2+,氮气和氧气的沸点不同,分离空气,CaCO3,K2CO3,蒸发结晶,OH-等内容,欢迎下载使用。








