
2022年广东省广州市白云区中考一模化学试题(word版无答案)
展开一、选择题:本题包括14小题,每小题3分,共42分。
1.垃圾分类从我做起。废旧金属属于
2.医用外科口罩,以聚丙烯[(C3H6)n] (n约为103~104) 为主要原料,对细菌、病毒有很强的阻隔作用。下列说法错误的是
A.用过的口罩应集中处理、销毁
B.对细菌、病毒的阻隔属于物理变化
C.聚丙烯的相对分子质量是42
D.聚丙烯是有机合成材料
3.葡萄糖酸钙是常用的补钙剂,其化学式为Ca(C6H11O7)2。下列关于葡萄糖酸钙的说法正确的是
A.钙是人体必需的微量元素 B.葡萄糖酸钙中氢元素的质量分数最小
C.由49个原子构成 D.钙元素、氧元素的质量比为1:14
4.乙醇是一种清洁能源。科学家利用新型催化剂,将二氧化碳转化为液态燃料乙醇,反应的微观示意图如图。下列说法不正确的是
A.反应前后都是混合物 B.反应前后有2种氧化物
C.若有44g二氧化碳反应,则生成氧气48g D.以上为置换反应
5.下列选项中,利于培养化学学科核心素养的是
A.变化与守恒:某物质R燃烧后生成CO2和H2O,则R中一定含C、H、O元素
B.模型与推理:碱中含有OH-,所以Cr(OH)SO4是碱类
C.宏观与微观:品红在水中扩散,说明分子总在不停地运动
D.探究与创新:探究红砖粉是否为过氧化氢分解的催化剂,只需设计实验证明红砖粉能否改变反应速率即可
6.端午节是我国重要的传统节日之一,包粽子是家庭劳动的项目。以下说法正确的是
A.“粽子香,香厨房。艾叶香,香满堂”香飘满堂说明分子的体积和质量都很小
B.粽子馅料可用多种食材,包括糯米、瘦肉、蛋黄等,其中富含糖类的是蛋黄
C.以上粽子的馅料中,缺乏的营养素之一是维生素
D.粽子馅料需要用含碘盐腌制一段时间, 碘元素可预防贫血
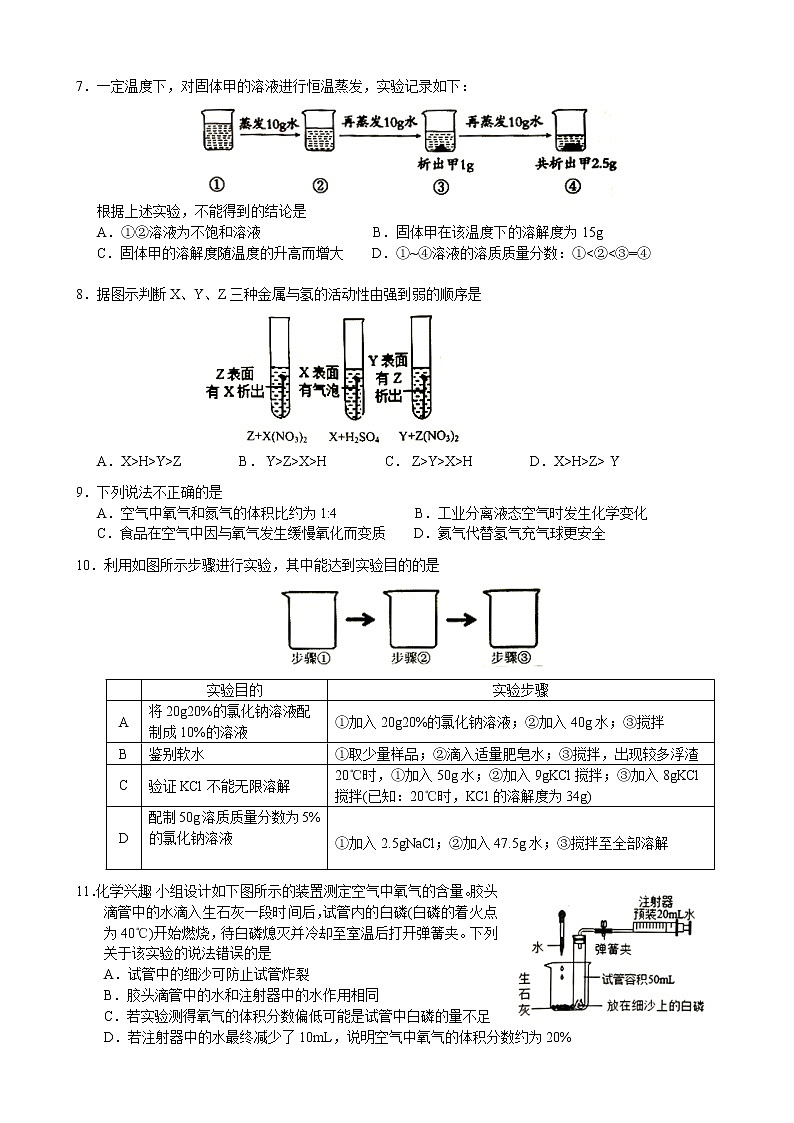
7.一定温度下,对固体甲的溶液进行恒温蒸发,实验记录如下:
根据上述实验,不能得到的结论是
A.①②溶液为不饱和溶液 B.固体甲在该温度下的溶解度为15g
C.固体甲的溶解度随温度的升高而增大 D.①~④溶液的溶质质量分数:①<②<③=④
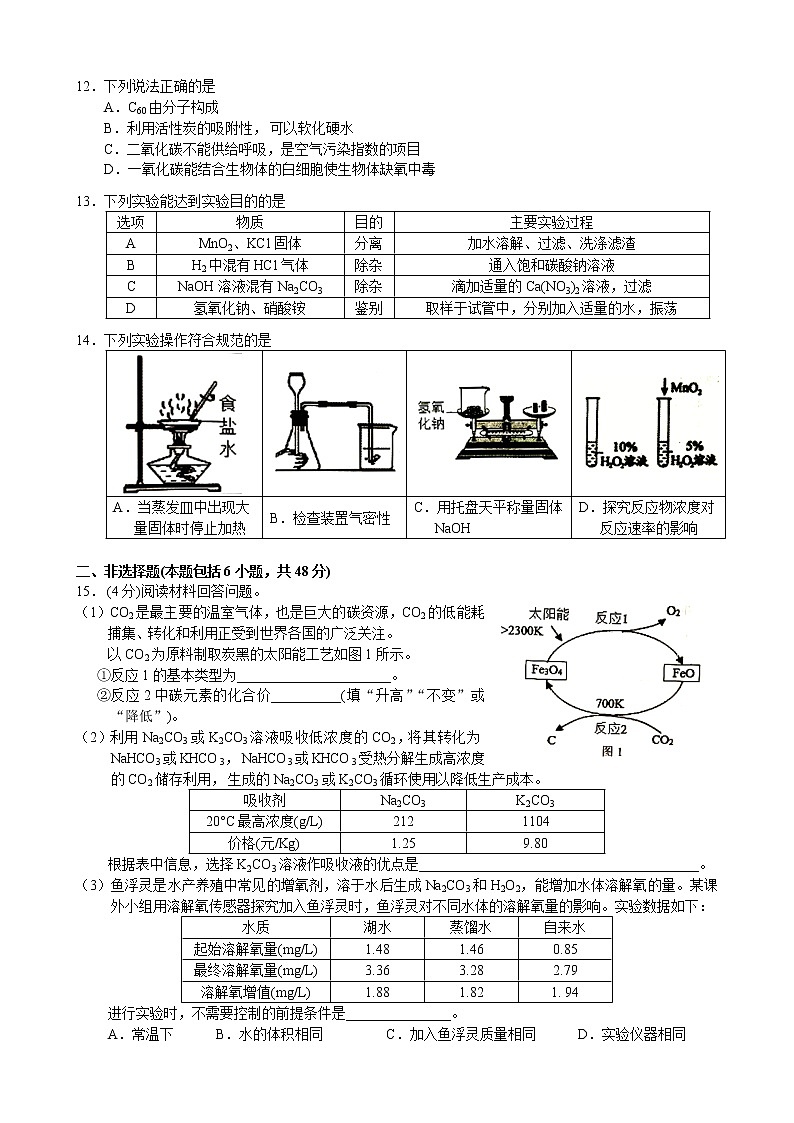
8.据图示判断X、Y、Z三种金属与氢的活动性由强到弱的顺序是
A.X>H>Y>Z B. Y>Z>X>H C. Z>Y>X>H D.X>H>Z> Y
9.下列说法不正确的是
A.空气中氧气和氮气的体积比约为1:4 B.工业分离液态空气时发生化学变化
C.食品在空气中因与氧气发生缓慢氧化而变质 D.氦气代替氢气充气球更安全
10.利用如图所示步骤进行实验,其中能达到实验目的的是
11.化学兴趣 小组设计如下图所示的装置测定空气中氧气的含量。胶头滴管中的水滴入生石灰一段时间后,试管内的白磷(白磷的着火点为40℃)开始燃烧,待白磷熄灭并冷却至室温后打开弹簧夹。下列关于该实验的说法错误的是
A.试管中的细沙可防止试管炸裂
B.胶头滴管中的水和注射器中的水作用相同
C.若实验测得氧气的体积分数偏低可能是试管中白磷的量不足
D.若注射器中的水最终减少了10mL,说明空气中氧气的体积分数约为20%
12.下列说法正确的是
A.C60 由分子构成
B.利用活性炭的吸附性, 可以软化硬水
C.二氧化碳不能供给呼吸,是空气污染指数的项目
D.一氧化碳能结合生物体的白细胞使生物体缺氧中毒
13.下列实验能达到实验目的的是
14.下列实验操作符合规范的是
二、非选择题(本题包括6小题,共48分)
15. (4分)阅读材料回答问题。
(1)CO2是最主要的温室气体,也是巨大的碳资源,CO2的低能耗捕集、转化和利用正受到世界各国的广泛关注。
以CO2为原料制取炭黑的太阳能工艺如图1所示。
①反应1的基本类型为______________________。
②反应2中碳元素的化合价__________(填“升高”“不变”或“降低”)。
(2)利用Na2CO3或K2CO3 溶液吸收低浓度的CO2,将其转化为NaHCO3或KHCO3, NaHCO3或KHCO3受热分解生成高浓度的CO2储存利用, 生成的Na2CO3或K2CO3循环使用以降低生产成本。
根据表中信息,选择K2CO3溶液作吸收液的优点是________________________________________。
(3)鱼浮灵是水产养殖中常见的增氧剂,溶于水后生成Na2CO3和H2O2,能增加水体溶解氧的量。某课外小组用溶解氧传感器探究加入鱼浮灵时,鱼浮灵对不同水体的溶解氧量的影响。实验数据如下:
进行实验时,不需要控制的前提条件是_______________。
A.常温下 B.水的体积相同 C.加入鱼浮灵质量相同 D.实验仪器相同
16. (11分)“ 宏微符”三重表征是重要的化学学科素养,请回答下列问题。
(1)《鲁滨逊漂流记》中的主人公在荒岛采用如图2方法将海水淡化。
①冷海水的作用是_________________________。图中得到的饮用水属于___________(混合物或纯净物)。
②从微观角度分析上述过程,下列说法正确的是_________(填序号)。
A.蒸发时水分子体积变大 B.冷凝时水分子质量减小
C.蒸发时水分子运动速率加快 D.冷凝时水分子间隔减小
(2)图3是稀盐酸和硝酸银反应,产生了白色沉淀,请另写一个与该反应的微观实质相同的化学方程式 :________________________________________________。
(3)某同学在收集满CO2的集气瓶中放入燃烧的钠,钠继续燃烧,充分反应后生成黑色的碳单质和一种白色固体。该同学认为白色固体可能是小苏打,请分析该猜想不合理的原因:__________________________________________________________。请写出钠在CO2中燃烧的化学方程式____________________________________。
(4)在硫酸铜溶液文中加入足量的铁钉充分反应,所得溶液质量随反应时间的变化如图4,请在图5上画出曲线上A、B两点所对应的溶液:液中存在的离子示意图,并进行必要的标注。
17.(8分)双氧水脱硫处理烟气(含SO2),并用铝灰(主要成分为Al、 Al2O3以及不溶于酸的混合结渣)制备硫酸铝的主要工艺流程如下:
注:除尘器的作用为除去悬浮在气体中的粉尘。
(1)脱硫塔中,双氧水脱硫过程发生的反应主要有:
①SO2+H2O === X;
②H2O2+X === Y+ H2O,Y的化学式是__________________。
反应①和②中化学价均未发生变化的元素是________________________。
吸收6.4Kg SO2能产生30%的Y溶液_________________Kg。(保留一位有效小数)
(2)用喷洒的方式注入双氧水的目的是________________________________________________。
(3)反应器中,生成氢气的原因是____________________________________(用化学方程式解释)。
(4)上图中Z的作用是_________________________________________。
(5) 上述流程中,烟气经过脱硫塔和________________设备的处理,减少了其对环境的污染。
18.(9分) N是空气中含量最高的元素。
(1)将含N物质进行分类,按要求写出化学式
单质 引起酸雨的氧化物 酸 含氮的不同化合价的盐
N2 ( ① ) HNO3 ( ② )
(2)镓元素的信息如图。
请设计理论上制备硝酸镓的三种方案(要求含镓原料分别属于不同的化合物类别)
(3)若硫酸铝铵晶体[NH4Al(SO4)2·12H2O,相对分子质量453]
①加热过程中,其质量随时间的变化如图所示。据此判断,从200℃到500℃间固体是否还存在结晶水,并作出解释。__________(是或否),_______________________________________________。
②写出一个能与硫酸铝铵溶液发生反应的原子团__________________________(写离子符号)。
19.(7分)实验室制取气体。
(1)选用药品进行对比实验。按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),测得产生二氧化碳体积随时间变化曲线如图所示:
①图中丙对应实验_____________(选填“I” “II”或“III”)。
②不用甲对应的药品,理由是_________________________________________________________。
(2)实验室制取多瓶氧气
①组装能随意添加双氧水的装置,应选用_______________________(选填编号)。
写出仪器c的名称_____________________。
写出用双氧水、二氧化锰制取氧气的化学方程式_______________________________________。
②收集氧气。用上图装置收集时,空气从___________端排出。
③写出用②收集氧气验满的方法_______________________________________________________。
20.(9分)有一包不纯的K2CO3样品,可能含有一定量的FeCl3、 K2SO4、KCl、KHCO3。小明为确定其成分,取10g样品充分溶解后进行如下实验。
查阅资料:碳酸氢钾可溶于水,难溶于乙醇。100℃时开始分解,200℃时完全分解,产生二氧化碳和碳酸钾等物质。
a.取少量样品于烧杯中,加入足量的水溶解,得到无色溶液A
b.取少量溶液A于试管中,滴入酚酞,溶液变红色
c.取少量溶液A于试管中,滴入足量的稀硝酸,再滴入适量氯化钡溶液,产生气泡,得到无色溶液B
d.取少量溶液B于试管中,滴入适量硝酸银溶液,有白色沉淀产生
(1)小明发现以上步骤错误的是___________(填选项),正确的实验操作是_________________________
____________________________________________________________________, 有白色沉淀产生。
(2)根据正确的实验操作和现象,分析上述实验过程,关于该样品的成分可以得到的结论是__________
_____________________________________________________________________________________。
(3)设计实验方案,进一步确定该样品的成分,完成下表。
(4)该样品作为肥料时_________________(能或不能)与铵态氮肥混合使用。
实验目的
实验步骤
A
将20g20%的氯化钠溶液配制成10%的溶液
①加入20g20%的氯化钠溶液;②加入40g水;③搅拌
B
鉴别软水
①取少量样品;②滴入适量肥皂水;③搅拌,出现较多浮渣
C
验证KCl不能无限溶解
20℃时,①加入50g水;②加入9gKCl搅拌;③加入8gKCl搅拌(已知:20℃时,KCl的溶解度为34g)
D
配制50g溶质质量分数为5%的氯化钠溶液
①加入2.5gNaCl;②加入47.5g水;③搅拌至全部溶解
选项
物质
目的
主要实验过程
A
MnO2、KCl固体
分离
加水溶解、过滤、洗涤滤渣
B
H2中混有HCl气体
除杂
通入饱和碳酸钠溶液
C
NaOH溶液混有Na2CO3
除杂
滴加适量的Ca(NO3)2溶液,过滤
D
氢氧化钠、硝酸铵
鉴别
取样于试管中,分别加入适量的水,振荡
A.当蒸发皿中出现大量固体时停止加热
B.检查装置气密性
C.用托盘天平称量固体NaOH
D.探究反应物浓度对反应速率的影响
吸收剂
Na2CO3
K2CO3
20°C最高浓度(g/L)
212
1104
价格(元/Kg)
1.25
9.80
水质
湖水
蒸馏水
自来水
起始溶解氧量(mg/L)
1.48
1.46
0.85
最终溶解氧量(mg/L)
3.36
3.28
2.79
溶解氧增值(mg/L)
1.88
1.82
1. 94
方案
预期反应的化学方程式
①
②
③
实验编号
药品
I
块状大理石、10%H2SO4溶液
II
块状大理石、7%HC1 溶液
III
大理石粉末、7%HC1溶液
实验操作
预期现象与结论
________________________
若__________________________,则该样品含有可能存在的成分;
若__________________________,则该样品不含可能存在的成分。
2023年广东省广州市白云区中考一模化学试题(含答案): 这是一份2023年广东省广州市白云区中考一模化学试题(含答案),共8页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
2020年广东省广州市白云区中考一模化学试题: 这是一份2020年广东省广州市白云区中考一模化学试题,文件包含精品解析2020年广东省广州市白云区中考一模化学试题解析版doc、精品解析2020年广东省广州市白云区中考一模化学试题原卷版doc等2份试卷配套教学资源,其中试卷共35页, 欢迎下载使用。
2022年广东省广州市白云区中考二模化学试题(word版含答案): 这是一份2022年广东省广州市白云区中考二模化学试题(word版含答案),共11页。试卷主要包含了单选题,填空题,流程题,实验题,科学探究题等内容,欢迎下载使用。












