





2021届高考化学三轮复习专项冲刺:有机实验(二)课件PPT
展开1. 有机物分离提纯的方法蒸馏(分馏)法、萃取法、(洗涤)分液法、过滤、洗气法、渗析、 盐析、 重结晶法有机物提纯的三种常用方法:蒸馏(分馏)法、(洗涤)分液法、 洗气法、
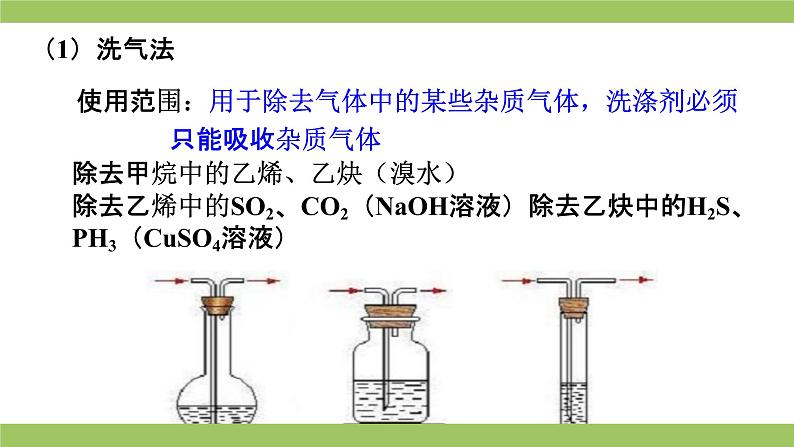
(1)洗气法使用范围:用于除去气体中的某些杂质气体,洗涤剂必须只能吸收杂质气体除去甲烷中的乙烯、乙炔(溴水)除去乙烯中的SO2、CO2(NaOH溶液)除去乙炔中的H2S、PH3(CuSO4溶液)
除去硝基苯中的残酸(NaOH溶液)除去溴苯中的溴(NaOH溶液)除去乙酸乙酯中的乙酸—(饱和碳酸钠溶液)除去苯中的苯酚(NaOH溶液)除去苯中的甲苯(酸性高锰酸钾溶液)除去苯酚中的苯甲酸(NaOH溶液通CO2)
用于除去某些液体中的杂质(有时分液前要加
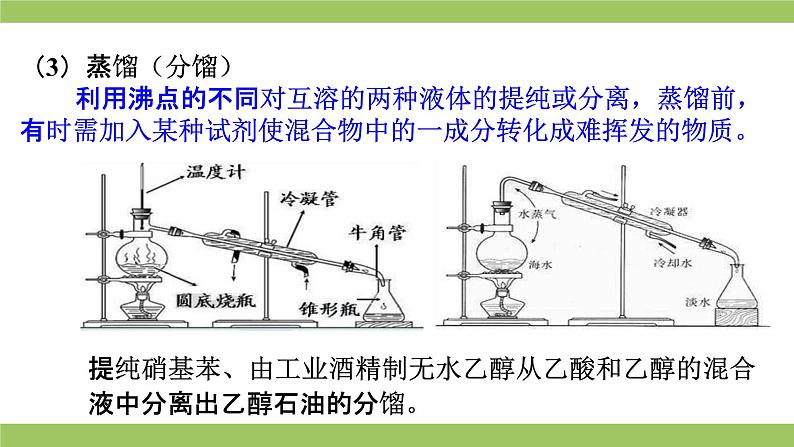
提纯硝基苯、由工业酒精制无水乙醇从乙酸和乙醇的混合液中分离出乙醇石油的分馏。
(3)蒸馏(分馏) 利用沸点的不同对互溶的两种液体的提纯或分离,蒸馏前,有时需加入某种试剂使混合物中的一成分转化成难挥发的物质。
盐析:除去肥皂中的甘油和过量碱渗析:除去淀粉中的少量葡萄糖或者NaCl
1、有机物鉴别常用的方法(1)有机物的溶解性和密度①易溶于水:低级醇、醛、羧酸、有机钠盐、乙二醇、丙三醇;且同系物随碳原子数目增加,溶解性降低;含-OH-COOH、-CHO数目越多,越易溶于水。②难溶于水,比水轻:烃、一氯(氟)代物、酯;③难溶于水,比水重:大多数卤代烃(溴苯,四氯化碳,溴乙烷等)、硝基苯 。
(2)有机物的燃烧情况① 是否可燃:大部分有机物可燃,除CCl4②燃烧时产生黑烟:如:区分乙烷、乙烯和乙炔③ 燃烧气味:如:区分蛋白质和纤维素(3)根据有机物官能团性质
水、溴水、KMnO4、新制Cu(OH)2、银氨溶液、NaOH、NaHCO3、碘水、浓硝酸、Fe3+
2、几种重要有机物的检验
1)步骤(含试剂):(1)取少量卤代烃(溴乙烷),(2)加氢氧化钠溶液,(3)充分振荡或加热, (4)冷却,(6)加硝酸银溶液,2)现象:若产生白色(淡黄色、黄色)沉淀。3)结论:有-Cl、(-Br、-I)。
3、卤代烃中卤素原子的检验:
4、烯醛中碳碳双键的检验:
(1)若是纯净的液态样品(无水):取样—加入溴的四氯化碳溶液—若褪色即可证明(2)若是水溶液:取样—加入足量的银氨溶液或新制氢氧化铜悬浊液,加热— 冷却(过滤)—加入硝酸酸化,再加入溴水—若褪色即可证明
5、二糖或多糖水解产物的检验:
—若二糖或多糖是在稀硫酸作用下水解检验方法: 取样,加稀硫酸加热一定时间—向水解液中加入足量NaOH溶液中和至碱性—再加入银氨溶液或新制氢氧化铜悬浊液,加热,观察现象6、溶解在苯中的苯酚的检验:检验方法: 取样,向试样中加入NaOH溶液—振荡,静置分液—向水溶液中加入盐酸酸化,再滴入几滴氯化铁溶液(饱和溴水)— 若溶液呈紫色(产生白色沉淀)即可证明。
1.(2020·陕西省渭南中学高三模拟)锡为ⅣA族元素,四碘化锡是常用的有机合成试剂(SnI4,熔点:144.5 ℃,沸点:364.5 ℃,易水解)。实验室以过量锡箔为原料通过反应Sn+2I2 SnI4制备SnI4。下列说法错误的是A.装置Ⅱ的主要作用是吸收挥发的I2B.SnI4可溶于CCl4中C.装置Ⅰ中a为冷凝水进水口D.加入碎瓷片的目的是防止暴沸
解析 SnI4易水解,装置Ⅱ的主要作用是防止空气中的水蒸气进入到反应装置中,故A错误;根据相似相溶原理,SnI4是非极性分子,可溶于CCl4中,故B正确;冷凝水方向是“下进上出”,因此装置Ⅰ中a为冷凝水进水口,故C正确;液体加热时易暴沸,因此需要加入碎瓷片,故D正确。
2.对实验室制得的粗溴苯[含溴苯(不溶于水,易溶于有机溶剂,沸点:156.2 ℃)、Br2和苯(沸点:80 ℃)]进行纯化,未涉及的装置是
解析 除去Br2可以用SO2,原理是:Br2+SO2+2H2O===H2SO4+2HBr,故A正确;分液可得苯和溴苯的混合液,故B正确;该实验不涉及过滤操作,故C错误;溴苯的沸点是156.2 ℃、苯的沸点是80 ℃,溴苯和苯用蒸馏法分离,故D正确。
3.在提纯粗苯甲酸(C6H5—COOH,常温下为晶体)过程中,下列操作未涉及的是
解析 提纯粗苯甲酸(C6H5—COOH,常温下为晶体)的步骤为:①将粗苯甲酸充分溶解于少量热水中,用到C装置;②将溶液蒸发浓缩得到苯甲酸的饱和溶液,用到装置D;然后趁热过滤,除去不溶性杂质,用到B装置;③滤液冷却结晶,滤出晶体;④洗涤晶体。并未涉及A操作,因此选A。
4.下列实验室制取乙烯、除杂质、性质检验、收集的装置和原理正确的是
解析 温度计没有插入液面下,故A错误;实验室制取乙烯时会产生杂质乙醇、SO2、CO2和H2O,SO2、乙醇和乙烯均可以使酸性高锰酸钾溶液褪色,故B错误;乙烯能使溴的四氯化碳溶液褪色,故C正确;乙烯的密度和空气相近,不能用排空气法收集,故D错误。
5.下列实验装置图正确的是
解析 乙烯密度稍小于空气,应该采用向下排空气法收集,但因为乙烯不易溶于水且乙烯密度接近空气密度,最好采用排水法收集,故A错误;分馏时,温度计测量馏分温度,水银球应该位于蒸馏烧瓶支管口处,且进、出水口错误,故B错误;实验室用苯和浓硝酸在浓硫酸作催化剂、加热50~60 ℃制备硝基苯,该实验操作正确,故C正确;实验室制取乙酸乙酯时,导气管不能伸入饱和碳酸钠溶液中,否则易产生倒吸现象,故D错误。
(2020·课标全国Ⅱ,27)苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
实验步骤:(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 ml)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。(3)纯度测定:称取0.122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25.00 mL溶液,用0.010 00 ml·L-1的KOH标准溶液滴定,三次滴定平均消耗21.50 mL的KOH标准溶液。
回答下列问题:(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为________(填字母)。A.100 mL B.250 mL C.500 mL D.1 000 mL(2)在反应装置中应选用________冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完成,其判断理由是________________________。(3)加入适量饱和亚硫酸氢钠溶液的目的是____________________________________________________________________________;该步骤亦可用草酸在酸性条件下处理,请用反应的离子方程式表达其原理_________________________________________________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是________。(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是_________________________________________________。(6)本实验制备的苯甲酸的纯度为________;据此估算本实验中苯甲酸的产率最接近于________(填字母)。A.70% B.60% C.50% D.40%(7)若要得到纯度更高的苯甲酸,可通过在水中________的方法提纯。
2021届高考化学三轮复习专项冲刺:综合实验探究(第二课时)课件PPT: 这是一份2021届高考化学三轮复习专项冲刺:综合实验探究(第二课时)课件PPT,共25页。PPT课件主要包含了考点3,典例分析,考点4,能力提升等内容,欢迎下载使用。
2021届高考化学三轮复习专项冲刺:综合实验(一)课件PPT: 这是一份2021届高考化学三轮复习专项冲刺:综合实验(一)课件PPT,共26页。PPT课件主要包含了实验综合题特点,考情预测,常见的量气装置,实验综合题常见考查点等内容,欢迎下载使用。
2021届高考化学三轮复习专项冲刺:综合实验(三)课件PPT: 这是一份2021届高考化学三轮复习专项冲刺:综合实验(三)课件PPT,共35页。PPT课件主要包含了实验综合题常见考查点,分析模型,明确题型,了解原理,物质制备分离型,性质原理探究型,定量分析型,装置功能各步骤分目的,实验目的方法,物质结构性质等内容,欢迎下载使用。












