

所属成套资源:2022届中考化学一轮复习理重点、攻难点专项特训(含解析)
(2)自然界的水——2022届中考化学一轮复习理重点、攻难点专项特训
展开
这是一份(2)自然界的水——2022届中考化学一轮复习理重点、攻难点专项特训,共12页。试卷主要包含了5时杀菌效果比pH=6,水在化学实验中有重要作用等内容,欢迎下载使用。
1.2019年3月19日,联合国水机制组织发布《2019年世界水资源发展报告》,主题为“不让一个人掉队”,提出改进水资源管理、获得充足的供水和卫生服务对解决各种社会、经济不平等现象至关重要。以下有关于水资源相关描述正确的是( )
A.地球表面的约70.8%被水覆盖,可利用的淡水资源所占比例也很大
B.只要是澄清透明的水就可以不经过任何处理直接饮用,非常安全
C.水体富营养化指的是水体中氮、磷等元素含量过多而引起的水质污染现象,为了避免出现水体富营养化,生活中应当禁用含磷洗衣粉
D.工业三废的随意排放是导致水体污染的重要因素之一,为了保护水资源,应当禁止所有工厂排放任何废弃物
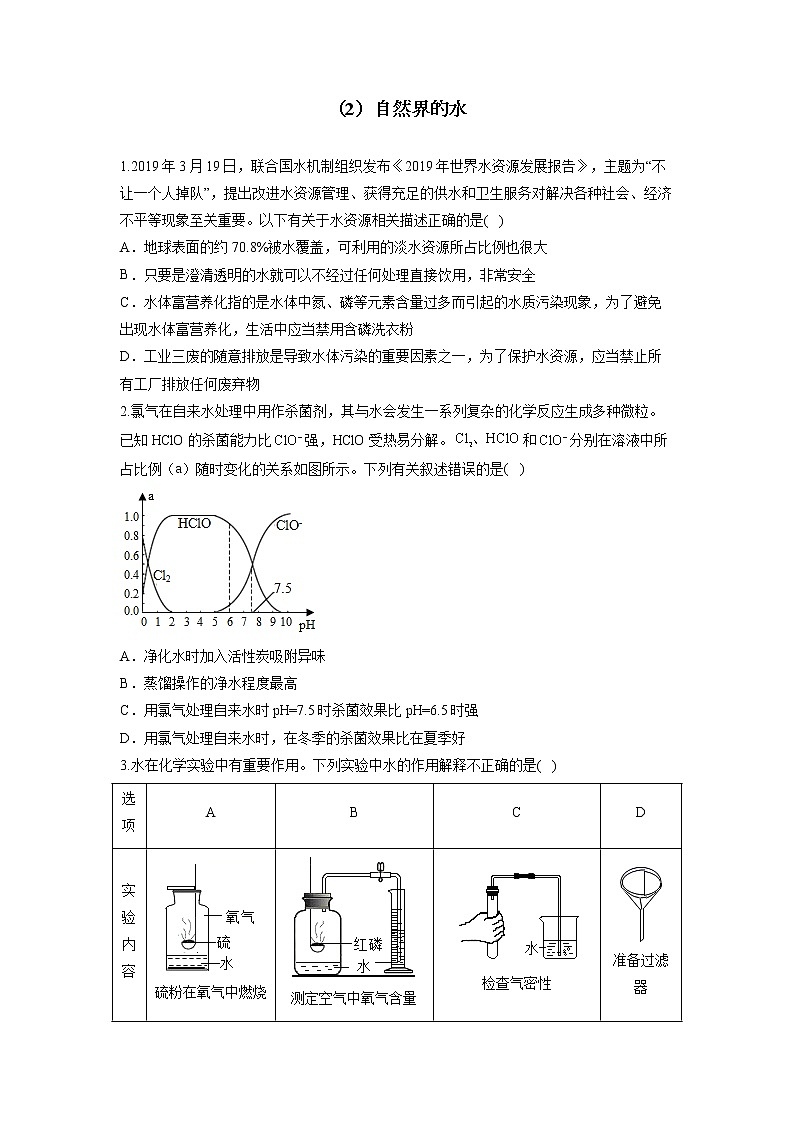
2.氯气在自来水处理中用作杀菌剂,其与水会发生一系列复杂的化学反应生成多种微粒。已知HClO的杀菌能力比强,HClO受热易分解。和分别在溶液中所占比例(a)随时变化的关系如图所示。下列有关叙述错误的是( )
A.净化水时加入活性炭吸附异味
B.蒸馏操作的净水程度最高
C.用氯气处理自来水时pH=7.5时杀菌效果比pH=6.5时强
D.用氯气处理自来水时,在冬季的杀菌效果比在夏季好
3.水在化学实验中有重要作用。下列实验中水的作用解释不正确的是( )
A.AB.BC.CD.D
4.自来水消毒过程中常会发生甲、乙两个化学反应.其反应的微观过程可用图表示:
下列说法正确的是( )
A.物质a、d都是氧化物B.气体b不能用排水法收集
C.物质c的溶液pH 大于7D.气体e具有可燃性
5.水在电离时会产生水合离子,我们称这种水为离子水,其本质还是水,除了电子得失和物理、化学性质发生极大变化外不添加任何物质。离子水的分子团小,溶解度大,渗透力强,直接饮用,口感极好,下列关于离子水的说法正确的是( )
A.离子水中的分子间没有间隙
B.离子水由氢、氧两种元素组成
C.离子水中的分子不运动
D.离子水带电,因此不能饮用
6.氢气在氧气中燃烧后生成水,下列说法错误的是( )
A.该反应中,分子种类发生了改变
B.该反应中,原子种类没有发生改变
C.氢气、氧气和水都是由分子构成的
D.该反应能说明水是由氢气和氧气构成的
7.兴趣小组使用石墨电极进行电解水实验(如图),添加增强水的导电性,添加后形成饱和溶液。连接电源,除两极有气泡产生外,正极附近还出现明显的白色浑浊。这一“异常”现象中白色不溶物形成原因不可能是( )
(查阅资料:电解过程中溶液的温度会升高。氢氧化钙的溶解度随温度升高而减小)
A.电解过程中,水的减少导致白色浑浊
B.电解过程中,水温上升导致白色浑浊
C.空气中的二氧化碳溶于水,与溶液反应导致白色浑浊
D.石墨电极含碳元素,电解过程中石墨电极与正极生成的反应生成导致的
8.某同学在水电解器中加入含酚酞的稀溶液(溶液呈中性且不参与反应),至充满管A和管B。通直流电一段时间后现象如下图所示,电解结束后将容器内所有液体倒入烧杯中,溶液呈无色。下列说法的是( )
A.硫酸钠在水中解离出和,可增强导电性
B.电解过程中化学能转化为电能
C.电解过程中,电极M附近产生的微粒有和
D.管A中的气体与管B中的气体体积比1:2
9.从2021年1月1日起重庆沿江各区县正式实施长江流域重点水域“十年禁渔”,此举是对长江生态系统保护具有历史意义的重要举措,让长江休养生息,以期实现长江母亲河两岸青山鱼翔浅底的美好画卷。下列关于水的相关说法中正确的是( )
A.向硬水中加明矾净水剂后得到纯水
B.工厂废水处理后循环使用
C.蒸馏水含有人体所需的矿物质和多种维生素
D.自来水需经过煮沸才能饮用,水沸腾变为水蒸气时,水分子种类发生改变
10.下列与水相关的说法不正确的是( )
A.在水中加入明矾的目的是吸附水中悬浮小颗粒形成大颗粒而沉降起到净水作用
B.为了增强水的导电性通常在水中加入氢氧化钠
C.生产自来水的过程中用氯气杀菌消毒是物理变化
D.蒸馏是净化程度最高的净水方法
11.将20g、的混合气体点燃,完全反应后生成18g水,则原混合物中和的质量比可能是( )
A.2:1B.1:8C.1:10D.1:4
12.如图是污水处理流程图,下列说法不正确的是( )。
A.“格栅”相当于基本操作中的溶解
B.一级处理中只发生了物理变化
C.二级处理中将有机物转化为无机物
D.消毒处理可除去水中的微生物
13.水是一种重要的资源,人类生活离不开水。
(1)自来水厂的净水流程如下:
①沉淀池中常用的絮凝剂是_______(填“名称”);吸附池中加入活性炭,是利其_______性;
②过滤池中利用了过滤操作。实验室进行过滤操作时,需用到的玻璃仪器有_______;过滤前需充分静置,然后先将上层清液转入过滤器中,这样做的好处是_______;
③向清水池中通入氯气杀菌消毒,此过程中发生了反应:,X的化学式为_____。
(2)下列甲是制备蒸馏水的装置,乙是电解水的装置,丙是电解水的微观示意图,请回答下列问题。
④甲图中水从A经B转移到C的过程中,水分子的组成没有发生变化,发生变化的是_______;
⑤乙图中,a管中产生的气体是_______,检验b管中气体的方法是_______;当b中气体的分子数目为n时,a中气体的分子数目为_______;
⑥丙图中,发生改变的粒子是_______(填“符号”,下同),没有变化的粒子是_______,该反应的化学方程式为_______。
(3)下列实验能证明水是由氧元素和氢元素组成的是______(填字母序号)。
A.水的电解
B.水的蒸馏
C.水的净化
D.氢气在氧中燃烧
(4)2020年,我国纪念“世界水日”和“中国水周”的宣传主题是“坚持节水优先,建设幸福河湖”。请写出节约用水的一种具体做法_______。
14.水是一种宝贵的自然资源,自来水厂的净水流程如下:
请回答下列问题:
(1)吸附池内常用_______吸附色素和异味。
(2)自来水厂常用氯气消毒,该过程发生的是_______(填“物理变化”或“化学变化”)。
(3)小宇同学用如图过滤装置对天然水进行处理,图中玻璃棒的作用是_______,发现得到的滤液仍然浑浊,则可能的原因是_______。
(4)小宁同学为了比较不同水样的硬度,用四种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
(解释与结论)硬度最大的水样是 _______。由上述实验可知,在日常生活中,能将自来水硬度降低的方法有 _______。
(5)小宁同学继续实验,发现山泉水的硬度大于自来水的硬度,其实验方案为_______。
(6)科学家们用“电解法”证明了水的组成(装置如图所示,电极不与水及生成的气体反应)。
①电解时,水中需加入少量的NaOH溶液, 其作用是_______。
②写出电解水反应文字表达式:_______。
③与电源两极相连的两端,乙量筒中收集到的气体是_______(填化学式),若乙量筒中收集了10mL气体,则甲量筒中收集的气体体积是_______。该实验说明水是由_______组成的。
15.兴趣小组进对电解水过程中发现的“异常”现象进行探究。
兴趣小组使用石墨电极进行电解水实验,添加增强水的导电性。添加后形成饱和溶液。连接电源,除两极有气泡产生外,正极附近还出现明显的白色浑浊。兴趣小组的的同学们对这“异常”现象中白色不溶物的成分和形成原因进行探究。
查阅资料:电解过程中溶液的温度会升高。
(1)兴趣小组同学首先排除溶于水中的,导致白色浑浊,原因是________。
(2)兴趣小组同学提出不同猜想,并设计相关实验进行验证。
①同学甲:取与上述实验相同体积的饱和溶液于烧杯中,加热至电解时上升的温度,观察到溶液中没有明显的浑浊现象,该实验目的是________。
②同学乙:认为可能是水的减少导致白色浑浊。设计验证该猜想的实验操作方案________。
③同学丙:认为可能是采用石墨电极电解导致白色浑浊。该同学用铂电极替代石墨电极重复上述实验,一段时间后溶液没有出现浑浊。根据这一现象,推测该白色不溶物可能是。为进一步验证不溶物的成分:
i.可用_______操作分离出不溶物;
ii.设计方案并实验:_________(填操作现象),证明白色不溶物中含有碳酸根;
iii.根据同学丙的实验,推测电解过程出现浑浊的主要原因:__________。
答案以及解析
1.答案:C
解析:A、地球表面约70.8%被水覆盖,淡水只约占全球水储量的2.53%,且可利用的淡水资源所占比例很小,应节约用水,不符合题意;
B、澄清透明的水中还含有可溶性杂质,因此不经过任何处理的水不能直接饮用,不符合题意;
C、水体富营养化指的是水体中氮、磷等元素含量过多,而引起的水质污染现象,为了避免出现水体富营养化,生活中应当禁用含磷洗衣粉,从而保护水资源,符合题意;
D、工业三废的随意排放是导致水体污染的重要因素之一,为了保护水资源,应当将废弃物处理达标后排放,而不是禁止所有工厂排放任何废弃物,不符合题意。
故选C。
2.答案:C
解析:A、净化水时加入活性炭吸附异味,因为活性炭的吸附作用,故A不符合题意;
B、蒸馏操作可得到纯净水,所以说蒸馏操作的净水程度最高,故B符合题意;
C、起杀菌作用较强的是HClO,由图象可知pH=6.5时,HClO的浓度要比pH=7.5时要大,HClO浓度越大,杀菌效果好,所以pH=7.5时杀菌效果比pH=6.5时弱。故C不符合题意;
D、夏季相比冬季温度高,HClO易分解,所以杀菌效果不如冬季,故D不符合题意;
3.答案:A
解析:A、硫燃烧生成二氧化硫,二氧化硫有毒,扩散到空气中污染空气,加入适量水,是为了吸收二氧化硫,防止污染空气,该选项说法不正确;
B、测定空气中氧气含量实验中,红磷燃烧消耗氧气,瓶内压强减少,冷却到室温,打开止水夹,量筒中水会进入集气瓶,所以量筒中加入适量水,通过水体积的变化得出空气中的体积,该选项说法正确;
C、检查装置气密性实验中,加入适量水,形成密闭系统,用于观察现象检查装置是否漏气,选项说法正确;
D、过滤器制作时,用水润湿,使滤纸紧贴漏斗内壁,以提高过滤速率,选项说法正确。
故选A。
4.答案:B
解析:根据氧原子、氢原子和氯原子的模型判断出:a是水分子;b是氯分子;c是氯化氢分子(HCl);d是次氯酸分子(HClO);e是氧分子。物质d即次氯酸(HClO),不是氧化物,而是酸,故A错误;由图可知,气体b为氯气,与水反应,故不能用排水法收集,故B正确;物质c易溶于水,其水溶液是盐酸,溶液pH小于7,故C错误;由于E物质为氧气,具有助燃性,但无可燃性,故D错误。
5.答案:B
解析:A、离子水中的分子间有间隙;故选项错误。
B、离子水由氢、氧两种元素组成;故选项正确。
C、离子水中的分子在不停的运动;故选项错误。
D、离子水带电,但可以直接饮用;故选项错误。
故选B。
6.答案:D
解析:该反应能说明水是由氧元素和氧元素组成的。
7.答案:C
解析:A、添加后形成饱和溶液,电解过程中,水的减少导致氢氧化钙析出形成白色浑浊,正确;
B、氢氧化钙的溶解度随温度升高而减小,电解过程中溶液的温度会升高,导致氢氧化钙析出,形成白色浑浊,正确;
C、空气中的二氧化碳含量很低,不会与溶液反应导致白色浑浊,如果导致浑浊则正、负均会出现浑浊,错误;
D、石墨电极含碳元素,电解过程中石墨电极与正极生成的反应生成,二氧化碳和氢氧化钙反应生成碳酸钙沉淀,导致浑浊,正确。
故选C。
8.答案:B
解析:A、硫酸钠在水中解离出和,自由离子增加,可增强导电性,选项A正确;
B、电解过程中不是化学能转化为电能,而是电能转化为化学能,选项B错;
C、电解过程中,电极M连接的是正极,所以附近产生的微粒有,电极N附近溶液显红色,说明溶液呈碱性,电解结束后将容器内所有液体倒入烧杯中,溶液呈无色,说明电极M溶液中呈酸性,所以电极M附近产生的微粒有,选项C正确;
D、管A中的气体是氧气,管B中的气体是氢气,氧气与氢气的体积比是1:2,所以管A中的气体与管B中的气体体积比1:2,选项D正确;
故选:B。
9.答案:B
解析:A、向硬水中加明矾净水剂只能吸附水的细小颗粒,不能除去水中可溶性的杂质,不能得到纯水,错误;
B、工厂废水处理后循环使用,可减少污染,节约水资源,正确;
C、蒸馏水中只有水,不含有人体所需的矿物质和多种维生素,错误;
D、自来水需经过煮沸才能饮用,水沸腾变为水蒸气时,水分子的间隔变大,水分子种类不发生改变,错误。
故选:B。
10.答案:C
解析:A、明矾溶于水形成胶状物,能吸附水中悬浮小颗粒形成大颗粒而沉降起到净水作用,正确。
B、纯水几乎不导电,为了增强水的导电性通常在水中加入氢氧化钠,正确。
C、生产自来水的过程中用氯气杀菌消毒有新物质生成,是化学变化。错误。
D、蒸馏可以除去水中的可溶性杂质,是净化程度最高的净水方法,正确。
故选C。
11.答案:D
解析:设生成18g水,需要氧气的质量为,生成氢气的质量为。
=2g
=16g
剩余气体的质量为:20g-18g=2g
当剩余气体是氧气时,原混合物中和的质量比为:2g:(16g+2g)=1:9;
当剩余气体是氢气时,原混合物中和的质量比为:(2g+2g):16g=1:4。
故选:D。
12.答案:A
解析:过滤是把不溶性固体与液体分开的一种方法,“格栅”可除去水中大块悬浮物,相当于化学实验操作中的过滤。
13.答案:(1)明矾;吸附;烧杯、漏斗、玻璃棒;加快过滤速率,防止滤纸破损;HClO
(2) 分子之间的间隔;氢气;将带火星的木条伸入b中,木条复燃则为氧气;2n;;H、O;
(3)AD
(4)用洗菜水浇花等
解析:(1)①沉淀池中常用的絮凝剂是明矾。吸附池中加入活性炭是利用其吸附性,活性炭疏松多孔可以吸附带有颜色和异味的物质。②过滤需要用到的玻璃仪器有烧杯、漏斗、玻璃棒。过滤前充分静置,可以让一些大颗粒杂质沉淀,然后一些颗粒小的固体进行过滤除去,可以加快过滤速率,防止滤纸破损。
③反应前后原子的种类和个数不变,反应前后除X外相差1个H、1个Cl,1个O,所以X是HClO。
(2)④水加热变成水蒸气后水蒸气冷凝变为水,这个过程中水分子的种类没有变化,变化的是分子之间的间隔。⑤水通电分解,正极产生的是氧气,负极产生的是氢气。所以a为氢气。b为氧气,氧气的检验方法是将带火星的木条伸入b中,木条复燃则为氧气。生成氢气和氧气的体积比为2:1,则生成氢气和氧气的分子个数比为2:1,所以当b中气体的分子数目为n时,a中气体的分子数目为2n。⑥该反应中水分子分解,发生改变,符号为。化学变化中原子种类不变,氢氧原子不变,符号为H、O。电解水的化学方程式为。
(3)电解水实验和氢气燃烧实验可以证明水是由氧元素和氢元素组成的,故选AD。
(4)节约用水的具体做法有用洗菜水浇花等,合理即可。
14.答案:(1)活性炭
(2)化学变化
(3)引流;滤纸破损(或液面高于滤纸的边缘或接收滤液的烧杯不干净)
(4)湖水;煮沸
(5)分别为取5mL山泉水、自来水,加肥皂水,记录观察到泡沫产生时所需肥皂水的用量,若自来水大于自来水所需肥皂水量,说明山泉水硬度大于自来水
(6) 增强导电性;;氢气;5mL;氢元素和氧元素
解析:(1)活性炭具有吸附性,吸附池内常用活性炭吸附色素和异味;
(2)自来水厂常用氯气消毒,能杀死水中的微生物,该过程中有新物质生成,发生的是化学变化;
(3)过滤操作中,玻璃棒的作用是引流,发现得到的滤液仍然浑浊,则可能的原因是滤纸破损(或液面高于滤纸的边缘或接收滤液的烧杯不干净);
(4)硬度越大,观察到泡沫产生时所需肥皂水的用量越大,故硬度最大的水样是湖水;由表中数据可知,煮沸后的自来水相对于自来水,观察到泡沫产生时所需肥皂水的用量减小,硬度减小,故煮沸可以降低自来水硬度;
(5)小宁同学继续实验,发现山泉水的硬度大于自来水的硬度,仿照题中方法,其实验方案为分别为取5mL 山泉水、自来水,加肥皂水,记录观察到泡沫产生时所需肥皂水的用量,若自来水大于自来水所需肥皂水量,说明山泉水硬度大于自来水;
(6)①电解时,水中需加入少量的 NaOH溶液, 其作用是增强导电性;②电解水时生成氢气和氧气,反应文字表达式:;③电解水时,正极产生氧气,负极产生氢气,体积比为1:2。与电源两极相连的两端,乙量筒中收集到的气体体积较大是氢气,化学式为:H2;若乙量筒中收集了10mL气体,则甲量筒中收集的气体体积是5mL。 氢气是由氢元素组成,氧气是由氧元素组成,化学变化中元素的种类不变,该实验说明水是由氢元素和氧元素组成的。
15.答案:(1)若为溶于水中的,导致白色浑浊,则一开始就会出现浑浊,而不是电解后出现浑浊
(2)探究温度升高能否导致白色浑浊;取与上述实验相同体积的饱和氢氧化钙溶液,蒸发出于上述实验相同量的水,再冷却至室温,观察溶液中是否出现明显的浑浊;过滤;取不溶物加稀盐酸,不溶物溶解且产生气体,生成气体通入澄清石灰水,石灰水变浑浊;石墨电极中碳与正极生成的氧气反应生成二氧化碳,生成的二氧化碳与石灰水反应生成碳酸钙沉淀
解析:(1)若为溶于水中的,导致白色浑浊,则一开始就会出现浑浊,而不是电解后出现浑浊;
(2)①同学甲:取与上述实验相同体积的饱和溶液于烧杯中,加热至电解时上升的温度,观察到溶液中没有明显的浑浊现象,该实验目的是探究温度升高能否导致白色浑浊;②设计验证可能是水的减少导致白色浑浊,可以通过减少水的量进行观察;实验操作方案可以为:取与上述实验相同体积的饱和氢氧化钙溶液,蒸发出于上述实验相同量的水,再冷却至室温,观察溶液中是否出现明显的浑浊;③i.过滤是分离固液的操作,可用过滤操作分离出不溶物;ii.碳酸根离子可以和酸反应生成使澄清石灰水变浑浊的二氧化碳气体;故设计方案为:取不溶物加稀盐酸,不溶物溶解且产生气体,生成气体通入澄清石灰水,石灰水变浑浊,证明白色不溶物中含有碳酸根;iii.根据实验,电解过程出现浑浊的主要原因:石墨电极中碳与正极生成的氧气反应生成二氧化碳,生成的二氧化碳与石灰水反应生成碳酸钙沉淀。
选项
A
B
C
D
实验内容
硫粉在氧气中燃烧
测定空气中氧气含量
检查气密性
准备过滤器
水的作用
集气瓶中的水:吸收热量,防止集气瓶炸裂
量筒中的水:通过体积变化得出空气中氧气的体积
烧杯中的水形成密闭系统,用于观察现象,检查装置是否漏气
用洗瓶挤少量水,让滤纸紧贴漏斗内壁
实验操作
水样
肥皂水用量/滴
市售纯净水
2
煮沸后的自来水
6
自来水
9
湖水
14
相关试卷
这是一份(12)化学与生活——2022届中考化学一轮复习理重点、攻难点专项特训,共12页。试卷主要包含了民以食为天,下列有关油脂的叙述正确的是,化学与生产生活关系密切等内容,欢迎下载使用。
这是一份(11)化学方程式——2022届中考化学一轮复习理重点、攻难点专项特训,共13页。试卷主要包含了已知某纯净物4,对于方程式的意义或读法正确是,已知,对于已经配平的化学方程式,取7等内容,欢迎下载使用。
这是一份(7)盐 化肥——2022届中考化学一轮复习理重点、攻难点专项特训,共13页。试卷主要包含了下列物质的主要成分不属于盐的是,下列实验不能成功的是,下列说法错误的是等内容,欢迎下载使用。








