
高中化学苏教版 (2019)选择性必修1第三单元 金属的腐蚀与防护课时练习
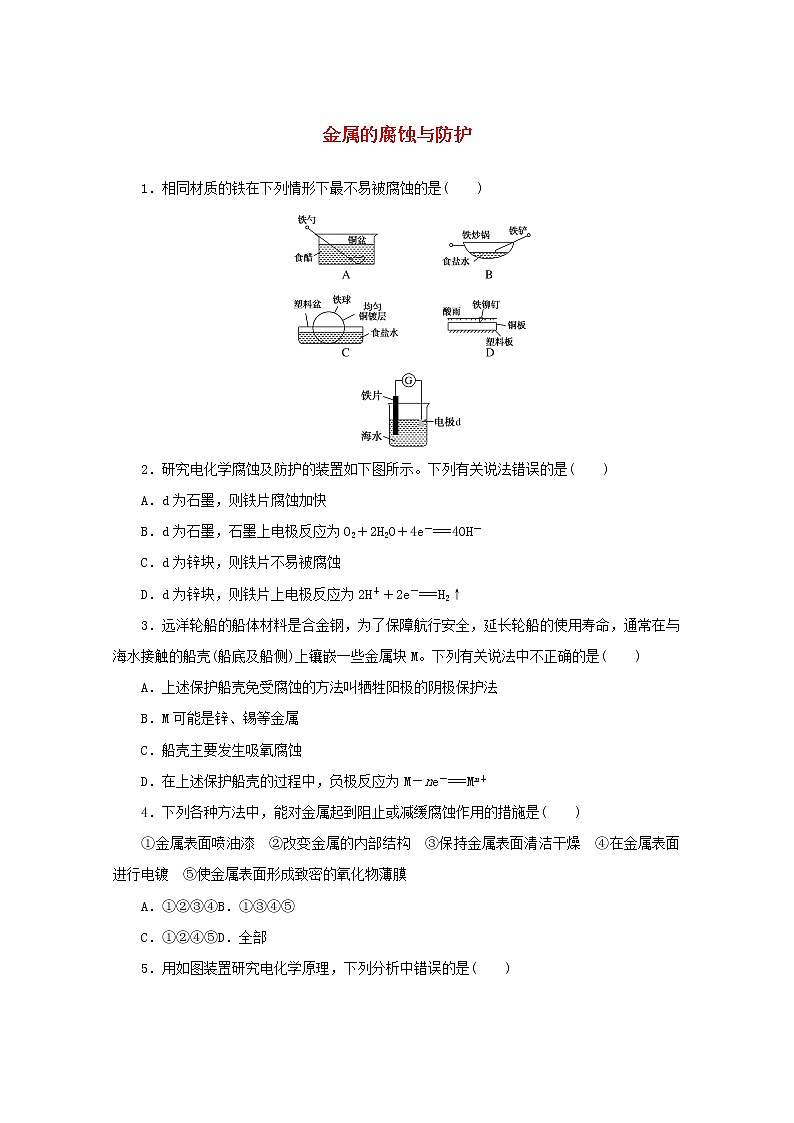
展开2.研究电化学腐蚀及防护的装置如下图所示。下列有关说法错误的是( )
A.d为石墨,则铁片腐蚀加快
B.d为石墨,石墨上电极反应为O2+2H2O+4e-===4OH-
C.d为锌块,则铁片不易被腐蚀
D.d为锌块,则铁片上电极反应为2H++2e-===H2↑
3.远洋轮船的船体材料是合金钢,为了保障航行安全,延长轮船的使用寿命,通常在与海水接触的船壳(船底及船侧)上镶嵌一些金属块M。下列有关说法中不正确的是( )
A.上述保护船壳免受腐蚀的方法叫牺牲阳极的阴极保护法
B.M可能是锌、锡等金属
C.船壳主要发生吸氧腐蚀
D.在上述保护船壳的过程中,负极反应为M-ne-===Mn+
4.下列各种方法中,能对金属起到阻止或减缓腐蚀作用的措施是( )
①金属表面喷油漆 ②改变金属的内部结构 ③保持金属表面清洁干燥 ④在金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜
A.①②③④B.①③④⑤
C.①②④⑤D.全部
5.用如图装置研究电化学原理,下列分析中错误的是( )
6.如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是( )
A.a中铁钉附近呈现红色
B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应
D.b中铝条附近有气泡产生
7.宝鸡被誉为“青铜器之乡”,出土了大盂鼎、毛公鼎、散氏盘等五万余件青铜器。研究青铜器(含Cu、Sn等)在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图,下列说法不正确的是( )
A.青铜器发生电化学腐蚀,图中c做负极,被氧化
B.正极发生的电极反应为O2+4e-+2H2O===4OH-
C.环境中的Cl-与正、负两极反应的产物作用生成a的离子方程式为2Cu2++3OH-+Cl-===Cu2(OH)3Cl↓
D.若生成0.2mlCu2(OH)3Cl,则理论上消耗的O2体积为4.48L
8.某校活动小组为探究金属腐蚀的相关原理,设计了如下装置(图a),图a的铁棒末端分别连一块Zn片和Cu片,并静置于含有K3[Fe(CN)6]及酚酞的混合凝胶上。一段时间后发现凝胶的某些区域发生了变化(图b)。已知Fe2+能与K3[Fe(CN)6]形成蓝色沉淀。下列说法错误的是( )
A.甲区发生的电极反应式:Fe-2e-===Fe2+
B.乙区产生Zn2+
C.丙区呈现红色
D.丁区呈现蓝色
9.溶液pH对含有碳杂质的金属铝的腐蚀影响关系如下图,下列说法中正确的是( )
A.pH越大,金属铝的腐蚀一定越严重
B.电解液的pH=9.5时,可发生原电池反应,负极反应为Al-3e-===Al3+
C.可用电解法在金属铝表面生成保护膜,其原理为2Al+3H2Oeq \(=====,\s\up7(电解))Al2O3+3H2↑
D.铝制餐具应该经常打磨以保持餐具光亮如新
10.铁碳微电解技术是利用金属电化学腐蚀原理处理酸性污水的一种工艺,装置如图所示。若上端开口关闭,可得到强还原性的H·(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的·OH(羟基自由基)。下列说法错误的是( )
A.无论是否鼓入空气,负极的电极反应式均为Fe-2e-===Fe2+
B.不鼓入空气时,正极的电极反应式为H++e-===H·
C.鼓入空气时,每生成1ml·OH,有2ml电子发生转移
D.处理含有草酸(H2C2O4)的污水时,上端开口应打开并鼓入空气
11.炒菜的铁锅不用时会因腐蚀而出现红褐色锈斑,其腐蚀原理如图所示。下列说法正确的是( )
A.腐蚀过程中,负极是C
B.Fe失去电子经电解质溶液转移给C
C.正极的电极反应式为4OH--4e-===2H2O+O2↑
D.每生成1ml铁锈(Fe2O3·nH2O)理论上消耗标准状况下的O233.6L
12.回答下列问题:
(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化学腐蚀称为________。
②图中A、B、C、D四个区域,生成铁锈最多的是________(填字母)。
③以锌为负极,采用牺牲阳极的阴极保护法防止铁闸的腐蚀,图中锌块的固定位置最好应在________处(填字母)。
(2)石墨可用于自然水体中铜件的电化学防腐,完成下面防腐示意图,并作相应标注:
(3)如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是________(填字母)。
A.K1闭合,铁棒上发生的反应为2H++2e-===H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001ml气体
13.铁生锈是比较常见的现象,某实验小组为研究铁生锈的条件,设计了如图所示的快速、易行的实验:
首先检查制取氧气装置的气密性,然后按图所示连接好装置,点燃酒精灯,持续3min左右,观察到的实验现象:①硬质玻璃管中干燥的团状细铁丝表面依然光亮,没有发生腐蚀;②硬质玻璃管中潮湿的团状细铁丝表面颜色变灰暗,发生腐蚀;③烧杯中潮湿的团状细铁丝表面依然光亮。
试回答下列问题:
(1)根据与金属接触的介质不同,金属腐蚀可分成不同类型,本实验中铁生锈属于________,能表示其原理的电极反应为________________________________________________________________________
________________________________________________________________________。
(2)仪器A的名称为________,其中装的药品可以是________,其作用是________________________________________________________________________。
(3)由实验可知,铁生锈的条件为________________________________________________________________________
________________________________________________________________________。
决定铁生锈快慢的一个重要因素是________________________________________________________________________。
14.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
(2)编号①实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了________腐蚀,请在图3中用箭头标出发生该腐蚀时电子的流动方向;此时,碳粉表面发生了__________(填“氧化”或“还原”)反应,其电极反应式是________________________________________________________________________。
(3)该小组对图2中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:________________________________________________________________________;
……
课时作业7 金属的腐蚀与防护
1.解析:A项,食醋是电解质溶液,铁勺和铜盆是相互接触的两种金属,形成原电池,铁是活泼金属,作负极,铁易被腐蚀;B项,食盐水是电解质溶液,铁炒锅和铁铲都是铁碳合金,符合原电池形成的条件,铁是活泼金属,作负极,碳作正极,铁易被腐蚀;C项,铜镀层将铁球覆盖,使铁被保护,铁不易被腐蚀;D项,酸雨是电解质溶液,铁铆钉和铜板接触,形成原电池,铁易被腐蚀。
答案:C
2.解析:A项,铁、石墨及海水构成原电池时,Fe为负极,腐蚀速率加快;B项,中性条件下,铁发生吸氧腐蚀,石墨上氧气得到电子,电极反应为O2+2H2O+4e-===4OH-;C项,由于金属活动性:Zn>Fe,所以Zn为原电池的负极,Fe为正极,铁片不易被腐蚀;D项,中性环境下发生吸氧腐蚀,铁片上的电极反应为O2+2H2O+4e-===4OH-。
答案:D
3.解析:为了保障航行安全,延长轮船的使用寿命,通常在与海水接触的船壳(船底及船侧)上镶嵌一些金属块M,如锌,形成原电池,这种保护船壳免受腐蚀的方法叫牺牲阳极的阴极保护法,A项正确;M可能是锌等比铁稍活泼的金属,在原电池中做负极,先被腐蚀,铁比锡活泼,铁做负极,被腐蚀,B项错误;船壳在海水中主要发生吸氧腐蚀,C项正确;负极活泼金属失电子,被氧化,在保护船壳的过程中,负极反应为M-ne-===Mn+,D项正确。
答案:B
4.解析:防止金属腐蚀最关键的问题是使金属与空气、水等物质隔离,最常用的做法是覆盖保护层,如本题中的①④⑤;另外还有改变金属的内部结构等。保持金属表面清洁干燥可以减缓金属的腐蚀。
答案:D
5.解析:a是石墨,b是铁,K1、K2连接时,形成原电池,食盐水呈中性,铁发生吸氧腐蚀,A正确;a是锌,b是铁,K1、K2连接时,形成原电池,Zn比Fe活泼,Zn作负极被腐蚀,Fe作正极受到保护,故可模拟钢铁防护中的牺牲阳极法,B正确;K1、K3连接时,形成电解池,a是石墨,作电解池的阳极,可模拟电解饱和食盐水,C正确;K1、K3连接时,形成电解池,a是铁,作电解池的阳极而被腐蚀,若模拟钢铁防护中的外加电流法,应将铁连接电源的负极,D错误。
答案:D
6.答案:B
7.解析:根据图知,氧气得电子生成氢氧根离子、Cu失电子生成铜离子,发生吸氧腐蚀,则Cu做负极被氧化,腐蚀过程中,负极是c,发生氧化反应,A项正确;氧气在正极得电子生成氢氧根离子,电极反应式为O2+4e-+2H2O===4OH-,B项正确;多孔粉状锈Cu2(OH)3Cl为固体,故生成Cu2(OH)3Cl的离子方程式为2Cu2++3OH-+Cl-===Cu2(OH)3Cl↓,C项正确;不确定氧气是否在标准状况下,则不能计算氧气的体积,D项错误。
答案:D
8.解析:铁棒连接Zn片,发生腐蚀时,Zn作负极,Fe作正极,故甲区发生的电极反应式为O2+2H2O+4e-===4OH-,A错误;Zn是负极,电极反应式为Zn-2e-===Zn2+,则乙区产生Zn2+,B正确;铁棒连接Cu片,发生腐蚀时,Fe作负极,Cu作正极,丙区发生的电极反应式为O2+2H2O+4e-===4OH-,电极附近溶液显碱性,则丙区呈现红色,C正确;丁区Fe发生电极反应生成Fe2+,与K3[Fe(CN)6]反应生成蓝色沉淀,D正确。
答案:A
9.解析:由图可知开始时pH越大,腐蚀程度越小,后来pH越大,腐蚀程度越大,A项错误;由题图可知,pH=9.5时,铝被腐蚀,负极反应为Al-3e-+4OH-===AlO eq \\al(\s\up1(-),\s\d1(2)) +2H2O,B项错误;将铝做阳极,电解时可形成Al2O3保护膜:2Al+3H2Oeq \(=====,\s\up7(电解))Al2O3+3H2↑,C项正确;铝制餐具外面的保护膜防止了铝的进一步被腐蚀,所以不应经常打磨,D项错误。
答案:C
10.解析:无论是否鼓入空气,铁均作为负极,易失去电子生成亚铁离子,电极反应式为Fe-2e-===Fe2+,A项正确;不鼓入空气时,正极上可得到强还原性的H·,电极反应式为H++e-===H·,B项正确;若上端开口打开,并鼓入空气,可得到强氧化性的·OH,电极反应式为2H++2e-+O2===2·OH,故每生成1ml·OH,有1ml电子发生转移,C项错误;除去草酸需要具有氧化性的物质,上端开口打开,并鼓入空气可得到强氧化性的·OH,D项正确。
答案:C
11.解析:铁锅的腐蚀原理为Fe-C-电解质溶液构成原电池,其中Fe做负极,负极反应式为Fe-2e-===Fe2+,碳做正极,正极反应式为O2+4e-+2H2O===4OH-,A、C项错误;原电池中电子沿导线从负极流向正极,电子不能通过电解质溶液,B项错误;负极产生的Fe2+与正极产生的OH-反应生成Fe(OH)2,Fe(OH)2被氧气氧化为Fe(OH)3,Fe(OH)3进一步转化为Fe2O3·nH2O,故每生成1ml铁锈(Fe2O3·nH2O),由原子守恒和得失电子守恒可得关系式2Fe~Fe2O3·nH2O~6e-~eq \f(3,2)O2,即需eq \f(3,2)mlO2,标准状况下为33.6L,D项正确。
答案:D
12.解析:(1)①金属在中性或较弱的酸性条件下发生的是吸氧腐蚀。②发生吸氧腐蚀,越靠近液面接触到的O2越多,腐蚀得越严重。③锌块应固定在腐蚀最严重的C处形成原电池,锌做负极,铁闸做正极,得到保护。(2)要用石墨通过电化学腐蚀保护铜,只能用电解池原理,碳接电源正极,铜接电源负极。(3)A项,K1闭合时,该装置构成了FeCNaCl溶液原电池,铁做负极,发生氧化反应,电极反应式是Fe-2e-===Fe2+;B项,石墨棒做正极,发生的电极反应式是2H2O+O2+4e-===4OH-,故石墨棒周围溶液pH逐渐升高;C项,K2闭合时,该装置构成了FeC外加电源的电解池,石墨棒做阳极,Fe做阴极而不被腐蚀,该方法称为外加电流的阴极保护法;D项,K2闭合时,阳极的电极反应式是2Cl--2e-===Cl2↑,阴极的电极反应式是2H++2e-===H2↑,所以当电路中通过0.002NA个即0.002ml电子时,生成H2和Cl2的物质的量均为0.001ml,则两极共产生0.002ml气体。
答案:(1)①吸氧腐蚀 ②B ③C
(2)
(3)B
13.解析:由实验现象①②可知,潮湿是铁生锈的必要前提;而当潮湿程度相同时,硬质玻璃管中的实验与烧杯中实验的对比说明O2的浓度是影响铁生锈快慢的重要因素。
答案:(1)吸氧腐蚀 负极:2Fe-4e-===2Fe2+,正极:2H2O+O2+4e-===4OH-
(2)球形干燥管 碱石灰(或无水CaCl2) 干燥O2
(3)与O2接触,与水接触 氧气浓度
14.解析:(1)探究醋酸浓度对电化学腐蚀的影响时,应保证碳粉和铁粉的质量与参照实验相同,因此实验②中铁粉为2.0g;对比实验①和③可知,铁粉的质量及醋酸的浓度相同,而碳粉的质量不同,显然探究的是碳粉的含量对铁的电化学腐蚀的影响。(2)当铁发生析氢腐蚀时,由于生成H2,容器的压强不断增大,而发生吸氧腐蚀时,由于消耗O2,容器的压强不断减小,t2时容器的压强明显小于起始压强,说明铁发生了吸氧腐蚀,此时Fe作负极,失去电子发生氧化反应;碳粉作正极,O2在其表面得到电子发生还原反应,电极反应式为O2+2H2O+4e-===4OH-。(3)Fe发生电化学腐蚀时,放出热量,使体系的温度升高。
答案:(1)②2.0 ③碳粉含量的影响
(2)吸氧 还原 2H2O+O2+4e-===4OH- (3)反应放热,温度升高选项
连接
电极材料
分析
a
b
A
K1、K2
石墨
铁
模拟铁的吸氧腐蚀
B
K1、K2
锌
铁
模拟钢铁防护中的牺牲阳极法
C
K1、K3
石墨
铁
模拟电解饱和食盐水
D
K1、K3
铁
石墨
模拟钢铁防护中的外加电流法
编号
实验目的
碳粉/g
铁粉/g
醋酸/%
①
为以下实验
作参照
0.5
2.0
90.0
②
醋酸浓度
的影响
0.5
36.0
③
0.2
2.0
90.0
高中专题1 化学反应与能量第三单元 金属的腐蚀与防护课后作业题: 这是一份高中专题1 化学反应与能量第三单元 金属的腐蚀与防护课后作业题,共8页。试卷主要包含了答案等内容,欢迎下载使用。
高中化学苏教版 (2019)选择性必修1第四单元 沉淀溶解平衡达标测试: 这是一份高中化学苏教版 (2019)选择性必修1第四单元 沉淀溶解平衡达标测试,共11页。试卷主要包含了解析等内容,欢迎下载使用。
化学选择性必修1第三单元 盐类的水解课后作业题: 这是一份化学选择性必修1第三单元 盐类的水解课后作业题,共9页。试卷主要包含了解析等内容,欢迎下载使用。













