
2022版高考化学一轮复习第11章化学实验基础第4节化学实验方案的设计与评价训练含解析
展开第4节 化学实验方案的设计与评价
[A组·基础练习]
1.(2020·江苏南京五校联考)下列图示实验设计能实现相应实验目的的是( )
【答案】B
2.(2020·山西祁县第二中学校期末)下列设计的实验方案正确且能达到实验目的的是( )
A.验证碳、硅的非金属性强弱:将CO2气体通入水玻璃中,观察现象
B.检验淀粉水解是否生成葡萄糖:取少量淀粉水解液于试管中,直接加入新制的银氨溶液,水浴加热,观察现象
C.探究NaCl是否属于离子化合物:将两个电极插入NaCl溶液中,进行导电性试验
D.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量NaOH溶液,振荡后静置分液,并除去有机相中的水
【答案】A
3.下列实验操作和现象所得出的结论合理的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液 | 溶液变黄色 | H2O2的氧化性比Fe3+强 |
B | 先向盛有FeSO4溶液的试管中加入氯水,然后滴加KSCN溶液 | 溶液变为红色 | 原FeSO4溶液已被空气中的O2氧化变质 |
C | 向试管底部有少量铜的Cu(NO3)2溶液中加入稀硫酸 | 铜粉逐渐溶解 | 铜可与稀硫酸反应 |
D | 向NaHCO3溶液中加入NaAlO2溶液 | 有白色沉淀生成 | AlO结合H+的能力比CO强 |
【答案】D
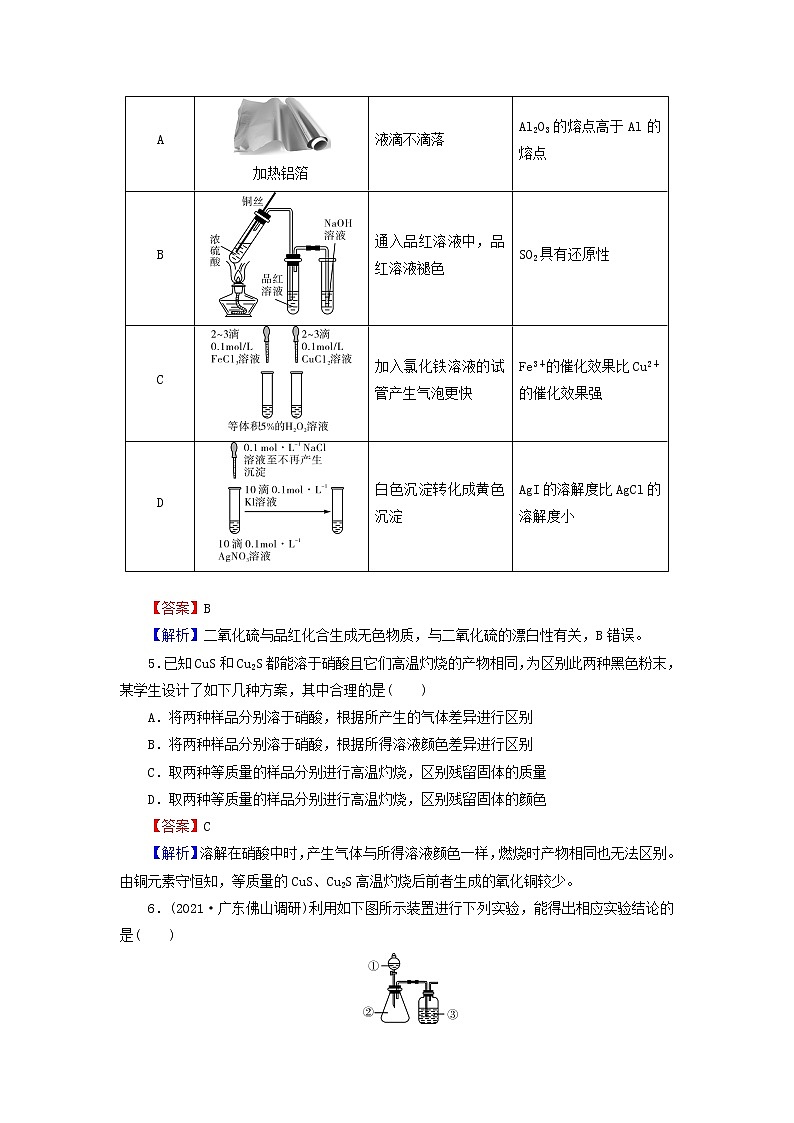
4.设计下列有关实验,其操作、现象和结论的叙述不相符的是( )
选项 | 实验 | 现象 | 结论 |
A | 加热铝箔 | 液滴不滴落 | Al2O3的熔点高于Al的熔点 |
B | 通入品红溶液中,品红溶液褪色 | SO2具有还原性 | |
C | 加入氯化铁溶液的试管产生气泡更快 | Fe3+的催化效果比Cu2+的催化效果强 | |
D | 白色沉淀转化成黄色沉淀 | AgI的溶解度比AgCl的溶解度小 |
【答案】B
【解析】二氧化硫与品红化合生成无色物质,与二氧化硫的漂白性有关,B错误。
5.已知CuS和Cu2S都能溶于硝酸且它们高温灼烧的产物相同,为区别此两种黑色粉末,某学生设计了如下几种方案,其中合理的是( )
A.将两种样品分别溶于硝酸,根据所产生的气体差异进行区别
B.将两种样品分别溶于硝酸,根据所得溶液颜色差异进行区别
C.取两种等质量的样品分别进行高温灼烧,区别残留固体的质量
D.取两种等质量的样品分别进行高温灼烧,区别残留固体的颜色
【答案】C
【解析】溶解在硝酸中时,产生气体与所得溶液颜色一样,燃烧时产物相同也无法区别。由铜元素守恒知,等质量的CuS、Cu2S高温灼烧后前者生成的氧化铜较少。
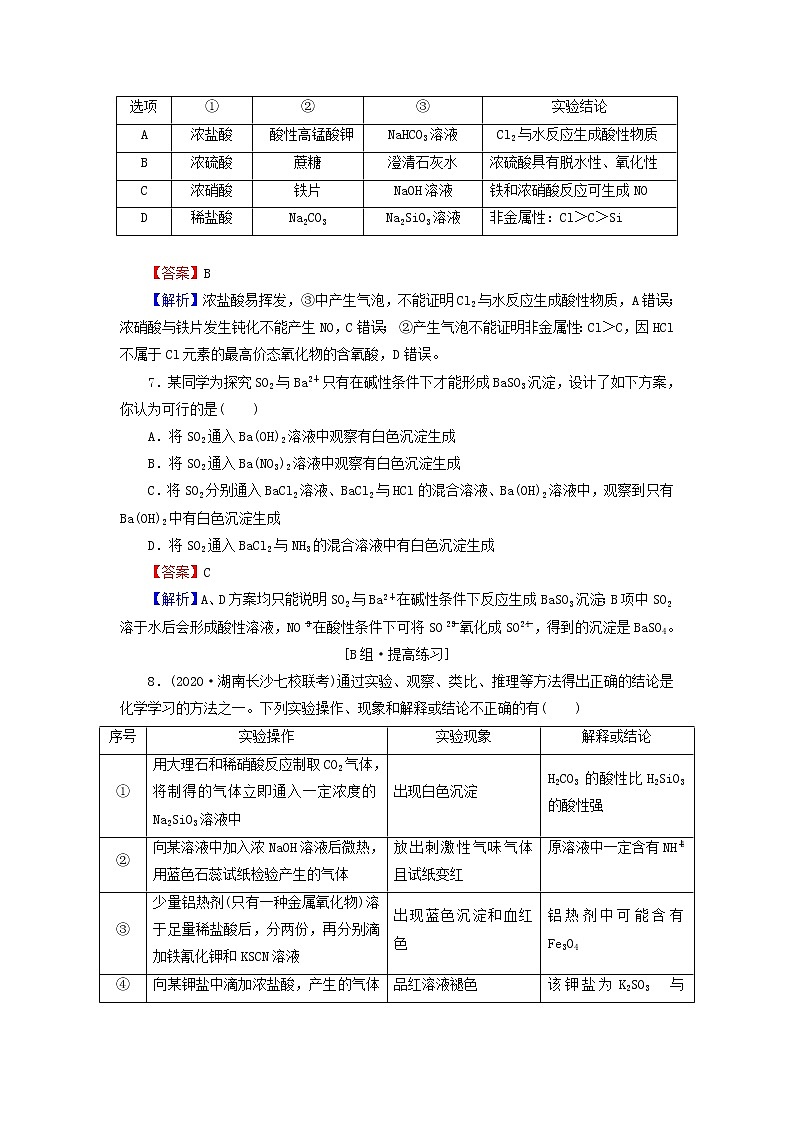
6.(2021·广东佛山调研)利用如下图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 |
A | 浓盐酸 | 酸性高锰酸钾 | NaHCO3溶液 | Cl2与水反应生成酸性物质 |
B | 浓硫酸 | 蔗糖 | 澄清石灰水 | 浓硫酸具有脱水性、氧化性 |
C | 浓硝酸 | 铁片 | NaOH溶液 | 铁和浓硝酸反应可生成NO |
D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
【答案】B
【解析】浓盐酸易挥发,③中产生气泡,不能证明Cl2与水反应生成酸性物质,A错误; 浓硝酸与铁片发生钝化不能产生NO,C错误; ②产生气泡不能证明非金属性:Cl>C,因HCl不属于Cl元素的最高价态氧化物的含氧酸,D错误。
7.某同学为探究SO2与Ba2+只有在碱性条件下才能形成BaSO3沉淀,设计了如下方案,你认为可行的是( )
A.将SO2通入Ba(OH)2溶液中观察有白色沉淀生成
B.将SO2通入Ba(NO3)2溶液中观察有白色沉淀生成
C.将SO2分别通入BaCl2溶液、BaCl2与HCl的混合溶液、Ba(OH)2溶液中,观察到只有Ba(OH)2中有白色沉淀生成
D.将SO2通入BaCl2与NH3的混合溶液中有白色沉淀生成
【答案】C
【解析】A、D方案均只能说明SO2与Ba2+在碱性条件下反应生成BaSO3沉淀;B项中SO2溶于水后会形成酸性溶液,NO在酸性条件下可将SO氧化成SO,得到的沉淀是BaSO4。
[B组·提高练习]
8.(2020·湖南长沙七校联考)通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一。下列实验操作、现象和解释或结论不正确的有( )
序号 | 实验操作 | 实验现象 | 解释或结论 |
① | 用大理石和稀硝酸反应制取CO2气体,将制得的气体立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
② | 向某溶液中加入浓NaOH溶液后微热,用蓝色石蕊试纸检验产生的气体 | 放出刺激性气味气体且试纸变红 | 原溶液中一定含有NH |
③ | 少量铝热剂(只有一种金属氧化物)溶于足量稀盐酸后,分两份,再分别滴加铁氰化钾和KSCN溶液 | 出现蓝色沉淀和血红色 | 铝热剂中可能含有Fe3O4 |
④ | 向某钾盐中滴加浓盐酸,产生的气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为K2SO3与KHSO3至少有一种 |
⑤ | 用pH试纸测量饱和新制氯水的pH | pH试纸先变为红色后褪色 | 饱和新制氯水呈酸性且Cl2具有漂白性 |
A.①②④⑤ B.②③④⑤
C.①②④ D.①②③⑤
【答案】A
【解析】硝酸易挥发,生成的CO2气体中含有一定量的硝酸,无法证明H2CO3的酸性比H2SiO3的酸性强,①错误;应用红色石蕊试纸检验产生的气体,试纸变蓝,②错误;能使品红溶液褪色,说明该气体的水溶液有漂白性,但是不能确定是二氧化硫还是氯气,④错误;pH试纸先变为红色后褪色,说明饱和新制氯水有酸性和漂白性,Cl2不具有漂白性,⑤错误。
9.下列关于各实验装置的叙述,不正确的是( )
A.图①可用于实验室制取少量NH3或O2
B.可用从a处加水的方法检验图②装置的气密性
C.实验室可用图③的方法收集Cl2或NH3
D.利用图④装置制取硫酸和氢氧化钠,其中b为阴离子交换膜,c为阳离子交换膜
【答案】C
【解析】图①可以利用碱石灰(或生石灰)与浓氨水制取氨气,用MnO2和双氧水(或Na2O2与水)反应制取氧气,A正确;图②关闭止水夹,从a处加水,U形管中产生液面差,静置一段时间,若液面差不变则气密性好,若不能形成液面差(或液面差发生变化),说明气密性不好,B正确;氯气密度比空气的大,收集时应从长导管通入,而氨气的密度比空气的小,收集时应从短导管通入,C错误;以Pt作电极电解Na2SO4溶液,电解时阳离子向阴极移动,阴离子向阳极移动,故SO通过阴离子交换膜b移到阳极产生硫酸,同理Na+通过阳离子交换膜c移到阴极形成NaOH,D正确。
10.下列有关实验,其操作、现象和解释或结论都正确的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 用玻璃棒蘸取溶液X进行焰色反应实验 | 火焰呈黄色 | 溶液X中含有Na+ |
B | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4 | 在管口观察到红棕色气体 | HNO3分解生成了NO2 |
C | 在新生成的AgCl沉淀中滴入稀KI溶液,振荡 | 白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
D | 向饱和碳酸钠溶液中通入过量的CO2 | 溶液变浑浊 | 析出了 Na2CO3 |
【答案】C
11.碱式碳酸镁可用于牙膏、医药和化妆品等工业,其化学式为4MgCO3·Mg(OH)2·5H2O。某碱式碳酸镁中含有SiO2杂质,为测定其纯度,某兴趣小组设计了如下两个方案。
方案Ⅰ:取一定质量的样品,与硫酸充分反应,通过测定生成CO2的质量计算纯度。
甲 乙 丙 丁
(1)乙中发生反应的方程式为____________________________________________。
(2)仪器接口的连接顺序为(装置可以重复使用)a____________,丁的作用是________________。
(3)当样品充分反应完后,缓慢通入空气的目的是________________。
方案Ⅱ:①称取碱式碳酸镁样品m g;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1 g。
(4)下列仪器中,该方案不会用到的是________________________。
A B C D E F
(5)判断样品完全分解的方法是________________________________;本实验至少需要称量______次。
(6)有同学认为方案Ⅱ高温煅烧的过程中会发生反应:MgCO3+SiO2MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?______(填“正确”或“错误”),请说明你的理由:______________________________。
【答案】(1)4MgCO3·Mg(OH)2·5H2O+5H2SO4==5MgSO4+11H2O+4CO2↑
(2)debcb(c) 除去CO2中的水蒸气
(3)将装置中残留的CO2全部赶出被完全吸收
(4)E
(5)样品连续两次高温煅烧,冷却称量质量相差0.1 g以内 4
(6)错误 该反应的发生不影响生成CO2和水蒸气的量
12.过氧化钙是一种温和的氧化剂,常温下为白色固体,易溶于酸,难溶于水、乙醇等溶剂。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。
A B C D E
(1)请选择必要的装置,按气流方向连接顺序为________________(填仪器接口的字母编号,装置可重复使用)。
(2)根据完整的实验装置进行实验,实验步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞,通入气体一段时间,加热药品;③反应结束后,__________________________________(填操作);④拆除装置,取出产物。
(3)若钙在空气中燃烧生成氮化钙(Ca3N2),同时可能生成过氧化钙。请利用下列试剂,设计实验检验钙的燃烧产物中是否含有过氧化钙______________________________。
(简要说明实验步骤、现象和结论;限选试剂:酸化的FeCl2溶液、NaOH溶液、KSCN溶液、稀硝酸)
(4)利用反应Ca2++H2O2+2NH3+8H2O==CaO2·8H2O↓+2NH,在碱性环境制取CaO2·8H2O的装置如下:
C中沉淀反应时常用冰水浴控制温度在0 ℃左右,其可能的原因分析:该反应是放热反应,温度低有利于提高CaO2·8H2O产率;________________。
(5)测定产品中CaO2含量的实验步骤如下:
步骤一:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的KI晶体(b g),再滴入少量2 mol·L-1的硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴__(作指示剂)。
步骤三:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2次,得出三次平均消耗Na2S2O3溶液体积为V mL。
CaO2的质量分数为____________(用字母表示)。[已知:I2+2S2O==2I-+S4O]
【答案】(1)dfebcf或dfecbf(答“dfebc”或“dfecb”也可)
(2)熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞(答出“先熄灭酒精灯,后停止通入氧气”即可)
(3)取少许样品于试管中,加入酸化的FeCl2溶解后,滴加KSCN溶液,若溶液变红色,则说明样品中含有过氧化钙;若溶液不变红色,则说明样品中不含有过氧化钙
(4)温度低可减少过氧化氢的分解,提高过氧化氢的利用率
(5)淀粉溶液 (或%)
13.已知:ClCH2CH2POOHOH+4NaOH―→NaCl+3H2O+
(乙烯利)
CH2—CH2↑+Na3PO4
可用如下图装置制取1,2-二溴乙烷(无色液体,密度为2.18 g·cm-3,熔、沸点分别为9.79 ℃、131.4 ℃,不溶于水);试管d中装有液溴(表面覆盖少量水)。
(1)e装置的作用是____________;当观察到___________________现象时,试管d中反应基本结束。
(2)若用冰水代替烧杯中的水(20 ℃),可能引起的不安全后果是________________。
(3)实验结束后,要精制试管d中的粗产品,操作先后顺序是________________(填标号)。
A.蒸馏 B.水洗
C.用干燥剂干燥 D.用10%NaOH溶液洗
E.水洗
(4)实验消耗40%乙烯利(摩尔质量为M)溶液50 g,制得产品m g,则乙烯利合成1,2-二溴乙烷的产率为_____________(用含M,m的代数式表示)。
(5)设计实验证明,反应后烧瓶中的混合溶液含有Cl-、PO,简述实验方案。已知:氯化银、磷酸银(黄色)、磷酸钡(白色)的Ksp分别为1.77×10-10、8.88×10-17 和3.4×10-23。______________________________。
【答案】(1)吸收溴蒸气 试管内溶液褪为无色
(2)d中长导管堵塞
(3)BDECA(或EDBCA)
(4)×100%
(5)取适量混合溶液,加入过量的Ba(NO3)2溶液,产生白色沉淀,证明溶液中存在PO;静置,取上层清液于试管中,加入过量稀硝酸和AgNO3溶液,产生白色沉淀,证明溶液中存在Cl-
【解析】(1)d中的液溴易挥发,会污染大气,应该进行尾气吸收,d中乙烯与溴发生加成反应使液溴褪色,生成的1,2-二溴乙烷为无色,当观察到试管内溶液褪为无色时说明d中反应基本结束。(2)温度过低会使1,2-二溴乙烷凝结为固体,导致d中长导管堵塞,发生危险。(3)实验结束后,要精制试管d中的粗产品,将粗产品先用水洗涤,再用10% NaOH溶液和水洗涤,分离后加入无水氯化钙干燥,待溶液澄清后进行蒸馏,可以得到纯净的1,2-二溴乙烷。(4)乙烯利合成1,2-二溴乙烷的产率为×100%=×100%。(5)由已知条件可知氯化银、磷酸银(黄色)、磷酸钡(白色)都是沉淀,且磷酸钡比氯化银更难溶,所以应该先检验PO再检验Cl-。
14.硝酸亚铁可用作媒染剂、分析试剂、催化剂等。
(1)硝酸亚铁可用铁屑在低温下溶于稀硝酸制得,还原产物为NO。反应的化学方程式为______________________________。
(2)某小组为探究硝酸亚铁晶体的热分解产物,按下图所示装置进行实验。
①仪器B的名称是________,实验中无水CuSO4变蓝,由此可知硝酸亚铁晶体含有______________________。
②实验中观察到A装置的试管中有红棕色气体生成,检验热分解后固体为氧化铁的实验方案为:
实验步骤 | 现 象 |
取少量固体加适量稀硫酸,振荡,将溶液分成两份 | 固体溶解后得黄色溶液 |
一份滴入________ | 溶液变成红色 |
另一份滴入1~2滴K3 [Fe(CN)6]溶液 | ________ |
A中硝酸亚铁晶体[Fe(NO3)2·xH2O]分解的化学方程式为________________。
(3)继续探究m g硝酸亚铁晶体中铁元素的质量分数。
①取A中热分解后的固体放入锥形瓶,用稀硫酸溶解,加入过量的KI溶液,滴入2滴__________作指示剂。
②用a mol/L Na2S2O3标准溶液滴定锥形瓶中的溶液(已知:I2+2S2O==2I-+S4O),滴定至终点时用去b mL Na2S2O3溶液,则硝酸亚铁晶体中铁的质量分数为______________________。
【答案】(1)3Fe+8HNO3(稀)==3Fe(NO3)2+2NO↑+4H2O
(2)①干燥管(或球形干燥管) 结晶水
②1~2滴KSCN溶液 无蓝色沉淀生成
4Fe(NO3)2·xH2O 2Fe2O3+8NO2↑+O2↑+4xH2O
(3)①淀粉溶液 ②%
高考化学一轮复习课时作业第10章第3讲 化学实验方案的设计及评价(含解析): 这是一份高考化学一轮复习课时作业第10章第3讲 化学实验方案的设计及评价(含解析),共10页。试卷主要包含了下列实验操作能达到实验目的的是,下列有关实验的操作正确的是,下列实验不能达到目的的是,已知等内容,欢迎下载使用。
苏教版高考化学一轮复习专题练10化学实验基础第31讲化学实验方案的设计与评价含答案: 这是一份苏教版高考化学一轮复习专题练10化学实验基础第31讲化学实验方案的设计与评价含答案,共9页。
高考化学一轮优化探究练习:第10章第32讲《化学实验方案的设计与评价》(含详解): 这是一份高考化学一轮优化探究练习:第10章第32讲《化学实验方案的设计与评价》(含详解),共14页。试卷主要包含了某学习小组在通过反应等内容,欢迎下载使用。












