2022年度最新人教版九年级化学下册第十单元 酸和碱期中复习试卷完整
展开这是一份2022年度最新人教版九年级化学下册第十单元 酸和碱期中复习试卷完整,共11页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
最新人教版九年级化学下册第十单元 酸和碱期中复习试卷完整
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
1、下列常见现象中,发生化学变化的是
A.潮解 B.乳化 C.溶解 D.指示剂变色
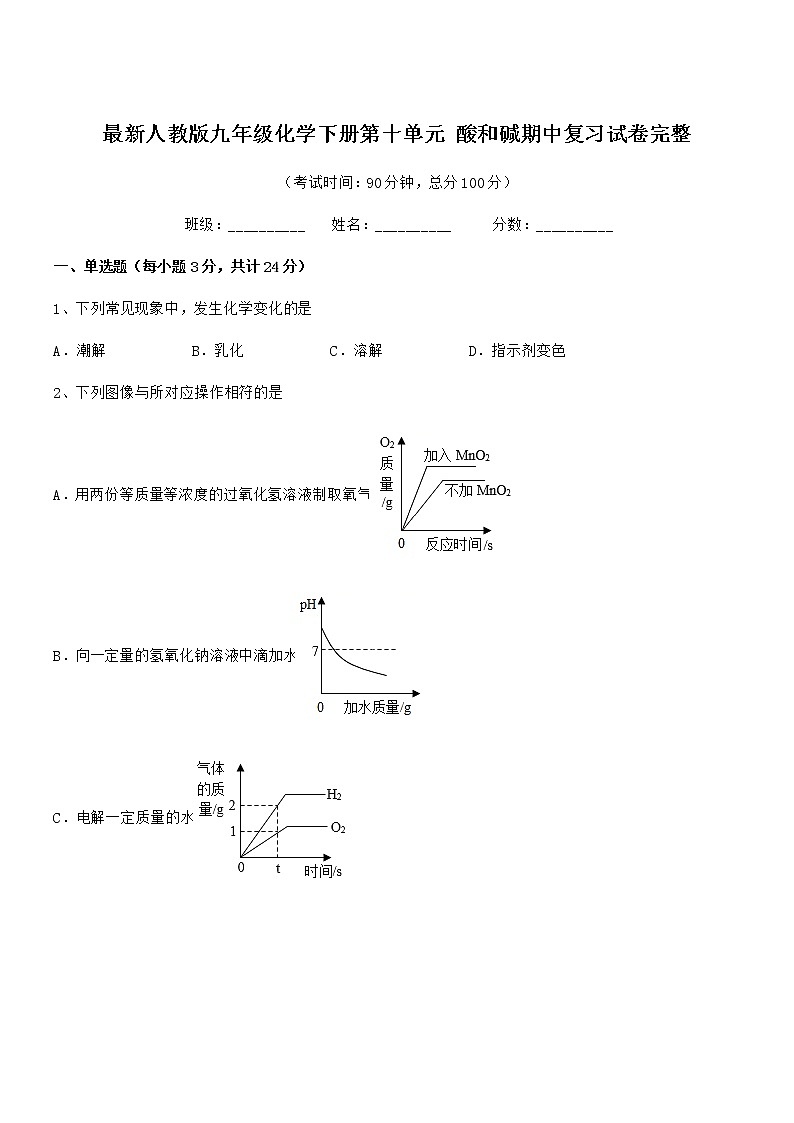
2、下列图像与所对应操作相符的是
A.用两份等质量等浓度的过氧化氢溶液制取氧气
B.向一定量的氢氧化钠溶液中滴加水
C.电解一定质量的水
D.一定质量的大理石中加入稀盐酸
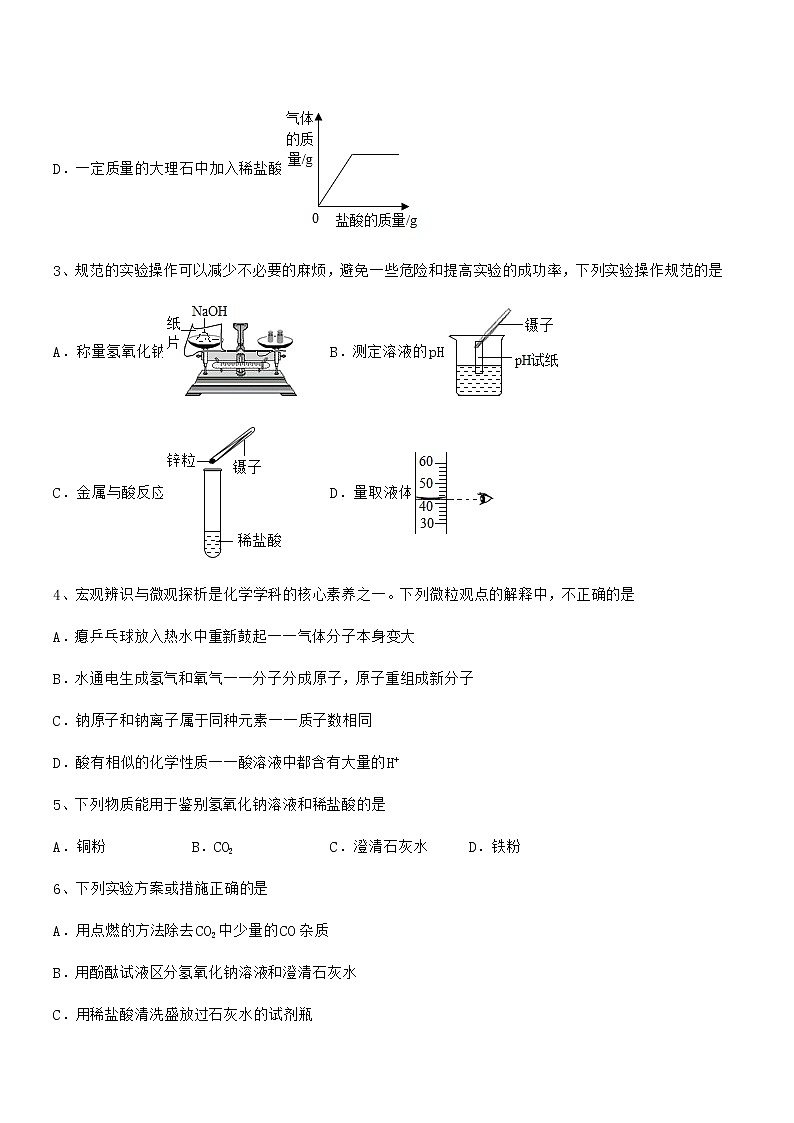
3、规范的实验操作可以减少不必要的麻烦,避免一些危险和提高实验的成功率,下列实验操作规范的是
A.称量氢氧化钠 B.测定溶液的pH
C.金属与酸反应 D.量取液体
4、宏观辨识与微观探析是化学学科的核心素养之一。下列微粒观点的解释中,不正确的是
A.瘪乒乓球放入热水中重新鼓起一一气体分子本身变大
B.水通电生成氢气和氧气一一分子分成原子,原子重组成新分子
C.钠原子和钠离子属于同种元素一一质子数相同
D.酸有相似的化学性质一一酸溶液中都含有大量的H+
5、下列物质能用于鉴别氢氧化钠溶液和稀盐酸的是
A.铜粉 B.CO2 C.澄清石灰水 D.铁粉
6、下列实验方案或措施正确的是
A.用点燃的方法除去CO2中少量的CO杂质
B.用酚酞试液区分氢氧化钠溶液和澄清石灰水
C.用稀盐酸清洗盛放过石灰水的试剂瓶
D.实验室稀硫酸和石灰石反应制取CO2
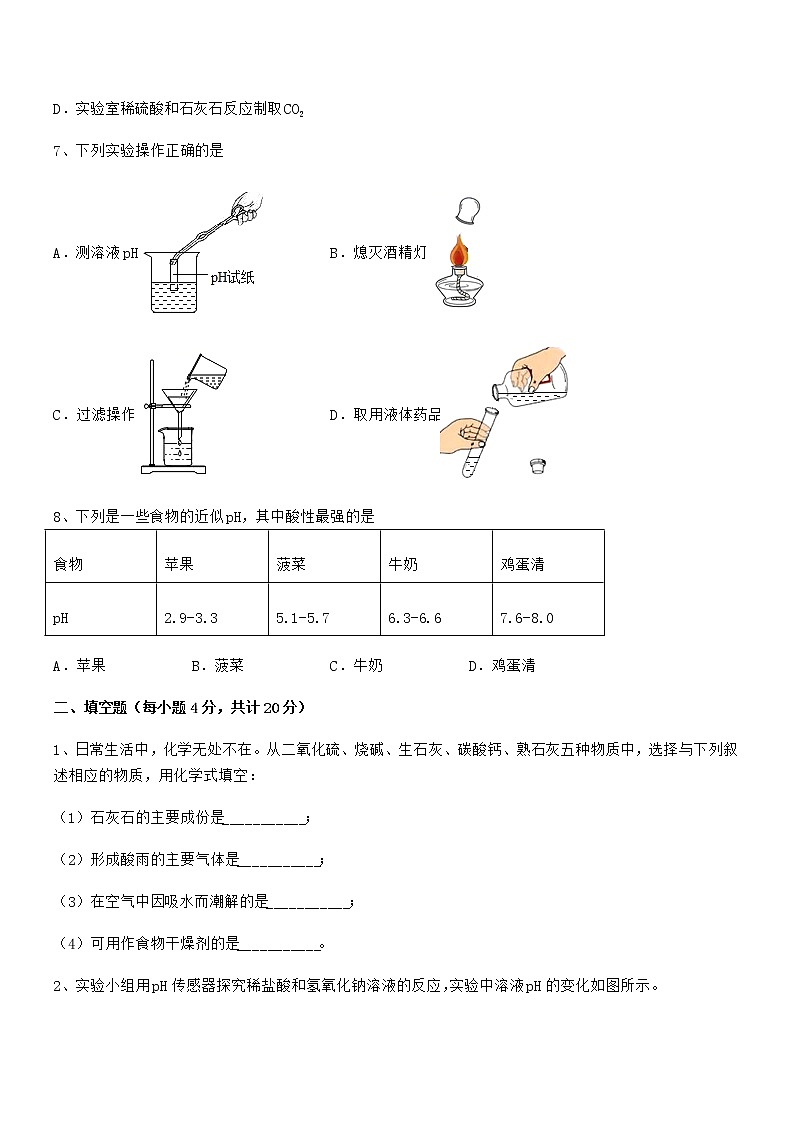
7、下列实验操作正确的是
A.测溶液pH B.熄灭酒精灯
C.过滤操作 D.取用液体药品
8、下列是一些食物的近似pH,其中酸性最强的是
食物 | 苹果 | 菠菜 | 牛奶 | 鸡蛋清 |
pH | 2.9-3.3 | 5.1-5.7 | 6.3-6.6 | 7.6-8.0 |
A.苹果 B.菠菜 C.牛奶 D.鸡蛋清
二、填空题(每小题4分,共计20分)
1、日常生活中,化学无处不在。从二氧化硫、烧碱、生石灰、碳酸钙、熟石灰五种物质中,选择与下列叙述相应的物质,用化学式填空:
(1)石灰石的主要成份是___________;
(2)形成酸雨的主要气体是___________;
(3)在空气中因吸水而潮解的是___________;
(4)可用作食物干燥剂的是___________。
2、实验小组用pH传感器探究稀盐酸和氢氧化钠溶液的反应,实验中溶液pH的变化如图所示。
(1)该实验是将______滴加到另一种溶液中;
(2)反应的化学方程式是______。
(3)a点时溶液中的溶质是______(用化学式表示), C点溶液中滴加紫色石蕊试液,溶液变______色。
3、盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化如图。
(1)根据pH变化图像判断,该反应的实验过程是按照___________(填“甲”或“乙”)图进行,实验室测定溶液酸碱度最简单的方法是使用___________。
(2)盐酸和氢氧化钠溶液反应的化学方程式为___________,实验现象为___________。
(3)向C点所对应的溶液中加入一种药品,便能确定溶质组成。这种药品可能是___________(填字母)。
A.CuO B.Cu C.紫色石蕊溶液
4、氨气是一种极易溶于水的无色有刺激性气味的气体。
(1)下图是液氨燃烧的微观示意图。
①氨气中氮元素的化合价为______。
②从微观角度看,该变化是化学变化的依据是______种类发生了改变。
③该反应的化学方程式为______。
(2)向氨水中滴入无色酚酞试液,溶液由无色变成______色;浓氨水需密封保存,其原因是______。
5、氢氧化镍是某种混合动力汽车电池的一种材料。镍原子结构示意图为:
(1)镍原子最外层电子数是:___________。
(2)氢氧化镍的化学式为__________,从组成上看,它属于________(选填“氧化物”、“酸”、“碱”、“盐”)。
三、计算题(每小题4分,共计36分)
1、某化工厂的废水中含少量氢氧化钠,技术人员欲测其含量。取废水20g,向其中逐滴滴加9.8%的稀硫酸,利用pH传感器测定溶液pH变化如图所示。
(1)图中A点表示的意义是______。
(2)通过计算判断该废水是否可以直接排放?(排放标准:废水中氢氧化钠的质量分数<0.001%)
2、某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HC1的质量。取10g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH值变化的部分数据如表所示:(已知BaC12溶液的pH=7)
滴加Ba(OH)2溶液的质量/g | 5 | 10 | 25 | 30 |
烧杯中产生沉淀的质量/g | 1.165 | 2.33 | m | 4.66 |
求:
(1)生成沉淀m的质量为__________。
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)。
3、固体氢氧化钠放置在空气中容易变质转化为碳酸钠。现称取一久置于空气中的烧碱样品20g完全溶于蒸馏水中配成100g溶液,现取100g的稀盐酸,分四次滴加到样品溶液中,产生气体与所加稀盐酸的质量关系如表所示。
次数 | 第1次 | 第2次 | 第3次 | 第4次 |
滴加盐酸的质量(g) | 25 | 25 | 25 | 25 |
产生气体的质量(g) | 2.2 | 4.4 | 4.4 | 4.4 |
(1)第_______次恰好完全反应。
(2)样品中氢氧化钠的质量分数_______?
4、常温下,在20g盐酸和硫酸混合液中,逐滴加入17.1%的氢氧化钡溶液。当碱液滴加至20g,硫酸钡沉淀达到最大值;当碱液加至60g时,溶液pH=7。求:
(1)原混合液中硫酸的质量分数。
(2)当pH=7时溶液中溶质的质量。
5、在托盘天平的两盘上各放一只等质量的烧杯,在两只烧杯里分别加入 50 g 溶质质量分数为 14.6%的稀盐酸。将天平调节平衡后,向左盘烧杯中投入一定量的碳酸钠固体,恰好完全 反应;向右盘烧杯中投入 6.4 g 金属镁的样品(样品有杂质且杂质不含镁元素,不与稀盐酸反应), 充分反应后天平再次平衡,则该金属镁样品中镁的质量分数 ω 的取值范围为______。
6、将40g稀盐酸逐滴加入20g溶质质量分数为4%的氢氧化钠溶液中,边滴加边搅拌。随着稀盐酸的滴入,溶液的pH变化如图一所示,溶液的温度变化如图二所示(不考虑反应过程中的热量损失)。试回答:
(1)图二中B点时溶液中溶质为______。
(2)计算稀盐酸中溶质的质量分数。
7、取铜与氧化铜的混合物5g于烧杯中,向烧杯中加入稀硫酸,发现烧杯中剩余固体的质量与加入稀硫酸质量的关系如图所示。回答下列问题:
(1)剩余的3.4克固体物质是______,该物质在原混合物中的质量分数是______。
(2)求所加稀硫酸的溶质质量分数。
8、某硫酸厂为了检验排放的酸性废水中硫酸的含量,取溶质质量分数为4%的标准氢氧化钠溶液100g,滴加5滴酚酞试液,然后逐渐加入废水样品至溶液刚好变为无色,共用去废水样品200g。假设废水中的酸性物质只有硫酸。试计算废水样品中硫酸的溶质质量分数。
9、造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
(1)检测废水呈碱性的简单方法是___________。
(2)若某造纸厂废水中NaOH的质量分数为l.6%,现有废硫酸9.8t(H2SO4的质量分数为20%),可以处理的废水质量是多少?
四、实验探究(每小题5分,共计20分)
1、某兴趣小组以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究。小组同学向烧杯中的氢氧化钠溶液加入稀硫酸,一会儿会发现忘记了滴加指示剂,因此,他们停止滴加稀硫酸,并对烧杯内稀硫酸与氢氧化钠溶液是否发生了反应进行探究。
(1)小组同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH_____7(填“>”、“=”或“<”) | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了 |
(2)写出该反应的化学方程式:__________。
(3)同学们经过讨论一致认为,不用上述方法,用其他试剂也可以证明稀硫酸与氢氧化钠溶液能发生反应,于是分成甲、乙两组继续试验:
甲组实验:探究 CuSO4溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应。
(实验操作及现象)向氢氧化钠溶液中滴加足量稀硫酸时无明显现象,再滴加CuSO4溶液时没有出现蓝色沉淀。
(实验结论)通过以上实验操作及现象,你认为用CuSO4溶液________(填“可以”或“不可以”) 证明稀硫酸与氢氧化钠溶液能发生反应。
乙组实验:探究BaCl2溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应。
(实验操作及现象)向稀硫酸中滴加足量NaOH溶液无明显现象,再滴加BaCl2溶液时出现白色沉淀。
(实验结论)通过以上实验操作及现象,你认为用BaCl2溶液__________(填“可以”或“不可 以”)证明稀硫酸与氢氧化钠溶液能发生反应,理由是__________。
2、在做氧化铜与木炭反应的实验时,往往会发现反应后试管中仍有黑色固体。小明对此进行了探究,并邀请你一起参与。
请写出反应的化学方程式_________________。
(提出问题)氧化铜与木炭充分反应结束后,试管中的黑色固体是什么?
(猜想或假设)可能是①木炭;②_______________;③____________________。
(查阅资料)铜、木炭都不与稀硫酸反应,而氧化铜能与稀硫酸反应形成蓝色溶液
(实验与结论)请设计实验验证小明的猜想
实验步骤 | 实验现象 | 实验结论 |
___________ | __________________ | _________________ |
(实验反思)科学探究的方法有多种,请你再设计两种方法来证明小明的猜想。
方案一:_______________________。
方案二:____________________。
3、化学兴趣小组的同学将足量的锌粒加入到某未知浓度硫酸中,发现有大量的气泡放出,并闻到有刺激 性气味,他们对气体的成分进行了探究。
(提出问题)锌粒加入某未知浓度硫酸后生成的气体是什么?
(查阅资料)①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气,能生成二氧化硫气体。
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色;
③浓硫酸有吸水性,常用作干燥剂。
④氢氧化钠溶液可吸收二氧化硫。
(提出猜想)甲:气体可能是 H2; 乙:气体可能是 SO2; 丙:气体可能是________。
(实验探究)为了验证上述猜想,同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:
(1)实验开始后,观察到 A 中品红溶液褪色,证明气体中含有_________。
(2)C装置在点燃酒精灯加热之前应先通一段时间的气体,目的是______;加热一段时间后,观察到__________,证明气体中含有H2,化学方程式为_________。
(问题讨论)(1)氢氧化钠与二氧化硫反应生成亚硫酸钠(Na2SO3)和水,化学方程式为: _____________。
(2)锌与浓硫酸和稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是____________(填一种合理的答案)。
4、某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石和稀盐酸制取),对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究。
(分析推断)根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙。但其中是否含有氯化氢需要通过实验来证明。若剩余溶液显酸性(含有H+),说明含有氯化氢。
(查阅资料)碳酸钙不溶于水,氢氧化钙微溶于水,氯化钙溶液呈中性。
(实验过程)将剩余的溶液倒入烧杯中,微热后冷却到室温。
| 实验操作 | 实验现象 | 实验结论 |
甲同学 | 取烧杯中的溶液少许于试管中,向其中滴加______ | 溶液变红 | 溶液显酸性(含有H+) |
乙同学 | 取烧杯中的溶液少许于试管中,向其中加入少量的锌粒 | 现象:有气泡产生 反应的化学方程式是______ | |
丙同学 | 取烧杯中的溶液少许于试管中,向其中加入少量的石灰石 | 现象:有气泡产生 反应的化学方程式是______ |
(拓展提高)若要从剩余溶液中得到尽可能多的纯净的氯化钙固体,同学们认为可以向剩余溶液中加入稍过量的______(填化学式),经______、蒸发等操作后即可完成。
相关试卷
这是一份2022年最新人教版九年级化学下册第十单元 酸和碱期中复习试卷【完整版】,共13页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2022年度最新人教版九年级化学下册第十单元 酸和碱期中试卷完整版,共12页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2022年度最新人教版九年级化学下册第十单元 酸和碱期中复习试卷【今年】,共15页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。












