
2022年度最新人教版九年级化学下册第九单元溶液期中复习试卷(学生专用)
展开最新人教版九年级化学下册第九单元溶液期中复习试卷(学生专用)
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
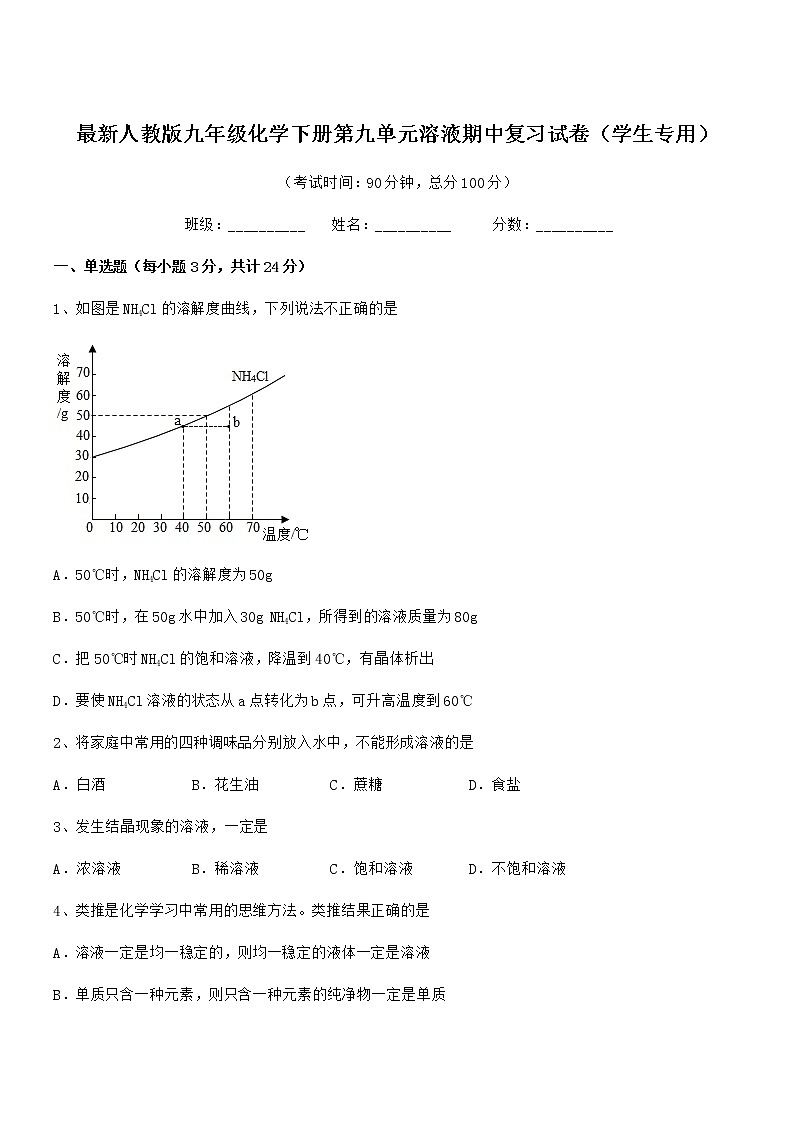
1、如图是NH4Cl的溶解度曲线,下列说法不正确的是
A.50℃时,NH4Cl的溶解度为50g
B.50℃时,在50g水中加入30g NH4Cl,所得到的溶液质量为80g
C.把50℃时NH4Cl的饱和溶液,降温到40℃,有晶体析出
D.要使NH4Cl溶液的状态从a点转化为b点,可升高温度到60℃
2、将家庭中常用的四种调味品分别放入水中,不能形成溶液的是
A.白酒 B.花生油 C.蔗糖 D.食盐
3、发生结晶现象的溶液,一定是
A.浓溶液 B.稀溶液 C.饱和溶液 D.不饱和溶液
4、类推是化学学习中常用的思维方法。类推结果正确的是
A.溶液一定是均一稳定的,则均一稳定的液体一定是溶液
B.单质只含一种元素,则只含一种元素的纯净物一定是单质
C.化合物中元素都显化合价,则同种元素在一种化合物中化合价一定相同
D.燃烧一定都伴随发光发热,则有发光发热现象的一定是燃烧
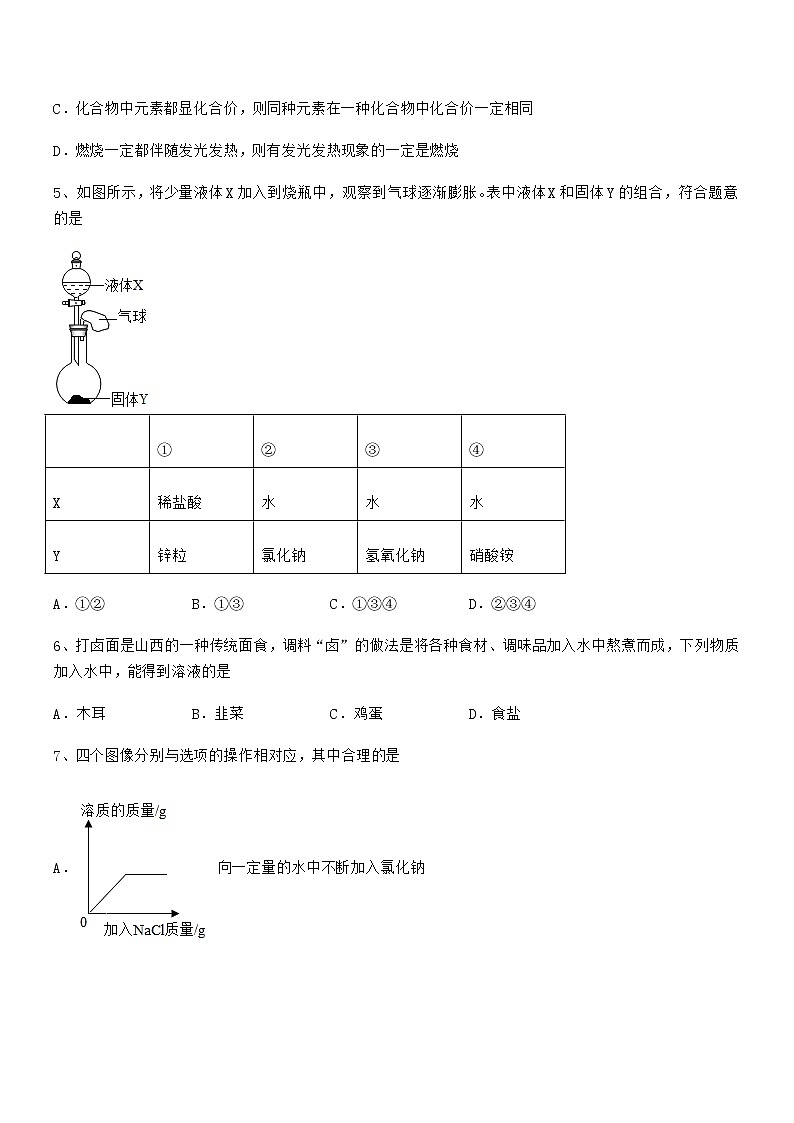
5、如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀。表中液体X和固体Y的组合,符合题意的是
| ① | ② | ③ | ④ |
X | 稀盐酸 | 水 | 水 | 水 |
Y | 锌粒 | 氯化钠 | 氢氧化钠 | 硝酸铵 |
A.①② B.①③ C.①③④ D.②③④
6、打卤面是山西的一种传统面食,调料“卤”的做法是将各种食材、调味品加入水中熬煮而成,下列物质加入水中,能得到溶液的是
A.木耳 B.韭菜 C.鸡蛋 D.食盐
7、四个图像分别与选项的操作相对应,其中合理的是
A. 向一定量的水中不断加入氯化钠
B. 恒温蒸发氯化钠的饱和溶液
C. 双氧水与二氧化锰反应
D. 高温条件下一氧化碳还原化铜
8、下列有关溶液的说法错误的是
A.溶液是均一、稳定的混合物
B.溶液中的溶质可以是固体、液体或气体
C.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
D.氯化钠溶于水就是钠离子和氯离子在水分子作用下均匀扩散到水中的过程
二、填空题(每小题4分,共计20分)
1、硝酸钾、氯化钾的溶解度曲线如图所示。
(1)t2℃时硝酸钾的溶解度为______g/100g水,P点的含义是______。
(2)若硝酸钾中混有少量的氯化钾,可采用______的方法提纯硝酸钾(填“蒸发结晶”或“降温结晶”)。
(3)t2℃时,将30g氯化钾加入到50g水中,充分溶解后形成的溶液的是______(填“饱和溶液”或“不饱和溶液“),其溶液的溶质质量分数为______(结果精确到0.1%)。
(4)将接近饱和的硝酸钾溶液转化为饱和溶液的方法是______(写二种方法)。
(5)t2℃相同质量的硝酸钾和氯化钾饱和溶液,降至t1℃时,析出晶体的质量,硝酸钾______氯化钾(填“大于“或“小于”或"等于”),t2℃,分别将100g和50g两份硝酸钾饱和溶液蒸发10g水,恢复到t2℃,析出晶体的质量,前者______后者(填“大于“或“小于“或“等于“)。
2、硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是硝酸钾、氯化铵中的一种物质。
(1)硝酸钾和氯化铵两种物质的溶解度均随温度的升高而______。
(2)由图1可知:t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为______。
(3)结合图1和图2判断:烧杯内的物质R是______,①②③三种情况下,一定是饱和溶液的有______(填序号)。
3、如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)A点的含义是______。
(2)在30 ℃时,向30克甲物质中加入50克水,充分溶解后所得溶液是______溶液(填“饱和”或“不饱和”)。
(3)若乙中混有少量甲,最好采用______的方法提纯乙。
(4)将30 ℃时甲、乙、丙三种物质的饱和溶液降温到10 ℃,则其溶质质量分数不变的物质是______。
(5)20℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
4、以李衍廷,张国航,田建傲,高中田,黄可心,郝佳艺,张潇文,候奉畅,王运涵,陈鹏旭,刘子豪,王志诚,陈文哲,张钊衡,郑德诩,赵兴冉,窦义政,夏俊杰同学为代表的化学兴趣小组用提取的精盐配制100g质量分数为11.7%的氯化钠溶液,请你帮忙参与完成:
(1)计算:氯化钠的质量为______g,水为______g。
称量:用托盘天平称量,氯化钠应放在左盘。
(2)溶解:用量筒来量取所需的水(水的密度为1g/cm3),量筒的规格是______(从下列中选用:10mL、25 mL、50 mL、100 mL)。量取液体时,量筒必须放平,视线与液体的______保持水平。溶解氯化钠要用到玻璃棒,其作用是______。
(3)反思:若称取的氯化钠中含有水分,则所配制的溶液溶质质量分数会______(填“偏大”、“偏小”或“无影响”)。
5、甲、乙两种固体物质的溶解度曲线如下图所示。
(1)t1℃时,甲、乙饱和溶液中溶质的质量分数:甲______乙(填“>”“<”或“=”)。
(2)t2℃时,将60g乙物质放入100g水中,所得溶液中,溶质与溶剂的质量比为______(填最简整数比)。
(3)现有t2℃时,甲、乙两种物质的饱和溶液各100,将这两种溶液分别降温到t1℃,所得溶液中溶质的质量分数甲______乙(填“>”、“<”或“=”)。
(4)小明同学进行了如下图所示的实验:
上述实验过程中所得的溶液,属于不饱和溶液的是______(填序号),溶液中溶质的质量分数相同的是______(填序号)。
(5)喝了汽水以后,常常会打嗝。这说明随温度升高气体的溶解度______。
三、计算题(每小题4分,共计36分)
1、某食品加工厂生产的酱油中氯化钠的质量分数为15%~18%,该厂日产酱油15t。试计算该厂每月(按30天计)消耗氯化钠的质量。
2、某同学为定量研究氢氧化钠溶液与稀盐酸反应,做了如下实验:取适量的溶质质量分数为10%的氢氧化钠溶液,加入到50克溶质质量分数为7.3%的稀盐酸中,恰好完全反应。求:(写计算过程)
(1)加入的氢氧化钠溶液的质量。
(2)反应后所得溶液中溶质的质量分数。
3、请你仔细分析如图所示的实验过程和提供的数据,计算反应后所得溶液中溶质的质量分数是____?
4、回答下列问题
(1)800kg质量分数为0.5%的过氧乙酸消毒液中,过氧乙酸的质量为_____kg。
(2)要配制800kg质量分数为0.5%的过氧乙酸消毒液,需质量分数为16%的过氧乙酸溶液的质量是多少?
5、实验室常用过氧化氢溶液与二氧化锰混合制取氧气.现将2.5g二氧化锰放入盛有50g过氧化氢溶液的锥形瓶中,完全反应后,放出气体的质量与反应时间的关系如图所示.
试求
(1)完全反应后生成的氧气的质量为______g.
(2)求过氧化氢溶液中过氧化氢的质量分数。
6、实验室制取二氧化碳结束后,17中学化学兴趣小组的同学对锥形瓶内剩余的固液混合物(以下简称废液)做了如下实验:
请回答下列问题:
(1)实验中发生反应的化学方程式为___________。
(2)根据已知条件列出求解12.5g大理石中碳酸钙质量(x)的比例式___________。
(3)根据实验可知废液中含有的可溶性物质有___________(填化学式);
(4)所用废液中盐酸的质量分数为___________。
(5)操作A的名称为___________。
(6)下图中可以表示H+变化的是___________(填序号)。
7、某合金可能由铜与镁、锌中的一种组成,现欲测定其组成,进行如下实验:取该合金样品30g放入烧杯中,然后将200g硫酸质量分数为19.6%的稀硫酸平均分四次依次加入该烧杯中,每次均充分反应。实验数据如下图所示:
请回答下列问题:
(1)写出合金中金属(用R表示)与酸反应的化学方程式_________。
(2)根据已知条件列出求解第二次产生氢气质量(x)的比例式_________。
(3)该合金由铜与_________两种金属组成。
(4)该合金中铜的质量分数为_________。
(5)欲将上述合金样品中的铜转化为铜盐,可将上述最终混合物过滤,将滤渣、洗涤、烘干,然后在空气中加热,充分反应,可得到氧化铜的质量为_______,再经过某些反应就制得铜盐。
8、如图,小明同学将200g质量分数为20%的硝酸钾溶液做如图操作,请通过计算回答:
(1)往甲烧杯溶液加入5g硝酸钾固体,完全溶解后,溶液的溶质质量分数为多少?(结果保留到0.1%)
(2)若将乙烧杯溶液稀释为溶质质量分数为5%的硝酸钾溶液,则需加水多少g?
9、某化工厂排放的废水中含有碳酸钾和氯化钾,十五中化学兴趣小组为探究废水中碳酸钾的含量,提取50g废水样品于容器中,逐滴加入9.8%的稀硫酸,反应过程中产生二氧化碳的质量与加入稀硫酸的质量如图。请计算:
(提示:碳酸钾与硫酸反应的化学方程式为,氯化钾不与酸反应)
(1)生成二氧化碳的质量为_________g。
(2)该废水中碳酸钾的质量分数为多少?(写出计算过程)
(3)反应后生成硫酸钾的质量为多少?
四、实验探究(每小题5分,共计20分)
1、对比归纳是学习化学的重要方法。请你参与下图三个探究活动并回答问题。
(探究活动一)探究影响木炭燃烧剧烈程度的因素:
木炭在氧气中燃烧比在空气中燃烧更剧烈,说明了影响木炭燃烧剧烈程度的因素是_____。
(探究活动二)探究影响物质溶解性的因素:
(1)同学们做了A试管和B试管的对比实验,发现B试管中固体可溶,A试管中固体几乎不溶。该对比实验说明了影响物质溶解性的因素是_____。
(2)同学们又补充了C试管所示实验,他们想探究的影响因素是_____。
(探究活动三)探究二氧化碳能否与水、饱和石灰水、氢氧化钠溶液反应:
小明分别振荡三个软质塑料瓶,观察到塑料瓶都变瘪且变瘪的程度由大到小的顺序为A>B>C。
(1)小明认为二氧化碳与三种物质都能发生反应,你认为小明的结论_____(填“是或否”)正确,理由是_____。
(2)B瓶中发生反应的化学方程式为_____。
(3)对比A瓶与_____瓶的实验现象,可证明二氧化碳能与氢氧化钠溶液发生反应且溶质的溶解性更强。
2、某校化学兴趣小组在老师指导下,对过氧化氢溶液分解制取氧气进行再探究。
(初步探究)写出实验室用过氧化氢溶液制取氧气的化学方程式:_____。
(继续探究)小组同学通过查阅资料得知,溶液也可作为过氧化氢溶液分解的催化剂,氯化铜溶液中含有H2O、Cu2+、Cl﹣,到底哪种微粒对过氧化氢溶液的分解起催化作用呢?
(作出猜想)
猜想一:可能是H2O;
猜想二:可能是_____;
猜想三:可能是Cl﹣。
(分析交流)猜想一肯定是错误的,因为_____。
(实验探究)为了进一步验证猜想,小组同学设计了如表实验:
实验操作 | 实验现象 |
其他条件不变,向过氧化氢溶液中加入NaCl溶液 | 无明显变化 |
其他条件不变,向过氧化氢溶液中加入Na2SO4溶液 | 无明显变化 |
其他条件不变,向过氧化氢溶液中加入_____(填化学式)溶液 | 立即产生大量气泡 |
(结论反思)猜想_____成立。
(拓展应用)与课本中二氧化锰相比,从循环利用的角度分析,_____(填“二氧化锰”或“氯化铜溶液”)更适合作该反应的催化剂。
(深入探究)小组同学查阅了不同金属离子对过氧化氢分解影响的实验资料得知,100℃时,在不同金属离子存在下,纯过氧化氢24h的分解率如表所示。
实验编号 | 离子 | 加入量(mg/L) | 分解率% |
① | 无 | ﹣ | 2 |
② | Al3+ | 1.0 | 2 |
③ | Fe3+ | 1.0 | 15 |
④ | Cu2+ | 0.1 | 86 |
⑤ | Cr3+ | 0.1 | 96 |
(交流反思)实验①的目的是_____,通过以上探究可得出的结论:_____(写一点即可)。
(继续探究)在实验时,小组同学发现实验室氯化铜溶液的颜色有绿色、蓝色等,氯化铜溶液颜色与什么有关呢?
(1)小组同学提出氯化铜溶液的颜色可能与溶液的浓度有关。
(实验)步骤Ⅰ:用托盘天平称取无水氯化铜固体5.0g置于小烧杯中;步骤Ⅱ:往小烧杯中加入一定量的蒸馏水,搅拌,观察溶液的颜色并记录。
室温下的实验现象及数据记录如表:(水的密度为1g/mL)
加入水的体积/mL | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 |
溶液颜色 | 深绿 | 墨绿 | 墨绿 | 蓝绿 | 绿色 | 深蓝 | 蓝色 | 蓝色 | 浅蓝 | 淡蓝 |
a 上述实验可以得到的结论是氯化铜溶液颜色和其浓度有关。
b 仅从上述实验数据判断,为配制蓝色的氯化铜溶液,其溶液中溶质质量分数不超过_____(数据精确到0.1%)。
(2)老师提示氯化铜溶液颜色还与温度有关,请设计实验验证_____。
3、(活动探究二)某小组同学在协助老师整理化学试剂时,发现一瓶标签残缺的无色液体(如下图)(温馨提示:标签上的5%表示该混合物中主要成分所占的质量分数)。他们对此瓶无色液体是什么产生了兴趣,于是进行了如下探究。
(大胆猜想)猜想一:水 猜想二: 过氧化氢溶液
小组同学对标签又进行了仔细的观察、分析,他们一致认为/猜想一不合理。理由是_____
(设计方案)同学们结合所学知识设计出如下探究方案:
向盛有少量二氧化锰的试管中加入适量的该液体,并将带火星的木条放在试管口。
(实验与事实)按上述方案进行实验,发现有大量气泡产生,带火星的木条复燃。
(结论与解释)(1)以上事实证明猜想_____是正确的;
(2)产生气体的反应可用化学方程式表示为_____。
(反思与评价)(1)在实验中,某同学提出应该先将气体收集,然后用带火星的木条检验,你认为 _____(填“有”或“没有”)必要。
(2)为避免在今后的实验中出现标签残缺的情况,在倾倒液体时应注意_____。
(拓展与迁移) 根据探究结果,重新贴好标签。标签上化学式中氧元素的化合价为_____价(已知氢元素显+1价)。
4、实验设计是化学实验的重要环节。请根据下列实验要求回答相关问题: (活动与探究一)用对比实验方法探究二氧化碳的性质。
(1)实验一中振荡3个矿泉本塑料瓶,观察到塑料瓶变瘪的程度为A > B > C,其中变浑浊的瓶内发生反应的化学方程式为___________________________;对比A瓶与__(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应。
(2)实验二观察到C装置中发生的现象是_____________________结论是______________
(用化学方程式表示)。
(活动与探究二)用变量控制方法探究影响物质溶解性的因素。
(3)实验三目的是探究_____对硝酸钾溶解性的影响;实验四是探究溶剂种类对物质溶解性的影响,该实验中需要控制的变量是温度和溶剂的质量。
(活动与探究三)定量测定空气中氧气的含量。
(4)实验五中,反应的原理为__________________________(用化学方程式表示);装置一比装置二更合理,理由是____________________________________________;
根据下表提供的实验数据,完成下表:
硬质玻璃管 | 反应前注射器中 气体体积 | 反应后注射器中 气体体积 | 实验测得空气中氧气 的体积分数 |
30mL | 20mL | 12 mL |
|
定量实验操作中易产生误差,如果反应前气球中存在气体(其量小于注射器内的空气),而实验后冷却至室温,将气球内的气体全部挤出读数,导致实验测得结果 ______(填“偏小、‘偏大”或“无影响”)。
2022年度最新人教版九年级化学下册第九单元溶液期末模拟试卷学生专用: 这是一份2022年度最新人教版九年级化学下册第九单元溶液期末模拟试卷学生专用,共15页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2022年最新人教版九年级化学下册第九单元溶液期中复习试卷学生专用: 这是一份2022年最新人教版九年级化学下册第九单元溶液期中复习试卷学生专用,共15页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2021年度最新人教版九年级化学下册第九单元溶液期中复习试卷(学生专用): 这是一份2021年度最新人教版九年级化学下册第九单元溶液期中复习试卷(学生专用),共13页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。












