






河北专版中考化学总复习第三部分模拟检测冲刺中考阶段检测卷三课件新人教版
展开河北省二○一八年初中毕业生升学文化课考试阶段检测卷(三)(模块四)
(时间:60分钟 满分:60分)
一、选择题(本大题共14个小题,共28分。每小题的四个选项中,只有一个选项符合题意,每小题2分)1.学校食堂提供了下列5种食物:小雨为自己选的午餐中,较合理的组合是( )①炒油菜 ②香蕉 ③米饭 ④红烧肉 ⑤炒豆腐A.①②③ B.①③⑤ C.①④⑤ D.③④⑤B 人体需要的六大营养物质:蛋白质、糖类、油脂、维生素、无机盐和水;结合题意,蔬菜、水果中富含维生素;米饭中富含淀粉,淀粉属于糖类;红烧肉、豆腐中含有蛋白质。①②③中富含维生素、糖类,①③⑤中富含维生素、糖类、蛋白质,①④⑤中富含维生素、蛋白质,③④⑤中富含糖类、蛋白质。安排的午餐食谱中,B的营养搭配较为齐全,较合理的是B。
2.下列事实与解释相符的是( )A.一氧化碳用于工业炼铁——一氧化碳具有还原性B.盐酸清除铁锈——盐酸能与铁反应C.用嘴吹燃着的蜡烛,蜡烛熄灭——降低了可燃物的着火点D.活性炭净水——活性炭能与水中杂质反应A 一氧化碳具有还原性,所以一氧化碳用于工业炼铁,A正确;盐酸清除铁锈,是利用盐酸能与金属氧化物反应的性质,B错误;物质着火点是固有属性,一般情况是不会发生改变的,用嘴吹蜡烛,蜡烛熄灭是因为降低了蜡烛周围的温度至可燃物的着火点以下,C错误;活性炭有吸附性,能吸附水中杂质,而不是与杂质反应,D错误。
3.下列图示实验操作正确的是( )C 检验二氧化碳是否收集满时,应将燃着的木条放在集气瓶口,不能伸入瓶中,A图中所示操作错误;稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散,一定不能把水注入浓硫酸中,B图中所示操作错误;酒精着火,可用湿布盖灭,C图中所示操作正确;用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,不能将pH试纸伸入待测液中,以免污染待测液,D图中所示操作错误。
4.如图是某化学反应的微观示意图,从示意图获取的信息不正确的是( )A.反应前后分子种类不发生改变 B.反应前后原子的种类与数目不发生改变C.参加反应的两种物质的分子个数比是1∶2 D.该反应的基本类型是化合反应A 由微粒的变化可知,反应前后分子种类发生了改变,A错误;由微粒的变化可知,反应前后原子的种类与数目不发生改变,B正确;由微粒的变化可知,参加反应的两种物质的分子个数比是1∶2,C正确;该反应由两种物质生成了一种物质,属于化合反应,D正确。
5.根据金属活动性顺序分析,下列描述或判断错误的是( )A.铁丝放到硫酸铜溶液中,表面有一层红色物质析出B.铜丝在空气中加热,生成黑色固体C.铁粉、镁带与等质量、等质量分数的稀盐酸反应,铁粉产生的气泡快,说明铁的活动性大于镁D.铁粉可以除去氯化亚铁溶液中的氯化铜C 铁金属活动性比铜活泼,所以铁丝放到硫酸铜溶液中,表面有一层红色物质析出,A正确;铜丝在空气中加热,生成黑色固体氧化铜,B正确;铁粉、镁带与等质量、等质量分数的稀盐酸反应,铁粉产生的气泡快,原因是铁与酸的接触面积大,不能说明铁的活动性大于镁,C错误;铁比铜活泼,铁粉可以除去氯化亚铁溶液中的氯化铜,D正确。
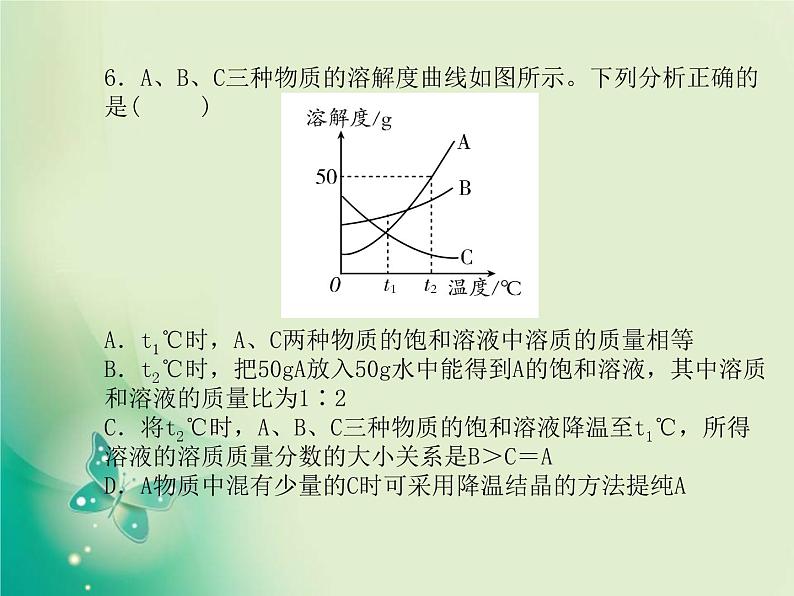
6.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是( )A.t1℃时,A、C两种物质的饱和溶液中溶质的质量相等B.t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶2C.将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=AD.A物质中混有少量的C时可采用降温结晶的方法提纯A
D t1℃时,相同质量的A、C两种物质的饱和溶液中溶质的质量相等,此处没有指出溶液的质量,故无法比较溶质质量的大小,A错误;t2℃时,A的溶解度是50g,把50gA放入50g水中能得到A的饱和溶液,只能溶解25g,故溶液质量是75g,其中溶质和溶液的质量比为25g∶75g=1∶3,B错误;将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,A、B的溶解度减小有晶体析出,t1℃时B的溶解度大于A的溶解度,故B的溶质质量分数大于A的溶质质量分数,C的溶解度随温度的降低而增大,故溶液组成不变,溶质质量分数与t2℃相同,据图可以看出,C的溶质质量分数最小,故所得溶液的溶质质量分数的大小关系是B>A>C,C错误;A的溶解度受温度的影响较大,随温度的升高而增大,C的溶解度随温度的升高而减小,故提纯A可用降温结晶的方法,D正确。
7.逻辑推理可以实现知识迁移,但不符合事实的推理会得出错误的结论。下列推理正确的是( )A.硝酸铵溶于水吸收大量的热,食盐溶于水也吸收大量的热B.氮肥氯化铵与碱研磨放出氨气,氮肥尿素与碱研磨也能放出氨气C.氢气与空气混合点燃可能爆炸,CO与空气混合点燃也可能爆炸D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐C 硝酸铵溶于水吸热,使溶液温度降低,而氯化钠溶于水不吸热,温度变化不明显,A错误;铵盐与碱研磨会放出氨气,氮肥尿素没有铵根离子,与碱研磨不会放出氨气,B错误;氢气和CO都属于可燃性的气体,不纯遇明火可能会发生爆炸,C正确;碳酸盐与盐酸反应放出气体二氧化碳,活泼金属也能与酸反应生成氢气,所以能与盐酸反应放出气体的物质不一定是碳酸盐,D错误。
8.从科学角度看,下列叙述正确的是( )A.用活性炭净水可以降低水的硬度 B.利用高压锅做饭快是因为压力大沸点低C.所有的杠杆使用都是为了省力 D.婴幼儿缺钙易患佝偻病D 活性炭能吸附水中的色素和异味,但并不能除去可溶性的钙镁化合物,故不能降低水的硬度,A不正确;压强增大水的沸点升高,高压锅就是利用这个原理,水的沸点升高后煮食物快,B不正确;杠杆根据动力臂与阻力臂长短的不同分为省力杠杆和费力杠杆两种,如理发剪刀就是费力杠杆,C不正确;钙是构成骨骼和牙齿的重要元素,婴幼儿缺钙易患佝偻病,D正确。
9.建立宏观和微观之间的联系是一种科学的思维方式。下列解释不正确的是( )A.金刚石、石墨物理性质存在明显差异的原因是它们的原子排列方式不同B.警用缉毒犬能根据气味发现毒品,是因为分子在不断运动C.压瘪的乒乓球放入热水中重新鼓起,是因为球内的气体分子体积增大D.酸有一些相似的性质,是因为在不同的酸溶液中都含有H+C 金刚石、石墨物理性质存在明显差异的原因是它们的原子排列方式不同,A选项解释正确;警用缉毒犬能根据气味发现毒品,是因为毒品中含有的分子是在不断运动的,向四周扩散,使训练有素的缉毒犬闻到毒品的气味,B选项解释正确;压瘪的乒乓球放入热水中重新鼓起,是因为分子间有间隔,在受热时间隔变大,分子的体积没有变化,C选项解释错误;酸有一些相似的性质,是因为在不同的酸溶液中都含有H+,D选项解释正确。
10.下列事例中,不是通过化学反应提供能量的是( )
B 蓄电池放电过程中是将化学能转化为电能,有其他物质生成,A属于化学变化;地热发电过程中没有其他物质生成,B属于物理变化;内燃机做功过程中是将内能转化为机械能,有其他物质生成,C属于化学变化;火箭升空过程中需要燃烧燃料,有其他物质生成,D属于化学变化。
11.下列选项符合图中从属关系的是( )
D 玻璃棒不是导体,A错误;臭氧是由一种物质组成的,属于纯净物,B错误;氯酸钾是由三种元素组成的化合物,不属于氧化物,C错误;新能源包括可燃冰、核能、地热能、潮汐能等,D正确。
12.如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中)。当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U型管中的a液面降低、b液面升高了。根据以上现象请你分析下列说法正确的是( )A.甲、乙一定分别是稀盐酸和大理石B.甲、乙有可能分别是水和硝酸铵C.石灰水变浑浊一定是因为发生了化学变化D.石灰水变浑浊有可能是发生了物理变化D 甲、乙分别是稀盐酸和大理石时,可以出现这些现象,但能生成二氧化碳的物质还有很多,A选项错误;甲、乙分别是水和硝酸铵时溶解吸热,温度降低,氢氧化钙溶解度升高,不会生成沉淀,也不会使容器内压强变大,B选项错误;石灰水变浑浊可能是化学变化导致的也可能是溶质析出导致的,C选项错误,D选项正确。
13.对图所示现象的解释不正确的是( ) B 合金的硬度大,黄铜的硬度比纯铜大,所以在纯铜上留下了较深的划痕,A正确;使氖管发光的是火线,B错误;只有具备了燃烧的三个条件才能燃烧,由于具备了燃烧的三个条件,因此白磷能在水下燃烧,C正确;流体压强的大小与流速有关,流速越快压强越小,所以人应站在安全线外,D正确。
14.如图是某大学研究小组研发的一种独特的复合材料——“石墨纸”,其成分以石墨为主,薄如纸张,比钢还要硬10倍且轻巧,还可以回收利用。下列说法错误的是( )A.与同体积的钢相比,石墨纸质量较小 B.与钢相比,石墨纸硬度较大C.石墨纸是绝缘体,不易导电 D.石墨纸是一种环保材料C 根据密度公式可得:m=ρV,由于石墨纸的密度小,故与同体积的钢相比,石墨纸的质量较小,A正确;“成分以石墨为主,薄如纸张,比钢要坚硬10倍”,体现了与钢相比,石墨纸的硬度较大,B正确;石墨易导电,属于导体,C错误;“可以回收再利用”,体现了石墨纸是一种环保材料,D正确。
15.如图,先关闭止水夹,将胶头滴管中的液体挤压到试管中,然后打开止水夹,发现烧瓶内的水沸腾起来。(1)胶头滴管内的液体是 氢氧化钠溶液 ,挤压到试管中后发生反应的化学方程式为 CO2+2NaOH===Na2CO3+H2O ;(2)烧瓶内的水沸腾的原因是 压强降低后,水的沸点降低 。先关闭止水夹,将胶头滴管中的液体挤压到试管中,然后打开止水夹,发现烧瓶内的水沸腾起来,是因为液体与烧瓶内的气体反应,使烧瓶内气体体积减小,压强减小,使水的沸点降低,胶头滴管内的液体可以是氢氧化钠溶液,烧瓶内的气体是二氧化碳,二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为CO2+2NaOH===Na2CO3+H2O。
二、填空及简答题(本大题共5个小题,共20分。每空1分)
16.水果含有果酸,如图所示在水果中插入两片不同金属制成的极板,就组成了一个水果电池,某科学兴趣小组对影响水果电池电压大小的因素进行了实验研究。(1)在水果中插入不同金属制成的极板,并保持两块极板之间的距离、极板与水果的接触面积不变,用电压表直接测量两块极板之间的电压,结果如下表:分析实验数据可以得出:在上述条件下,从金属活动性顺序看,所选用的两块极板材料之间的 活动性差别 越大,水果电池的电压越大;并且水果电池的电压还与 水果的种类 有关;(2)若该小组的同学选用一只橙子并用铜-锌作极板,研究水果电池的电压跟极板与水果的接触面积之间的关系时,应控制 两块极板之间的距离 不变。
17.化学源于生活,生活中很多现象蕴含着化学知识:(1)茶壶内的纱网,可将茶叶与茶水分离,该设计和化学实验中 过滤 (一种操作)原理相似;(2)合成纤维和羊毛是两种重要的衣服成分,它们可以用 灼烧 法区别;(3)山药中含有碱性皂角素,皮肤沾上会奇痒难忍,你认为可涂厨房中的 食醋 来止痒;(4)《生活饮用水卫生标准》中指出,饮用水消毒剂除了目前采用的液氯外,还补充了一氯胺(NH2Cl)、臭氧(O3)、二氧化氯(ClO2)等,二氧化氯中氯元素的化合价是 +4 ,NH2Cl氮元素与氢元素的质量比是 7∶1 。 (1)茶杯内的纱网可将茶叶与茶水分离,便于饮用,该设计原理类似化学实验操作中的过滤。(2)羊毛的主要成分是蛋白质,灼烧时能够产生烧焦羽毛的气味,而灼烧合成纤维时不产生这种气味。(3)食醋呈酸性,可以与碱性物质反应。(4)根据在化合物中正负化合价代数和为零,在ClO2中氧元素显-2价,设氯元素的化合价是x,则x+(-2)×2=0,解得x=+4。NH2Cl含有氮、氢、氯三种元素,其中氮元素与氢元素的质量比为14∶(1×2)=7∶1。
18.小雨同学想制作“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液,请回答下列问题:(1)若用氢氧化钠固体配制,需称取氢氧化钠 5 g(称量氢氧化钠的烧杯质量已知),配制时应选用 50 (选填“10”、“20”、“50”、“100”)mL的量筒量取蒸馏水;(2)用如图1所示的序号表示正确配制该溶液的操作顺序为 BACD ;(3)某同学用如图2所示的方法量取水,则他配制的溶液 小于 (填“大于”、“等于”或“小于”)10%;(4)配制好的氢氧化钠溶液应该贴好标签后 密封 保存在试剂瓶中。
(1)溶质质量=溶液质量×溶质的质量分数,配制50g质量分数为10%的氢氧化钠溶液,需氢氧化钠的质量为50g×10%=5g;溶剂质量=溶液质量-溶质质量,则所需蒸馏水的质量为50g-5g=45g(合45mL),应选用50mL的量筒。(2)配制50g质量分数为10%的氢氧化钠溶液,首先计算配制溶液所需氢氧化钠和水的质量,再称量所需的氢氧化钠和量取水,最后进行溶解,故正确配制该溶液的操作顺序为BACD。(3)某同学用如图所示的方法量取水,即仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小。(4)氢氧化钠溶液能与空气中的二氧化碳反应生成碳酸钠和水,为防止变质,配制好的氢氧化钠溶液应该贴好标签后密封保存在试剂瓶中。
19.如图是初中化学中常见物质间的转化关系,G是目前世界年产量最高的金属,F与H是组成元素相同的气体,I是常见的重要的建筑材料(反应条件、部分反应物和生成物均已略去)。(1)写出物质J的俗称 熟石灰(或消石灰) ;(2)H的一种用途 灭火 ;(3)G→D反应的基本类型是 置换反应 ;(4)写出E+F→G+H的化学方程式Fe2O3+3CO 2Fe+3CO2 。
G是目前世界年产量最高的金属,所以G是铁,A能通电生成C和D,故A是水,生成的C和D是氢气和氧气;F与H的组成元素相同且为气体,E和F反应生成铁和H,所以F为一氧化碳,H为二氧化碳,E为铁的氧化物;I是重要的建筑材料,J和二氧化碳反应生成I和水,所以J为氢氧化钙,I是碳酸钙;B和水反应生成氢氧化钙,所以B为氧化钙,E可能是氧化铁;水生成C和D,C能生成一氧化碳,铁可以生成D,所以C为氧气,D为氢气,带入框图,推断合理。(1)J是氢氧化钙,俗称熟石灰或消石灰;(2)H是二氧化碳,可以用于灭火;(3)铁和酸反应生成盐和氢气,属于置换反应;(4)F是一氧化碳,E是氧化铁,一氧化碳和氧化铁高温反应生成铁和二氧化碳。
20.小明在商场见到一种神奇的蜡烛,买回点燃后发现怎么也“吹不灭”,对这种蜡烛产生了浓厚的兴趣,于是带到学校和学习小组同学们进行了下列探究。【查阅资料】普通蜡烛由石蜡和烛芯制成的,吹不灭的蜡烛在普通蜡烛的烛芯外包裹了一层打火石。打火石是在某种金属中掺入少量稀土元素制成的合金,它的着火点只有150℃。当吹“灭”蜡烛时,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。【问题与思考】(1)吹不灭的蜡烛利用的原理是燃烧必须满足 温度达到可燃物的着火点 (填燃烧的条件之一),如果将这种蜡烛熄灭,应采用的方法是 用湿抹布盖灭或剪除灯芯等 ;(2)蜡烛芯外包裹的金属是什么?
三、实验探究题(本大题共1个小题,共7分)
【实验探究】吹不灭的蜡烛芯外的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,他们继续探究。(不考虑打火石中稀土元素对探究金属性质的影响)(1)同学们取该打火石,用砂纸打磨后,立即否认了该打火石中的金属是铜,那么他们观察到的是打火石呈现 银白 色。(2)取少量打磨后的打火石于试管中,加入稀盐酸,观察现象,经过对现象的分析后,他们认为该金属一定不是铁,他们观察到的现象是 溶液为无色 。【讨论交流】(1)为了进一步确定该金属的种类,小强提议用硫酸铜溶液进行实验,请你预测,将打火石加入到硫酸铜溶液后的现象是 打火石表面有红色固体附着,溶液颜色变浅(或变为无色) ,其中涉及到的化学方程式为 Mg+CuSO4===MgSO4+Cu (任写一个)。(2)同学们一致认为小强的方案不合理,经过讨论他们设计了下面的实验方案,确认了打火石中的金属是镁,他们的方案是 将打火石加入到硫酸铝溶液中,打火石表面有银白色固体附着 。
【问题与思考】(1)吹蜡烛主要是降低可燃物的温度,吹不灭的蜡烛利用的原理是燃烧必须满足:温度达到可燃物的着火点;要想使其熄灭可控制燃烧的条件完成;(2)【实验探究】打火石是银白色,而铜是紫红色的,所以该金属一定不是铜;根据氯化亚铁的溶液是浅绿色的事实分析可知:取灯芯加入盐酸,如果生成无色的溶液,则可说明有没有铁存在;【讨论交流】(1)实验排除了铜和铁,剩余镁和铝,活动性都大于铜,可以与铜反应将铜从硫酸铜溶液中置换出来,所以打火石表面有红色固体附着,溶液颜色变浅(或变为无色),化学方程式为Mg+CuSO4===MgSO4+Cu[或2Al+3CuSO4===Al2(SO4)3+3Cu]。(2)要验证打火石中的金属是镁,排除是铝,可以将打火石加入到硫酸铝溶液中,打火石表面有银白色固体附着。
21.为测定某纯碱样品(含少量的氯化钠)中碳酸钠的含量,小明称取该纯碱样品6g,充分溶解于水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示,求:(1)该纯碱样品中碳酸钠的质量分数(精确到0.1%);(2)所加入氯化钙溶液的溶质质量分数。
四、计算应用题(本大题共1个小题,共5分。解答时,要求有必要的文字说明、公式和计算步骤等,只写最后结果不得分)
泰安专版中考化学总复习第三部分模拟检测冲刺中考阶段检测卷二课件: 这是一份泰安专版中考化学总复习第三部分模拟检测冲刺中考阶段检测卷二课件,共35页。PPT课件主要包含了阶段检测卷二等内容,欢迎下载使用。
河北专版中考化学总复习第三部分模拟检测冲刺中考阶段检测卷二课件新人教版: 这是一份河北专版中考化学总复习第三部分模拟检测冲刺中考阶段检测卷二课件新人教版,共29页。
河北专版中考化学总复习第三部分模拟检测冲刺中考阶段检测卷一课件新人教版: 这是一份河北专版中考化学总复习第三部分模拟检测冲刺中考阶段检测卷一课件新人教版,共34页。












