
河北专版中考化学复习教材知识梳理模块一身边的化学物质课时7常见的酸和碱练习
展开1.(2017邵阳中考)下列试剂能将稀硫酸、氯化钠溶液、澄清石灰水三种溶液一步鉴别出来的是( D )
A.稀盐酸 B.二氧化碳
C.碳酸钙 D.石蕊溶液
2.下列说法正确的是( D )
A.盐酸能使紫色石蕊试液变蓝
B.浓硫酸露置于空气中,溶质的质量质量分数变大
C.长期露置于空气中的固体氢氧化钠,其成分不会发生变化
D.打开盛浓盐酸的试剂瓶,瓶口会产生白雾
3.(2017泰安中考)类推是一种重要的学习方法,但如果不具体问题具体分析就会产生错误的结论。下列类推结论错误的是( A )
①CO能与Fe2O3反应生成Fe,CO也能与CuO反应生成Cu;②NaOH溶液能使无色酚酞溶液变红色,Cu(OH)2也能使无色酚酞溶液变红色;③有机化合物含碳元素,则含碳元素的化合物一定是有机化合物;④中和反应生成盐和水,但生成盐和水的反应不一定是中和反应;⑤碱的溶液呈碱性,则呈碱性的溶液一定是碱的溶液。
A.②③⑤ B.①②⑤ C.①⑤ D.③④⑤
4.(2017重庆中考A卷)某实验小组将Ba(OH)2溶液逐滴滴入硫酸溶液中,溶质的质量与加入的Ba(OH)2溶液的质量关系如图所示。下列说法错误的是( C )
A.a点溶液为酸性
B.b点恰好完全反应
C.c点溶液的溶质为硫酸
D.b、c两点沉淀质量相等
5.下列说法中不正确的是( A )
A.纯碱是发酵粉的主要成分
B.硫酸可用于制铅酸蓄电池
C.烧碱可用于生产炉具清洁剂
D.熟石灰可用于改良酸性土壤
6.(2017滨州中考)下列图像能正确反映其对应操作中各量变化关系的是( C )
A.图①是利用二氧化锰分解过氧化氢制氧气
B.图②是向一定温度的饱和氢氧化钙溶液中不断加入氧化钙固体
C.图③是向pH=1的酸溶液中不断加水
D.图④是向一定质量的稀硫酸中加入锌粒
二、填空及简答题
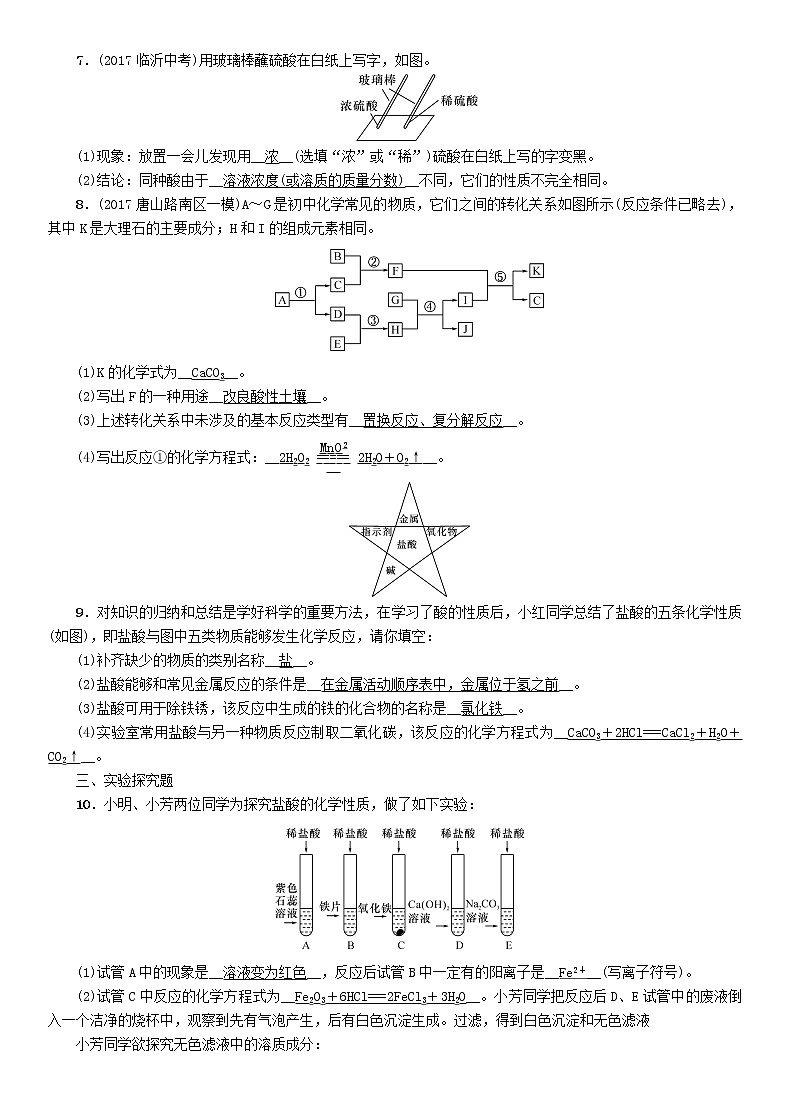
7.(2017临沂中考)用玻璃棒蘸硫酸在白纸上写字,如图。
(1)现象:放置一会儿发现用__浓__(选填“浓”或“稀”)硫酸在白纸上写的字变黑。
(2)结论:同种酸由于__溶液浓度(或溶质的质量分数)__不同,它们的性质不完全相同。
8.(2017唐山路南区一模)A~G是初中化学常见的物质,它们之间的转化关系如图所示(反应条件已略去),其中K是大理石的主要成分;H和I的组成元素相同。
(1)K的化学式为__CaCO3__。
(2)写出F的一种用途__改良酸性土壤__。
(3)上述转化关系中未涉及的基本反应类型有__置换反应、复分解反应__。
(4)写出反应①的化学方程式:__2H2O2eq \(=====,\s\up7(MnO2))2H2O+O2↑__。
9.对知识的归纳和总结是学好科学的重要方法,在学习了酸的性质后,小红同学总结了盐酸的五条化学性质(如图),即盐酸与图中五类物质能够发生化学反应,请你填空:
(1)补齐缺少的物质的类别名称__盐__。
(2)盐酸能够和常见金属反应的条件是__在金属活动顺序表中,金属位于氢之前__。
(3)盐酸可用于除铁锈,该反应中生成的铁的化合物的名称是__氯化铁__。
(4)实验室常用盐酸与另一种物质反应制取二氧化碳,该反应的化学方程式为__CaCO3+2HCl===CaCl2+H2O+CO2↑__。
三、实验探究题
10.小明、小芳两位同学为探究盐酸的化学性质,做了如下实验:
(1)试管A中的现象是__溶液变为红色__,反应后试管B中一定有的阳离子是__Fe2+__(写离子符号)。
(2)试管C中反应的化学方程式为__Fe2O3+6HCl===2FeCl3+3H2O__。小芳同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成。过滤,得到白色沉淀和无色滤液
小芳同学欲探究无色滤液中的溶质成分:
小芳同学分析得出无色滤液中一定不含HCl,理由是__混合后,先有气泡产生,后有白色沉淀生成,说明盐酸被消耗完__。
【提出问题】无色滤液的溶质是什么?
【做出猜想】①NaCl;②NaCl和CaCl2;③NaCl、CaCl2和Na2CO3;④NaCl和Na2CO3。
小明认为猜想__③__一定不正确。
【进行实验】
11.某化学实验小组欲探究盐酸、氢氧化钙两种物质的化学性质,取8支试管分别用A~H编号后,做如下实验。
(1)实验中观察到有气泡出现的试管是__CD__,有沉淀生成的试管是__GH__。
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式__Ca(OH)2+2HCl===CaCl2+2H2O__。
(3)实验后某试管中为红色溶液,当向其中加入过量的__Ca(OH)2__后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是__紫色石蕊溶液__。
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现,则该滤液中的溶质是__Na2CO3、NaOH__。
四、计算应用题
12.(2017邯郸中考模拟)为测定的某氢氧化钠样品(含少量氯化钠)中氢氧化钠的质量分数。称取5 g样品,加水完全溶解后,继续加入溶质质量分数为10%的稀盐酸,记录的实验数据如下表,请回答下列问题。
(1)计算样品中氢氧化钠的质量,应选择实验序号__②__的数据最合适。
(2)计算样品中氢氧化钠的质量分数。
解:设样品中氢氧化钠的质量为x。
NaOH+HCl===NaCl+H2O
40 36.5
x 36.5 g×10%
eq \f(40,36.5)=eq \f(x,36.5 g×10%) x=4 g
样品中氢氧化钠的质量分数为:eq \f(4 g,5 g)×100%=80%。
答:样品中氢氧化钠的质量分数为80%。
实验步骤
实验现象
实验结论
取少量滤液于试管中,滴加少量碳酸钠溶液
无明显现象
取少量滤液于试管中,滴加少量①__稀盐酸__
有气泡产生
猜想②__④__成立
实验序号
加入稀盐酸的质量
溶液的pH
①
20 g
pH>7
②
36.5 g
pH=7
③
50 g
pH<7
河北专版中考化学复习教材知识梳理模块一身边的化学物质课时8盐化肥练习: 这是一份河北专版中考化学复习教材知识梳理模块一身边的化学物质课时8盐化肥练习,共4页。试卷主要包含了选择题,填空及简答题,实验探究题,计算应用题等内容,欢迎下载使用。
河北专版中考化学复习教材知识梳理模块一身边的化学物质课时5金属材料及金属的冶炼与防护练习: 这是一份河北专版中考化学复习教材知识梳理模块一身边的化学物质课时5金属材料及金属的冶炼与防护练习,共4页。试卷主要包含了选择题,填空及简答题,实验探究题,计算应用题等内容,欢迎下载使用。
河北专版中考化学复习教材知识梳理模块一身边的化学物质课时6金属的化学性质练习: 这是一份河北专版中考化学复习教材知识梳理模块一身边的化学物质课时6金属的化学性质练习,共4页。试卷主要包含了选择题,填空及简答题,实验探究题,计算应用题等内容,欢迎下载使用。












