




2022版高考化学选考山东专用一轮总复习课件:专题十一化学能与电能的转化 —应用篇
展开一、二次电池(可充电电池)充电及放电分析1.二次电池放电(1)若给出新型电池的装置图,先找出电池的正、负极,即找出氧化剂和还 原剂,再结合电解质确定出还原产物和氧化产物,判断相应的电极反应式 的正误。(2)若给出新型电池的总反应式,分析总反应式中各元素化合价的变化情 况,找出氧化剂及其对应的还原产物,以及还原剂及其对应的氧化产物,然 后考虑电解质是否参加反应,判断电极反应式的正误。2.二次电池充电充电时阴、阳极的电极反应式是该电池放电时的负、正极反应式的 “逆反应”。
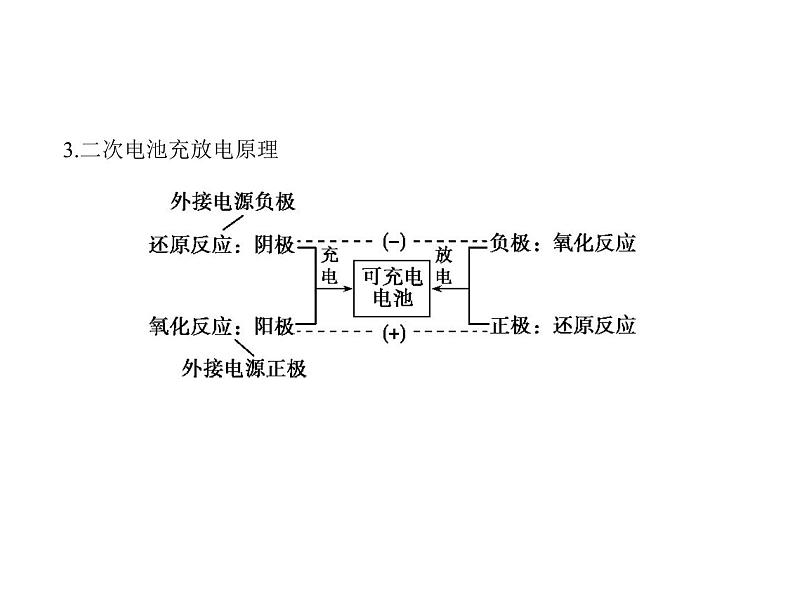
3.二次电池充放电原理
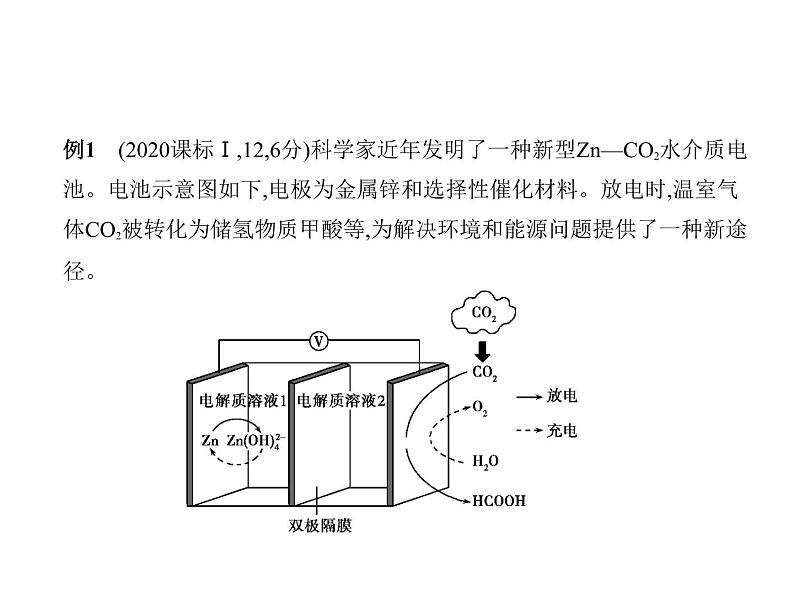
例1 (2020课标Ⅰ,12,6分)科学家近年发明了一种新型Zn—CO2水介质电 池。电池示意图如下,电极为金属锌和选择性催化材料。放电时,温室气 体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途 径。
下列说法错误的是 ( )A.放电时,负极反应为Zn-2e-+4OH- Zn(OH B.放电时,1 ml CO2转化为HCOOH,转移的电子数为2 mlC.充电时,电池总反应为2Zn(OH 2Zn+O2↑+4OH-+2H2OD.充电时,正极溶液中OH-浓度升高
解析 放电时,CO2转化为HCOOH,CO2被还原,放电时右侧电极为正极,左 侧电极为负极,负极上Zn被氧化为Zn(OH ,电极反应式为Zn-2e-+4OH- Zn(OH ,A正确;放电时,CO2转化为HCOOH,C元素化合价降低2价,1 ml CO2转化为HCOOH时,转移电子数为2 ml,B正确;充电时,正极(阳 极)上H2O转化为O2,负极(阴极)上Zn(OH 转化为Zn,总反应为2Zn(OH 2Zn+O2↑+4OH-+2H2O,C正确;充电时,正极(阳极)电极反应式为2H2O-4e- 4H++O2↑,溶液中H+浓度增大,则OH-浓度降低,D错误。
题目价值 借助新型Zn—CO2水介质电池对二次电池的工作原理进行分 析,对复杂的化学问题情境中的关键要素进行分析,构建解题模型。
二、电化学计算1.解题思路:各电极上转移电子的物质的量相等(电子转移守恒)。2.计算方法
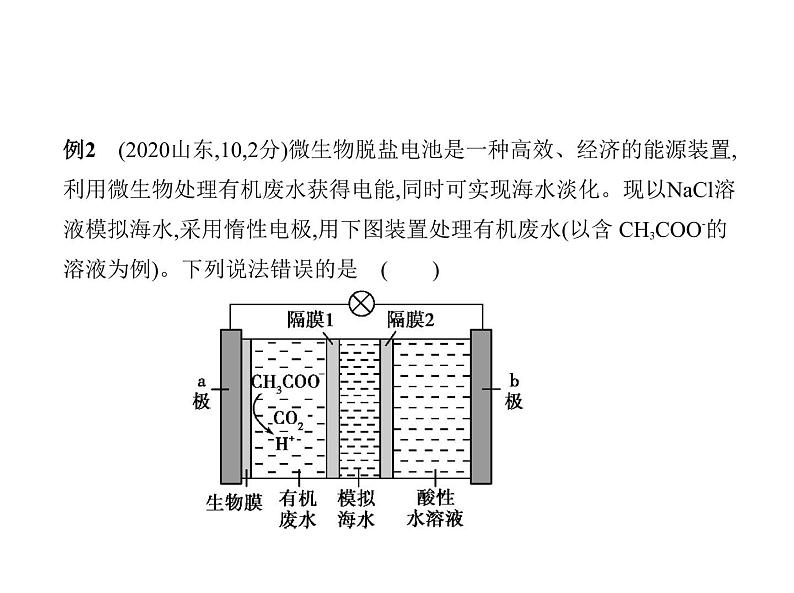
例2 (2020山东,10,2分)微生物脱盐电池是一种高效、经济的能源装置, 利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶 液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的 溶液为例)。下列说法错误的是 ( )
A.负极反应为 CH3COO-+2H2O-8e- 2CO2+7H+B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜C.当电路中转移1 ml电子时,模拟海水理论上除盐58.5 gD.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1
解析 结合题给微生物脱盐装置,可知a极上CH3COO-转化为CO2,C元素 被氧化,故a极为负极,电极反应式为CH3COO-+2H2O-8e- 2CO2↑+7H+,A正确;淡化海水过程中,模拟海水中的氯离子向负极(a极)移动,则隔膜1 为阴离子交换膜,钠离子需要向正极(b极)移动,则隔膜2为阳离子交换膜, B错误;当电路中转移1 ml电子时,模拟海水中会有1 ml Cl-和1 ml Na+ 分别移向负极和正极,可除去1 ml NaCl,质量为58.5 g,C正确;b极为正极, 水溶液显酸性,电极反应式为2H++2e- H2↑,当转移8 ml电子时,正极产生4 ml H2,负极产生2 ml CO2,物质的量之比为2∶1,D正确。
题目价值 本题以原电池工作原理在污水处理、海水淡化上的应用为 情境,不仅将化学理论应用于生产实际,也体现了科学态度与社会责任的 学科核心素养。
“隔膜”在化工生产中的创新应用近几年高考中,不管是原电池还是电解池,大部分都含有离子交换膜,离子 交换膜对溶液中离子具有选择透过性,根据透过离子的类型,离子交换膜 可以分为阳离子交换膜、阴离子交换膜、质子交换膜等多种。1.离子交换膜的类型和作用
2.多室电解池多室电解池是利用离子交换膜的选择透过性,即只允许带某种电荷的离 子通过而限制带相反电荷的离子通过,将电解池分为两室、三室、多室 等,以达到浓缩、净化、提纯及电化学合成的目的。3.考情趋势(1)“膜”数量变化:由“单膜”→“双膜” →“多膜”,进行“膜”的数 量变化。(2)“膜”种类变化:由“阴、阳离子交换膜” →“质子交换膜” →“高 聚物隔膜”→“双极隔膜”等,进行“膜”的种类变化。(3)“膜”作用变化:由“离子交换”→“物质制备”→“分离提纯”等, “膜”的作用发生变化。
4.离子交换膜类型的判断方法(1)写出阴、阳(或正、负)两极上的电极反应。(2)依据电极反应式确定该电极附近哪种离子剩余。(3)根据电极附近溶液呈电中性,从而判断出离子移动的方向。(4)根据离子移动的方向,确定离子交换膜的类型。
例 (2020昌乐二中高三模拟,11)酒石酸(RH2)分子的结构简式为 。它可以通过电渗析法制备。“三室电析”工作原理如图所示(电极均为惰性电极)。下列说法正确的是 ( ) A.A为阴离子交换膜,B为阳离子交换膜
B.阴极每生成标准状况下22.4 L的气体时,转移的电子数为NAC.阳极反应为2H2O+4e- O2↑+4H+D.若用铅蓄电池作电源,当生成1 ml RH2时,理论上电源的负极增重96 g
解析 根据题意制备酒石酸,电解过程中,R2-应向阳极移动与阳极室产生 的氢离子结合生成酒石酸,Na+向阴极移动,故A为阳离子交换膜,B为阴离 子交换膜,A错误;阴极电极反应式为2H2O+2e- H2↑+2OH-,每生成标准状况下22.4 L H2,即1 ml H2,转移电子的物质的量为2 ml,即2NA,B错误; 阳极失电子发生氧化反应,反应式应为2H2O-4e- O2↑+4H+,C错误;生成1 ml RH2时,转移2 ml电子,铅蓄电池电源负极反应为Pb-2e-+S PbSO4,根据电子转移守恒,负极增重1 ml×96 g·ml-1=96 g,D正确。
山东专用高考化学一轮复习专题十一化学能与电能的转化_基础篇课件: 这是一份山东专用高考化学一轮复习专题十一化学能与电能的转化_基础篇课件,共28页。
2022版高考化学选考山东专用一轮总复习课件:专题四氧化还原反应 —应用篇: 这是一份2022版高考化学选考山东专用一轮总复习课件:专题四氧化还原反应 —应用篇,共11页。PPT课件主要包含了实践探究,答案D,答案C等内容,欢迎下载使用。
2022版高考化学选考山东专用一轮总复习课件:专题十一化学能与电能的转化 —基础篇: 这是一份2022版高考化学选考山东专用一轮总复习课件:专题十一化学能与电能的转化 —基础篇,共28页。












